Glycerol
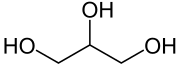
| Glycerol | |||||||
 | |||||||
 | |||||||
| Všeobecné vlastnosti | |||||||
| Sumárny vzorec | C3H8O3 | ||||||
| Synonymá | propan-1,2,3-triol | ||||||
| Fyzikálne vlastnosti | |||||||
| Molárna hmotnosť | 92,0932 g/mol | ||||||
| Teplota topenia | 17,8 °C | ||||||
| Teplota varu | 290 °C | ||||||
| Hustota | 1,26 g/cm³ | ||||||
| |||||||
| Ďalšie informácie | |||||||
| Číslo CAS | 56-81-5 | ||||||
| Pokiaľ je to možné a bežné, používame jednotky sústavySI. Ak nie je hore uvedené inak, údaje sú zanormálnych podmienok. | |||||||
Glycerol,aleboglycerín,systematickým názvompropán-1,2,3-triol,je hygroskopická bezfarebnáviskóznakvapalinabez zápachu, sladkej chuti. Je dôležitou biogénnouorganickou zlúčeninou,lebo je vo forme svojichesterovsúčasťoutukov.
Chemické a fyzikálne vlastnosti
[upraviť|upraviť zdroj]Glycerol je trojsýtnyalkohol.Jeho oxidáciou vzniká celý rad látok. Šetrnou oxidáciou jednej primárnej alkoholickej skupiny vzniká jednoduchýmonosacharid,aldotriózaglyceraldehyd
- 2 HO-CH2-CH(OH)-CH2-OH + 2 O2→ 2 HO-CH2-CH(OH)-CHO + H2O.
Naopak oxidáciou sekundárnej alkoholickej skupiny vzniká iný monosacharid,ketotriózadihydroxyaceton
- 2 HO-CH2-CH(OH)-CH2-OH + 2 O2→ 2 HO-CH2-CO- CH2-OH + H2O.
Plnou oxidáciou jednej primárnej alkoholickej skupiny dostanemekyselinu glycerovú
- HO-CH2-CH(OH)-CH2-OH + O2→ HO-CH2-CH(OH)-COOH + H2O.
Úplnou oxidáciou oboch primárnych alkoholických skupín vznikákyselina tartronová
- HO-CH2-CH(OH)-CH2-OH + 2 O2→ HOOC-CH(OH)-COOH + 2 H2O.
Úplnou oxidáciou vzniká najjednoduchšia ketodikyselina,kyselina mesoxalová
- 2 HO-CH2-CH(OH)-CH2-OH + 5 O2→ 2 HOOC-CO-COOH + 6 H2O.
Zahrievaný bez prístupu vzduchu odštepuje vodu a mení sa na nenasýtenýaldehydakrolein(propenal)
- HO-CH2-CH(OH)-CH2-OH → H2C=CH-CH=O + 2 H2O.
Pôsobením nitračných činidiel (napr. zmesi koncentrovanejkyseliny dusičnejakyseliny sírovej) na glycerol vzniká trinitrát glycerolu, známejší pod názvomnitroglycerín
- HO-CH2-CH(OH)-CH2-OH + HNO3→ O2NO-CH2-CH(ONO2)- CH2-ONO2+ 3 H2O,
ktorý je zložkou raduvýbušnín(napr.dynamitu) astrelivín(napr.bezdymného strelného prachu).
Vďaka prítomnosti hydroxylových skupín je molekula glycerolu polárna a preto sa neobmedzene miesi svodoua jednoduchými alkoholmi (napr.metanolomaetanolom). V nepolárnych rozpúšťadlách (napr.benzín) sa nerozpúšťa.
Výroba
[upraviť|upraviť zdroj]Glycerol vzniká prisaponifikáciialebotransesterifikácii.
Saponifikácia
[upraviť|upraviť zdroj]Hlavným zdrojom glycerolu boli prírodné tuky. Pri výrobe mydla sa pôsobenímhydroxidu sodnéhoalebodraselnéhotuky štepia na glycerol a zmes alkalických solí alifatickýchkyselín,ktoré sú podstatoumydiel:
Transesterifikácia
[upraviť|upraviť zdroj]Pri výrobe bionafty je glycerol vedľajším produktom v podiele asi 10 %. So vzrastajúcim objemom výroby bionafty vo svete tak vzrastá aj objem vyrobeného glycerolu.
Biochémia
[upraviť|upraviť zdroj]
Glycerol vzniká vedľa etanolu v procese kvasenia glukózy z 1,3-dihydroxyacetonu, resp. 1,3-dihydroxyacetonfosfátu, ktorý je bežným produktom štiepeniaglukózyenzýmatickouredukciou redukovanou formou β-nikotinamidadenindinukleotidu (NADH) za prítomnosti glycerolhydrogenasy.
Preto je tiež vedľajším produktom prípravyetanoluzglukózyfermentácioukvasinkamiSaccharomyces cerevisiae.Keď prebieha kvasenie glukózy za prítomnosti väčšieho množstva siričitanov, blokuje sa čiastočne redukciaacetaldehyduna etanol a vo výslednej zmesi sa zvýši obsah glycerolu. Podobne možno produkciu glycerolu na úkor etanolu zvýšiť, keď prebieha fermentácia v neutrálnom alebo slabo zásaditom prostredí.
Omnoho väčšiu produkcie glycerolu možno však dosiahnuť pri použití iných druhov mikroorganizmov, napr.Debaryomyces mogii,Saccharomyces rouxii,Saccharomyces mellis,Pichia miso,Pichia farinosa,Torulopsis magnoliae,Zygosaccharomyces acidificiensa i.
Fyziologické pôsobenie
[upraviť|upraviť zdroj]Glycerol je slabo jedovatý. V menších dávkach spôsobuje bolesti hlavy, žalúdočné problémy a zvracanie. Vo väčších dávkach môže spôsobiť poškodenie pečene. Najnižšia toxická dávka podaná orálne u človeka činí približneLDLo= 1,5 g/kg živej hmotnosti, čo znamená, že priemerný človek by ho musel požiť najmenej 90 až 120 g, aby sa u neho prejavili symptómy otravy. V nízkych koncentráciách je prakticky neškodný.
V zriedenom stave sa používa k zvlhčovaniu pokožky a slizníc, lebo viaže atmosférickú vlhkosť a tým ju prenáša do povrchu tela; naopak použitie čistého glycerínu je nevhodné, pretože naopak z pokožky odčerpáva vlhkosť a tým ju vysušuje.
Použitie
[upraviť|upraviť zdroj]Glycerol sa používa o. i. v kozmetických výrobkoch, hlavne ako prísada v hydratačných krémoch a mydlách, ako prísada do zubných pást, pri výrobe plastických hmôt hlavne ako zmäkčovadlo, liečiv, žuvačiek, pást, farbív a výbušnín. Používa sa tiež pri výrobe bezvodého etanolu pre odstránenie prímesi vody.
Je súčasťou nemrznúcich zmesí, väčšinou v kombinácii setylénglykolom.
V potravinárskom priemysle sa užíva ako prísada pre úpravu nápojov a menej kvalitnýchvín,ako sladidlo napr. v šľahačkách v bombičkách, ako zmäkčovadlo želé a iných cukroviniek a pod.
Ako súčasť potravín má označenie E 422.
V lekárstve sa užíva pri liečbe opuchov mozgu ako prísadainfúzií,na znižovanie vnútroočného tlaku, pri zápchach, na zmäkčenie stolice vo forme glycerínových čapíkov alebo ako súčasť klystíru.
Pôvod mena
[upraviť|upraviť zdroj]Názov je odvodený od dvoch význačných vlastností glycerolu, a to jeho sladkej chuti a značnej viskozity. Základom súgréckeslovoγλυκύς,glykys,po slovenskysladkýalatinskéslovocera,tj.vosk.

