Reaktivna kisikova spojina
Reaktivne kisikove spojinealireaktivne kisikove zvrsti(angleškoreactive oxygen species, ROS) so visoko reaktivniprosti radikali,ki vsebujejokisikoveionealiperokside.Nastanejo kot stranski produkt normalnepresnove(metabolizma) kisika in imajo pomembno vlogo pri celičnem signaliziranju, poleg tega pa jihlevkocitiizrabljajo kot obrambni mehanizem proti različnimmikrobom(npr. protibakterijam), tj. imajo citotoksično delovanje.[1][2]Po drugi strani lahko med okoljskim stresom (npr. izpostavljenostultravijoličnim žarkomalitoploti) količine teh spojin zelo narastejo, kar povzroči obsežne poškodbeceličnihstruktur; tovrstno stanje imenujemooksidativni stres.Lahko nastanejo tudi preko zunanjih virov (eksogeni izvor), kot jeionizirajoče sevanje.
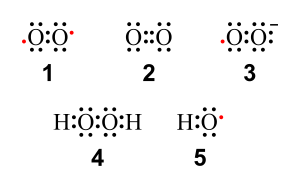
Z biološkega vidika so pomembne predvsem naslednje 3 spojine:
- vodikov peroksid(H2O2),
- superoksidali superoksidni anionski radikal (O2•–),
- hidroksilni radikal(OH•–).
Nastanek
urediCelično dihanje
urediReaktivne kisikove spojine nastajajo v telesu neprestano, v glavnem med prenosomelektronovpodihalni verigivmitohondrijih,torej kot nezaželeni produkti pri nepopolnemceličnem dihanju.V aktivnih mitohondrijih se približno 0,1–4 % celotnega vdihanega kisika pretvori v reaktivne kisikove spojine.[3][4][5]
Reaktivne spojine nastanejo povečini pri prenosu elektronov izubikinona(QH2) nakompleks IIIter izkompleksa Ina ubikinon. Prenos vključuje semikinonski radikal (QH•), ki lahko odda elektron kisiku (O2):[3][4][5]
Nastali superoksid deluje naakonitazo,ki sprostiželezovekatione v fero obliki (Fe2+). Superoksid in vodikov peroksid lahko reagirata poHaber-Weissovi reakciji,pri čemer so železovi ionikatalizatorjireakcije. Nastanejo kisik, hidroksidni anion inhidroksilni radikal,ki je še reaktivnejši od superoksida.[3][4][5]
Vodikov peroksid lahko poFentonovi reakcijirazpade nahidroksilni anioninhidroksilni radikal,katalizatorji reakcije pa so ioni Fe2+.[3][4][5]
Ksenobiotiki
urediVeliko radikalov lahko nastane tudi zaradi vnosa različnih telesu tujih snovi oz.ksenobiotikov,kot sopesticidi,katran,umetna barvila,konzervansiinzdravilaali pa zaradi izpostavljenostiionizirajočemu sevanju.[6]
Nevtralizacija reaktivnih kisikovih spojin
urediKljub temu, da radikali v nas nastajajo neprestano, naše telo ne postane žarko, tako kot se npr. pokvari maščoba nazraku.V živih bitjih so se namreč razvili mnogi mehanizmi, ki zmanjšujejo nastajanje radikalov, jih odstranjujejo in popravljajo škodo, ki so jo ti že povzročili. Tovrstni mehanizmi potrebujejo za svoje delovanje različne snovi, ki jih dobimo s hrano, predvsem ssadjem,zelenjavo,pa tudi z zdravilnimi rastlinami -vitamin C(askorbinska kislina),vitamin E(alfa tokoferol),provitamin A(beta karoten),cink(Zn) inselen(Se).
Za preprečitev poškodb sprvaencimsuperoksid dismutaza(SOD) pretvori superoksid v vodikov peroksid po naslednji reakciji:
Dedni dejavniki in način življenja vplivajo na količino SOD v telesu pri posamezniku. Če telo ne uspe proizvesti zadostne količine SOD pod 5nmol/ml seruma, se začne sekundarna oksidativna škoda, ki vodi v degenerativne bolezni.
Po tem obstajata dve poti nevtralizacije vodikovega peroksida. Po prvi encimkatalaza,ki se nahaja vperoksisomih,katalizira pretvorbo H2O2v neškodljivo vodo in kisik:
ali pa encimglutation peroksidazakatalizira redukcijo vodikovega peroksida v dve molekuli vode, v vlogi reducenta pa nastopaglutation(GSH):
Oksidirani glutation (GSSG) encimglutation reduktazapretvori nazaj v reducirano obliko, pri čemer uporabi elektrone iz reducirane oblikenikotinamid adenin dinukleotid fosfata(NADPH + H+).
Nevtralizacijo lahko povzamemo po naslednji shemi (upoštevana je samo katalazna pot):
Funkcije
urediObramba pred mikroorganizmi
urediAktiviranimakrofagiinnevtrofilcilahko proizvajajo velike količine superoksida in njegovih derivatov preko fagocitnih izoformNADPH oksidaze.V primeruvnetjalahko znaša koncentracija vodikovega peroksida v aktiviranih makrofagih od 10-100µM.Obsežna proizvodnja reaktivnih spojin imenujemo »oksidativni izbruh« in ima pomembno vlogo v obrambi pred okoljskimipatogenimimikrobi. Poleg tega vodita kombinirani aktivnosti NADPH oksidaze inmieloperoksidazedo nastankahipoklorove kisline(HOCl), ki je eden od najmočnejših fiziološkihoksidantovin protimikrobnih sredstev. Fiziološke koncenracije reaktivnih spojin lahko tudi modulirajo različne signalne kaskade in tako ojačajo imunske funkcije limfocitov (amplifikacija signalov). V limfocitih je eden od pomembnih virov nastanka ROS tudi encim5-lipooksigenaza(5-LO), ki je sicer znana po svoji vlogi v biosintezilevkotrienov.[1][2]
Aktivacijo NAPDH oksidaze lahko inducirajo produkti mikrobov, kot so bakterijskilipopolisaharidiinlipoproteiniali pacitokini,kot jeinterferon gama(IFN-γ).[1]
Signalizacijske lastnosti
urediROS proizvajajo tudi mnoge druge nefagocitne izoforme NAD(P)H oksidaz in imajo pomembno vlogo v uravnavanju (regulaciji) znotrajceličnih (intracelularnih) signalnih kaskad v različnih tipih celic, kot sofibroblasti,endotelijske celice,gladke mišične celicekrvni žil,kardiomiocititer celiceščitnice.Oksidaze lahko aktivirajo različni dejavniki: v kardiomiocitih so to lahkohormoni(angiotenzin II), hemodinamične sile ali lokalne spremembe presnove (metabolizma).[1]
Glede na različne raziskave naj bi nastanek ROS v primeruhipoksijeuravnaval dihanje preko delovanja na karotidna telesca (tipparaganglijev,ki zaznavajo med ostalimparcialni tlakkisika), ter nastanekeritrocitovpreko aktivacijetranskripcijskih faktorjevHIF(angleškohypoxia induced factor), ki delujejo nagen,ki nosi zapis (kodira) zaeritropoetin(EPO).[1]
Reaktivne spojine naj bi uravnavale tudi celično adhezijo (npr. adhezijolevkocitovna endotelijske celice) in induciraleapoptozo.[1]
Rastline in ROS
urediPrirastlinahse v primeru vdora mikrobov sproži t. i.hipersenzitivni odziv,ki vodi v nastanek superoksida in vodikovega peroksida. Le-ta bodisi delujeta na gene, ki so vključeni v obrambo organizma, bodisi vodita celice v apoptozo in imata s tem prav tako zaščitno vlogo.[1]
Poškodbe celičnih struktur zaradi delovanja ROS
urediGlavna reaktivna spojina, ki povzroča poškodbe celičnih struktur, je hidroksilni radikal. Le-ta povzroča poškodbe dednega materiala, tj.RNKinDNK(še posebejmitohondrijsko DNK,mtDNK),[7]pri čemer napada takodeoksiribozokot tudipurinskeinpirimidinskebaze, ter poškodbelipidovpreko lipidne peroksidacije inbeljakovin,npr. preko oksidacijetiolnihskupin (-SH), pri čemer nastanejo prečne vezi v oblikidisulfidnih vezi(-S-S-), zaradi česar se tvorijo agregati proteinov in postanejo nefunkcionalni.
Lipidna peroksidacija
urediNajbolj pogosta škoda, nastala zaradi prostih radikalov, vključuje oksidacijo lipidov. Gre za proces, ki onesposablja funkcionalnost membran in homeostazo organizma. Maščobe hitro reagirajo s prostimi radikali in tako se razširi lipidna peroksidacija ter vse ostale verižne reakcije prostih radikalov. Zaradi poškodovanecelične membrane(plazmaleme) celica umre, saj ne more uvažati hranil in kisika iz krvi ter izvažati odpadnih snovi inogljikovega dioksidav kri, poleg tega pa celica ni zmožna prepoznati prisotnost sosednjih celic, zaradi česar lahko začne nenadzorovanoproliferirati,kar pripomore k nastankutumorja.
Peroksidacijapoteče, ko kakršen koli prosti radikal napade nenasičenomaščobno kislino(npr. v membrani). Čim bolj nenasičena je ta maščobna kislina (tj. čim več dvojnih vezi ima), tem bolj je dovzetna za napade prostih radikalov. Radikal na koncu maščobne kisline reagira z vodikom. Sprosti se voda, na koncu maščobne kisline pa nastane ogljik-centriran lipidni radikal. Ta radikal hitro reagira z O2.Posledica je nastanek lipidnega peroksilnega radikala. Le-ta lahko napade druge maščobne kisline in tako nadaljuje verigo omenjenih reakcij, sam pa se pretvori v lipidni peroksid (CO2H). Lipidni peroksid se začne nabirati v celični membrani ter jo naredi nestabilno in nepropustno zaione.Lipidni peroksilni radikali pa poleg membranskih lipidov napadajo tudi membranske proteine in s tem poškodujejo encime,receptorje,signalni sistem in podobno.
Klinični pomen
urediS starostjo učinkovitostavtofagijeupada, zato se kopičijo poškodovani in starimitohondriji,ki prepuščajo ione in tako povzročijo nastanek reaktivnih kisikovih spojin. Ti so vzrok za razne spremembe v celici, kot so poškodbe DNK, peroksidacija lipidov v membranah, tvorbe prečnih vezi med proteini, delujejo pa tudi tako, da skrajšujejotelomere.Spremembe v koncentraciji ROS so lahko tudi posledica mutacij encimov, ki so udeleženi v nevtralizaciji teh spojin (npr.superoksid dismutaza).[1][4]
ROS so asociirani s številnimi boleznimi, kot so:[1]
- rakasta obolenja[7]zaradi poškodb DNK in s tem njihove vlogekarcinogenov;
- sladkorna bolezen:hiperglikemijainducira nastanek ROS in še poslabša stanje ali dodatno povzroči različne zaplete;
- ateroskleroza:vezava oksidiranihLDLlipoproteinov stimulira izražanje gena za superoksid dizmutazo, s tem pa je povečan nastanek H2O2;
- nevrodegenerativne bolezni:Downov sindromali trisomija 21.kromosomazaradi lokalizacije gena za Cu/Zn-superoksid dizmutazo na 21. kromosomu in v zvezi s tem njegovo povečano izražanje,Alzheimerjeva bolezenzaradi povezave med peroksidacijo lipido in nastankom amiloidnih agregatov;
- revmatoidni artritis;
- okužbasHIV:za tovrstno okužbo je značilen tudi povečan katabolizemcisteinav sulfate, zaradi česar je količina cisteina, s tem pa tudi glutationa (ker je prekurzor tega antioksidanta) zmanjšana, delovanje lifmocitov pa je še dodatno okrnjeno.
Glej tudi
urediOpombe in sklici
uredi- ↑1,01,11,21,31,41,51,61,71,8Dröge, Free radicals in the physiological control of cell function, 2005.
- ↑2,02,1Rada, B. & Leto, T.L. (2008).»Oxidative innate immune defenses by Nox/Duox family NADPH oxidases«.Contrib. Microbiol.15:164-87.
- ↑3,03,13,23,3Nelson, D.L.; Cox, M.M. (2008).Lehninger Principles of Biochemistry(5 izd.). NY: W.H. Freeman and Company. str.720-721.COBISS68330753.ISBN9781429208925.
- ↑4,04,14,24,34,4Muller, F. (2000), »The nature and mechanism of superoxide production by the electron transport chain: Its relevance to aging«,AGE,23(4): 227–253,doi:10.1007/s11357-000-0022-9
- ↑5,05,15,25,3Han D.; Williams E.; Cadenas E. (2001).»Mitochondrial respiratory chain-dependent generation of superoxide anion and its release into the intermembrane space«.Biochem. J.353(Pt. 2): 411–6.doi:10.1042/0264-6021:3530411.PMC1221585.PMID11139407.
- ↑Halliwell, Gutteridge; Free Radicals in Biology and Medicine, 2005.
- ↑7,07,1Tennant D.A.; Durán R.V.; Boulahbel H.; Gottlieb E. (2009). »Metabolic transformation in cancer«.Carcinogenesis.Zv. 30, št. 8. str. 1269–1280.doi:10.1093/carcin/bgp070.
Viri
uredi- Dröge, W. (2002).»Free radicals in the physiological control of cell function«.Physiological Reviews.82(1): 47–95.doi:10.1152/physrev.00018.2001.PMID11773609.
- Halliwell, B. & Gutteridge, J.M.C. (2005).Free Radicals in Biology and Medicine.Oxford: Oxford University Press.
Nadaljnjo branje
uredi- Sen, C.K. (2003). »The general case for redox control of wound repair«.Wound Repair Regen.11(6): 431–8.PMID14617282.
- Krötz, Florian; Sohn, Hae Young; Gloe, Torsten; Zahler, Stefan; Riexinger, Tobias; Schiele, Thomas M.; Becker, Bernhard F.; Theisen, Karl; Klauss, Volker; Pohl, Ulrich (1. avgust 2002). »NAD(P)H oxidase–dependent platelet superoxide anion release increases platelet recruitment«.Blood.100(3): 917–924.doi:10.1182/blood.v100.3.917.
- Pignatelli, Pasquale; Pulcinelli, Fabio M.; Lenti, Luisa; Paolo Gazzaniga, Pier; Violi, Francesco (15. januar 1998). »Hydrogen Peroxide Is Involved in Collagen-Induced Platelet Activation«.Blood.91(2): 484–490.doi:10.1182/blood.v91.2.484.