Blok f
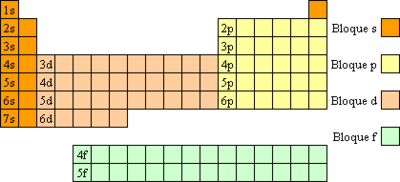
Blok fperiodnega sistemaelementovje sestavljen iz elementov, katerihatomiimajo v osnovnem stanjuelektronez najvišjo energijo naorbitali f.Elementi se imenujejo tudinotranji prehodni elementialiredke zemeljske kovine.
V nasprotju z drugimi bloki periodnega sistema so elementi v bloku f razvrščeni po periodi oziroma po naraščajočihvrstnih številihin ne po skupinah s podobnimielektronskimi konfiguracijami.Blok f je zato razdeljen v dve skupini:lantanoidiinaktinoidi.[1][2]
Elementi iz bloka f so, tako kot elementi izbloka s,zelo reaktivnekovine.Nazrakuse zelo lahko vnamejo, zvodopa tvorijo hidrokside invodik.Imajo večjegostoteter višjatališčainvreliščaodalkalijskih zemeljskih kovin.Zaradi velike reaktivnosti je njihova uporabnost omejena. Pridobivajo se zelektrolizotalin njihovih kloridov, ker elektrolizeraztopinzaradi velike reaktivnosti ne pridejo v poštev.
Večinaspojinelementov iz bloka f so ionske soli z M3+ioni, ki so v vodnih aztopinah pogosto hidratizirane.Cerijtvori tudi nekaj spojin, v katerih je voksidacijskem stanju4+, na primer CeO2,ki so močnioksidanti.Aktinoidi odprotaktinijadoamericijalahko s svojimi f elektroni sodelujejo v tvorbikemijskih veziin tvorijo spojine, v katerih imajo oksidacijska stanja od 2+ do 6+. Težji aktinoidi odkirijadolavrencijapritegnejo notranje f elektrone proti jedru, tako da ne morejo sodelovati pri tvorbi vezi. V spojinah zato nastopajo samo kot M3+ioni.
Reference[uredi|uredi kodo]
Glej tudi[uredi|uredi kodo]
- Periodni sistem elementov
- Blok periodnega sistema
- Elektronska konfiguracija
- Blok s
- Blok p
- Blok d
- Blok g
Zunanje povezave[uredi|uredi kodo]
- Slike f-orbitalArhivirano2012-03-21 naWayback Machine.
