Tiol
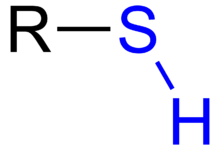
U organskoj hemiji,tioljeorganosumporno jedinjenjekoje sadrži za ugljenik vezanu sulfhidrilnu (–C–SH ili R–SH) grupu (gde R označavaalkan,alken,ili drugu koja sadrži atome ugljenika). –SH funkcionalna grupa se naziva bilotiolnomilisulfhidrilnomgrupom. Tioli su sumporni analozialkohola(tj. sumpor zauzima mesto kiseonika uhidroksilnojgrupi alkohola), a reč je mešavina „tio-” i „alkohola”, pri čemu prva reč potiče izgrčkogθεῖον –teion= sumpor.[1]
Mnogi tioli imaju jak miris koji podseća na beli luk ili trulajaja.Tioli se koriste kao odoranti koji pomažu u detekcijiprirodnog gasa,koji u čistom obliku nema mirisa, i „miris prirodnog plina” posledica je mirisa tiola koji se koristi kao odorans. Tioli se često nazivajumerkaptanima.[2][3]Taj termin je izveden izlat.mercurium captans(hvatanje žive),[4]jer tiolna grupa formira jake veze sa jedinjenjimažive,uveo jeVilijam Kristofer Zeise1832.[5][6]
Struktura i vezivanje
[уреди|уреди извор]Tioli strukture R–SH nazivaju se alkanetioli ili alkil-tioli, u kojima jealkilgrupa (R) vezana zasulfhidrilgrupu (SH).[7]Tioli i alkoholi imaju sličnu molekulsku strukturu. Glavna razlika je veličinahalkogenida.Dužina C–S veze je oko 180pikometara,a C–S–H ugao je oko 90°.Vodonično vezivanjeizmeđu individualnih tiolnih grupa je slabo, i glavna kohezivna sila suvan der Valsove interakcijeizmeđu visoko polarizablnih divalentnih sumpornih centara. S−H veza je mnogo slabija od O–H veze, što se odražava u njihovojenergiji disocijacije veze(BDE). Za CH3S–H BDE iznosi 366 kJ/mol, dok je za CH3O–H BDE 440 kJ/mol.[8]
Usled male razlike uelektronegativnostiizmeđu sumpora i vodonika, S–H veza je manjepolarnanegohidroksilnagrupa. Tioli imaju manjedipolne momenteod korespondirajućih alkohola.
Nomenklatura
[уреди|уреди извор]Postoji nekoliko načina za imenovanje alkiltiola:
- Sufiks–tioldodat je imenu alkana. Ovaj način je gotovo identičanimenovanju alkoholai koristi jeIUPAC,npr. CH3SH bi biometanetiol.
- Terminmerkaptanzamjenjujealkoholu imenu ekvivalentnog alkoholnog jedinjenja. Primer: CH3SH bi bio metil-merkaptan, baš kao što se CH3OH nazivametilnimalkoholom.
- Terminsulfhidril–ilimerkapto–koristi se kaoprefiks,npr.merkaptopurin.
Fizičke osobine
[уреди|уреди извор]Miris
[уреди|уреди извор]Mnogi tioli imaju jakemirisenalik mirisubelog luka.Mirisi tiola, posebno onih niske molekulske težine, često su jaki i odbojni. Sprej odtvorasastoji se uglavnom od niskomolekularnih tiola i derivata.[9][10][11][12][13]Ova jedinjenja detektuje ljudski nos u koncentraciji od samo 10 delova na milijardu.[14]Ljudskiznojsadrži (R)/(S)-3-metil-3-merkapto-1-ol (MSH), koji se detektuje u 2 dela na milijardu i ima voćni miris sličanluku.(Metiltio) metantiol (MeSCH2SH; MTMT) je isparljivi tiol sa jakim mirisom, koji se takođe detektuje u delovima na milijardu, a koji je prisutan u urinu muškihmiševa.Lovrens C. Kaci njegovi saradnici su pokazali da MTMT funkcioniše kaosemiohemikalija,aktivirajući određene olfaktorne senzorne neurone miša, privlačeći ženske miševa.[15]Pokazalo se da je bakar neophodan za specifični mirisni receptor miša, MOR244-3, koji je visoko responsivan na MTMT, kao i na razne druge tiole i srodna jedinjenja.[16]Identifikovan je ljudski mirisni receptorOR2T11koji je u prisustvu bakra veoma responsivan na gasne zadahe (vidi ispod)etantiolit-butil merkaptankao i na druge tiole male molekulske težine, uključujućialil merkaptankoji se nalazi u ljudskom zadahu odbelog lukai ciklični sulfidtietansa jakim mirisom.[17]
Tioli su takođe odgovorni za klasuvinskih zadahaizazvanih nenamernom reakcijom sumpora ikvasca,kao i „neugodnim “mirisom piva koje je bilo izloženo ultraljubičastoj svetlosti.
Nisu svi tioli neprijatnih mirisa. Na primer,furan-2-ilmetanetioldoprinosi aromi prženekafe,dok jegrejpfrut merkaptan,monoterpenoidnitiol, odgovoran za karakterističan mirisgrejpfruta.Efekat potonjeg jedinjenja prisutan je samo u niskim koncentracijama. Čisti merkaptan ima neprijatan zadah.
Od distributeraprirodnog gasase očekuje da dodaju tiole, prvobitnoetantiol,prirodnom gasu (koji prirodno nema mirisa). Taj zahtev je postao mandatoran nakon smrtonosneeksplozije škole Nju LondonuNovom Londonuu Teksasu 1937. godine. Mnogi distributeri gasa su odorizirali gas i pre ovog događaja. Većina upotrebljenih odornih gasova trenutno sadrži smeše merkaptana i sulfida, sat-butil merkaptanomkao glavnim sastojkom mirisa u prirodnom gasu ietantiolomu utečnjom naftnom gasu (TNG, propan).[18]U situacijama u kojima se tioli koriste u komercijalnoj industriji, kao što su cisterne sa tečnim naftnim gasom i sistemi za rukovanje velikih količina, oksidacioni katalizator se koristi za neutralisanje mirisa. Katalizator na bazi oksidacije bakra neutrališe isparljive tiole i pretvara ih u inertne proizvode.
Tačke ključanja i rastvorljivost
[уреди|уреди извор]Tioli pokazuju mali stepen povezanostivodoničnim vezivanjem,kako sa molekulima vode, tako i među sobom. Stoga imaju nižetačke ključanjai manje surastvorljiviu vodi i drugimpolarnim rastvaračimaod alkohola slične molekulske težine. Iz tog razloga, tioli i njihove korespondirajućeizomerisulfidne funkcionalne grupe imaju slične karakteristike rastvorljivosti i tačke ključanja, dok to ne važi za alkohole i njihove odgovarajuće izomerne etre.
Vezivanje
[уреди|уреди извор]Veza S-H u tiolima je slaba u poređenju sa O-H vezom u alkoholima. Za CH3X−H, entalpije veza su365,07±2,1 kcal/molza X = S i440,2±3,0 kcal/molza X = O.[19]Abstrakcija atoma vodonika iz tiola dajetiilni radikalformule RS•,gde je R = alkil ili aril.
Reakcije
[уреди|уреди извор]- Stvaranjesoli
Kao što jevodonik-sulfidkiseliji od vode, merkaptani su kiseliji odalkoholai reagiraju s jakim bazama rastvorenim u vodi, dajući soli. Kao inatrijum sulfid,ove soli u vodenom rastvoru znatno se hidroliziraju.
- RSH + NaOHRSNa + H2O
Soli teških metala, kao soli olova, žive,bakra,kadmijumaisrebra,nerastvorne su u vodi.
- Oksidacija u disulfide

Rastvori natrijum hipohalogenida oksiduju na sobnoj temperaturi merkaptane dosulfida.
- 2 RSH + I2+ 2 NaOH → RSSR + 2 NaI + 2 H2O
Ako se upotrebi standardni rastvorjoda,ova reakcija povoljna je za kvantitativno određivanje merkaptana. Lako se oksiduju navazduhu,posebno u prisustvuamonijaka.
Doktorov procesza uklanjanje neugodnog mirisabenzinazavisi od reakcije merkaptana u disulfide, koji imaju slabiji miris, pomoću rastvora natrijum plumbita i male količinesumpora.
- 2 RSH + Na2PbO2→ Pb(SR)2+ 2 NaOH
- Pb(SR)2+ S → PbS + (RS)2
Doktorov rastvor se regeneriše provođenjem vazduha kroz vrući rastvor.
- PbS + 4 NaOH + 2 O2→ Na2PbO2+ Na2SO4+ 2 H2O
Doktorov rastvorse može takođe upotrebiti kao dokaz sulfhidrilne grupe. Stvaranje crnog olovnogsulfidaznak je pozitivne reakcije. Oksidacije sulfhidrilne grupe izcisteinskogdela proteinskih molekula u disulfidne grupe i redukcija disulfida u sulfhidril ima značajnu ulogu u biološkim procesima.
- Oksidacija u sulfonske kiseline
Ova reakcija obično se odvija greanjem merkaptana ilisoli,kao što je olovni merkaptid, s koncentrovanomazotnom kiselinom.
- RSH + 3 [O] (HNO3) → RSO3H
- (RS)2Pb + 6 [O] (HNO3) → (RSO3)2Pb
- Stvaranje estera

Kad primarni tioli reaguju skarboksilnim kiselinama,nastajutioestriivoda,pre negoestriiivodonik-sulfid.
- RCOOH + HSRRCOSR + H2O
Ova reakcija bila je osnov za pretpostavku da se, pri esterifikaciji primarnih alkohola s kiselinama,hidroksilna grupaotcepljuje pre s kiseline nego s alkohola, što je dokazano pomoćuizotopaO18.
Merkatani reaguju takođe s halogenidima kiselina, dajući tioestere.
- RSH + ClCOR → RSCOR + HCl
Za razliku od hidroksilne grupe, merkapto grupa se ne zamenjuje lako. Fosforni triklorid npr. reaguje formirajući tioester.
- RSH + PCl3→ RSPCl2+ HCl
- Nastajanje tioacetala
Tioli lako reaguju saldehidimaiketonimauzhlorovodonikilicink jodid,formirajući tioacetale.
- RCHO + 2 R`SH → RCH(SR`)2+ H2O
- R2CO + 2 R`SH → R2C(SR`)2+ H2O
Ova jedinjenja su mnogo stabilnija nahidrolizukiselinom od acetala, ali se aldehid ili keton mogu regenerirati hidrolizom uz živin(II) oksid.
Primeri tiola
[уреди|уреди извор]- Metantiol– CH3SH [metil merkaptan]
- Etantiol– C2H5SH [etil merkaptan]
- 1-Propanetiol– C3H7SH [n- propil merkaptan]
- 2-propantiol– CH3CH(SH)CH3[2C3 merkaptan]
- Alil merkaptan– CH2=CHCH2SH [2-propentiol]
- Butantiol- C4H9SH [n- butil merkaptan]
- Terc- butil merkaptan– (CH3)3CSH [t- butil merkaptan]
- Pentantiol– C5H11SH [pentil merkaptan]
- Tiofenol– C6H5SH
- Dimerkaptosukcinska kiselina
- Tiosirćetna kiselina
- Koenzim A
- Glutation
- Metalotionein
- Cistein
- 2-Merkaptoetanol
- Ditiotreitol/dithioerythritol(parepimera)
- 2-Merkaptoindol
- Grapefruit merkaptan
- Furan-2-ilmetantiol
- 3-Merkaptopropan-1,2-diol
- 3-Merkapto-1-propansulfonska kiselina
- 1-heksadekantiol
- Pentahlorobenzentiol
Vidi još
[уреди|уреди извор]Reference
[уреди|уреди извор]- ^θεῖονАрхивирано2017-05-10 на сајтуWayback Machine,Henry George Liddell, Robert Scott,A Greek–English Lexicon
- ^Patai, Saul, ур. (1974).The chemistry of the thiol group.London: Wiley.ISBN978-0-471-66949-4.
- ^R. J. Cremlyn (1996).An Introduction to Organosulfur Chemistry.Chichester: John Wiley and Sons.ISBN978-0-471-95512-2.
- ^Dictionary:mercaptanАрхивирано2012-11-13 на сајтуWayback Machine
- ^Oxford American Dictionaries(Mac OS X Leopard).
- ^See:
- Zeise, William Christopher (1834).„Mercaptanet, med bemaerkninger over nogle andre nye producter af svovelvinsyresaltene, som og af den tunge vinolie, ved sulfureter”[Mercaptan, with remarks on some other new products of salts of ethyl hydrogen sulfate as well as of heavy oil of wine, by means of hydrogen sulfide].Kongelige Danske Videnskabers Selskabs Skrifter.4th series (на језику: дански).6:1—70.On p. 13 the word "mercaptan" is coined.
- German translation:Zeise, W. C. (1834).„Das Mercaptan, nebst Bermerkungen über einige neue Producte aus der Einwirkung der Sulfurete auf weinschwefelsaure Salze und auf das Weinöl”[Mercaptan together with comments on some new products from the effect of hydrogen sulfide on salts of ethyl sulfate ((C2H5)HSO4) and heavy oil of wine (a mixture of diethyl sulfate, diethyl sulfite, and polymerized ethylene)].Annalen der Physik und Chemie.2nd series (на језику: немачки).31(24): 369—431.From p. 378:"…nenne ich den vom Quecksilber aufgenommenen StoffMercaptum(von:Corpus mercurio captum)… "(… I name the substance [that is] absorbed by mercury "mercaptum" (from: the body (substance) [that] has been absorbed by mercury)… )
- German translation is reprinted in:Zeise, W. C. (1834).„Das Mercaptan, nebst Bemerkungen über einige andere neue Erzeugnisse der Wirkung schwefelweinsaurer Salze, wie auch des schweren Weinöls auf Sulphurete”.Journal für Praktische Chemie.1(1): 257—268, 345—356, 396—413, 457—475.doi:10.1002/prac.18340010154.
- Summarized in:Zeise, W. C. (1834).„Ueber das Mercaptan”[On mercaptan].Annalen der Pharmacie.11(1): 1—10.doi:10.1002/jlac.18340110102.Архивираноиз оригинала 2015-03-20. г.
- Zeise, William Christopher (1834).„Sur le mercaptan; avec des observations sur d'autres produits resultant de l'action des sulfovinates ainsi que de l'huile de vin, sur des sulfures metalliques”[On mercaptan; with observations on other products resulting from the action of sulfovinates [typically, ethyl hydrogen sulfate] as well as oil of wine [a mixture of diethylsulfate and ethylene polymers] on metal sulfides].Annales de Chimie et de Physique.56:87—97.Архивираноиз оригинала 2015-03-20. г."Mercaptan" (ethyl thiol) was discovered in 1834 by the Danish professor of chemistryWilliam Christopher Zeise(1789–1847). He called it "mercaptan", a contraction of "corpus mercurio captans" (mercury-capturing substance) [p. 88], because it reacted violently with mercury(II) oxide ( "deutoxide de mercure" ) [p. 92].
- The article inAnnales de Chimie et de Physique(1834) was translated from the German article:Zeise, W. C. (1834).„Das Mercaptan, nebst Bemerkungen über einige neue Producte aus der Einwirkung der Sulfurete auf weinschwefelsaure Salze und auf das Weinöl”.Annalen der Physik und Chemie.107(27): 369—431.Bibcode:1834AnP...107..369Z.doi:10.1002/andp.18341072402.Архивираноиз оригинала 2015-03-20. г.
- ^„Alkanethiols”.Royal Society of Chemistry.Приступљено4. 9. 2019.
- ^Lide David R., ур. (2006).CRC Handbook of Chemistry and Physics(87th изд.). Boca Raton, FL: CRC Press.ISBN978-0-8493-0487-3.
- ^Andersen K. K.; Bernstein D. T. (1978).„Some Chemical Constituents of the Scent of the Striped Skunk (Mephitis mephitis)”.Journal of Chemical Ecology.1(4): 493—499.S2CID9451251.doi:10.1007/BF00988589.
- ^Andersen K. K., Bernstein D. T.; Bernstein (1978).„1-Butanethiol and the Striped Skunk”.Journal of Chemical Education.55(3): 159—160.Bibcode:1978JChEd..55..159A.doi:10.1021/ed055p159.
- ^Andersen K. K.; Bernstein D. T.; Caret R. L.; Romanczyk L. J., Jr. (1982). „Chemical Constituents of the Defensive Secretion of the Striped Skunk (Mephitis mephitis)”.Tetrahedron.38(13): 1965—1970.doi:10.1016/0040-4020(82)80046-X.
- ^Wood W. F.; Sollers B. G.; Dragoo G. A.; Dragoo J. W. (2002). „Volatile Components in Defensive Spray of the Hooded Skunk,Mephitis macroura”.Journal of Chemical Ecology.28(9): 1865—70.PMID12449512.S2CID19217201.doi:10.1023/A:1020573404341.
- ^William F. Wood.„Chemistry of Skunk Spray”.Dept. of Chemistry,Humboldt State University.Архивираноиз оригинала 8. 10. 2010. г.Приступљено2. 1. 2008.
- ^Aldrich, T.B. (1896).„A Chemical Study of the Secretion of the Anal Glands ofMephitis mephitiga(Common Skunk), with Remarks on the Physiological Properties of This Secretion”.J. Exp. Med.1(2): 323—340.PMC2117909
 .PMID19866801.doi:10.1084/jem.1.2.323.
.PMID19866801.doi:10.1084/jem.1.2.323.
- ^Lin, Dayu; Zhang, Shaozhong; Block, Eric; Katz, Lawrence C. (2005). „Encoding social signals in the mouse main olfactory bulb”.Nature.434(7032): 470—477.Bibcode:2005Natur.434..470L.PMID15724148.S2CID162036.doi:10.1038/nature03414.
- ^Duan, Xufang; Block, Eric; Li, Zhen; Connelly, Timothy; Zhang, Jian; Huang, Zhimin; Su, Xubo; Pan, Yi; et al. (2012).„Crucial role of copper in detection of metal-coordinating odorants”.Proc. Natl. Acad. Sci. U.S.A.109(9): 3492—3497.Bibcode:2012PNAS..109.3492D.PMC3295281
 .PMID22328155.doi:10.1073/pnas.1111297109.
.PMID22328155.doi:10.1073/pnas.1111297109.
- ^„Copper key to our sensitivity to rotten eggs' foul smell”.chemistryworld.Архивираноиз оригинала 10. 5. 2017. г.Приступљено3. 5. 2018.
- ^Roberts, J. S., ур. (1997).Kirk-Othmer Encyclopedia of Chemical Technology.Weinheim: Wiley-VCH.
- ^Luo, Y.R.; Cheng, J.P. (2017). „Bond Dissociation Energies”. Ур.: J. R. Rumble.Handbook of Chemistry and Physics.CRC Press.
Spoljašnje veze
[уреди|уреди извор]- Primena, osobine, i sinteza tiola
- Merkaptan
- Šta je merkaptan?Архивиранона сајтуWayback Machine(20. децембар 2008)
- Mercaptans (or Thiols)atThe Periodic Table of Videos(University of Nottingham)
- What Is the Worst Smelling Chemical?Архивиранона сајтуWayback Machine(6. јун 2011), by About Chemistry.

