Diboran
| Den här artikelnbehöverkällhänvisningarför att kunnaverifieras.(2023-01) Åtgärda genom att lägga till pålitliga källor (gärna som fotnoter). Uppgifter utan källhänvisning kanifrågasättasoch tas bort utan att det behöver diskuteras pådiskussionssidan. |
| Diboran | |
  | |
| Systematiskt namn | Diborhexahydrid |
|---|---|
| Kemisk formel | B2H6 |
| Molmassa | 27,67 g/mol |
| Utseende | Färglös gas |
| CAS-nummer | 19287-45-7 |
| SMILES | [H][B]1([H])[H][B]([H])([H])[H]1 |
| Egenskaper | |
| Densitet | 1,2 g/cm³ |
| Löslighet(vatten) | Hydrolys |
| Smältpunkt | -165,5 °C |
| Kokpunkt | -92,4 °C |
| Faror | |
| Huvudfara | |
| NFPA 704 | |
| SI-enheter&STPanvänds om ej annat angivits | |
Diboranär en kemisk förening bestående avborochväte.Vid rumstemperatur är den en färglös gas med kväljande sötaktig lukt. Diboran blandar sig lätt med luft och bildar en explosiv blandning. I fuktig luft kan blandningen spontandetonera.
Molekylstruktur
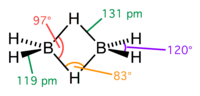
[redigera|redigera wikitext]Diboranmolekylen består av två boratomer med vardera två väteatomer med normalakovalent bindningarsamt två väteatomer mellan boratomerna. De sistnämnda två väteatomerna och boratomerna har envalenselektronvar, tillsammans fyra elektroner, som skapar en cirkulär bindning liknande den som finns iaromatiska kolväten.
Framställning
[redigera|redigera wikitext]Industriell framställning sker genom reduktion avbortrifluoridellerbortrikloridmed en annanmetallhydrid:
För småskalig framställning för laboratoriebruk så är oxidation av borhydridsalt en lämpligare metod:
Användning
[redigera|redigera wikitext]Diboran används som raketbränsle,vulkaniseringsmedelför gummi samt som katalysator förpolymerisationavkolväten.Det är också ett mellansteg vid tillverkning av kemiskt ren bor för dopning av halvledare.




