Ädelgas
| Grupp | 18 | ||||||||
|---|---|---|---|---|---|---|---|---|---|
| Period | |||||||||
| 1 | 2 He | ||||||||
| 2 | 10 Ne | ||||||||
| 3 | 18 Ar | ||||||||
| 4 | 36 Kr | ||||||||
| 5 | 54 Xe | ||||||||
| 6 | 86 Rn | ||||||||
| 7 | 118 Og | ||||||||
Teckenförklaring
| |||||||||
Ädelgaserärgrundämnenaigrupp 18i detperiodiska systemet.Dessa grundämnen kännetecknas dels av att de äricke-metallersom ogärna reagerar ikemiska reaktioner,men även för att de alla är igasformvidstandardtryck och -temperatur.De fem ädelgaser som har stabilaisotoperärhelium (He),neon (Ne),argon (Ar),krypton (Kr)ochxenon (Xe).Ädelgasenradon (Rn)är radioaktiv och på grund av detta har den studerats mindre än de första fem medlemmarna i gruppen. Ensyntetiskmedlem av gruppen,oganesson (Og),har också upptäckts, men mycket lite är känt om dess egenskaper på grund av dess kortahalveringstid.
Kemiskt sett är ädelgaserna stabila, detta på grund av att de har maximalt antalvalenselektroneri sitt ytterstaelektronskal,vilket i sin tur leder till att de extremt sällan reagerar med andra ämnen. Under standardtryck och -temperatur är de luktlösa, färglösa, enatomiska gaser. Ädelgasernas smält- och kokpunkter ligger mycket nära varandra, alla inom ett intervall på 10 °C där de är flytande. Då ädelgaserna påvisar extremt låg kemisk reaktivitet, finns därför endast ett par hundra kända ädelgasföreningar, betydligt färre än för andra grundämnen.
Neon, argon, krypton och xenon utvinns från luften genomgaskondenseringochfraktionerad destillation.Helium framställs oftast från oljekällor, och radon isoleras vanligtvis från radioaktiv sönderdelning av lösta radiumföreningar.
Ädelgaser har många industriellt viktiga funktioner sombelysning,svetsningochrymdutforskning.Helium används ofta inom dykning, där det ersätter en del av luftblandningen. Helium har även fått ersättavätgasiluftskeppochballonger,då det blev uppenbart att vätgas utgör en stor brandrisk.

Historia
[redigera|redigera wikitext]Ordet "ädelgas" kommer från det tyska substantivetEdelgas,som användes för första gången 1898 avHugo Erdmann[1]."Ädel" syftar till den extremt låga reaktiviteten hos grundämnena i grupp 18 i detperiodiska systemetpåvisade understandardtryck och -temperatur,på samma vis somädelmetallerockså reagerar mycket lite med sin omgivning.
Ädelgaserna har även kallats för "inerta gaser",men detta är en felaktig benämning då alla naturliga ädelgaser kan delta i kemiska reaktioner under rätt förhållanden.[2]"Ovanliga gaser" är en annan term som använts,[3]men även denna är felaktig då argon utgör en betydande del (0,94% efter volym, 1,3% efter massa) avjordens atmosfär[4]
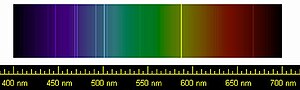
Pierre JanssenochJoseph Norman Lockyervar18 augusti1868de första att upptäcka en ädelgas då de studeradesolenskromosfär.De gav gasen namnetheliumefter detgrekiskaordet för solen,Helios(ἥλιος)[5]Redan 1784 hade emellertid den engelska kemisten och fysikernHenry Cavendishupptäckt att luft innehöll en liten mängd av ett ämne som var mindre reaktivt änkväve.[6]Ett århundrade senare, 1895, upptäckteLord Rayleighatt kväveprover från luften hade en annandensitetän det kväve som framställts genomkemiska reaktioner.Tillsammans med forskarenWilliam Ramsayla Lord Rayleigh fram en teori om att det kväve som togs fram ur luften var blandat med ytterligare en gas, vilket bekräftades med ett experiment i vilket ett nytt grundämne,argon,lyckades isoleras. Namnet fick argon från det grekiska ordet för "inaktiv" (αργό(ν)).[6]Med denna upptäckt insåg man att en hel klass med gaser saknades i det periodiska systemet. Under sökandet efter argon hade Ramsay även lyckats isolera helium för första gången då han hettade uppmineralencleveit.1902 inkluderadeDmitrij Mendelejevgrundämnena helium och argon i grupp 0 i sin schematiska uppdelning av grundämnena, vilket senare blev det periodiska systemet.[7]
Ramsay fortsatte att leta efter dessa gaser med hjälp avfraktionerad destillation,för att på så vis separera de olika komponenterna iflytande luft.1898 upptäckte han grundämnenakrypton,neonochxenon,och han namngav dessa efter de grekiska ordenκρυπτός(kryptos,dold),νέος(neos,ny) ochξένος(xenos,främling).Radonupptäcktes 1898 avFriedrich Ernst Dorn[8]och fick namnet "radiumemanation ", men den ansågs inte vara en ädelgas förrän 1904, då man upptäckte att grundämnet liknade de andra ädelgaserna.[9]Rayleigh och Ramsay fick 1904Nobelprisetifysikrespektive i kemi, för sina upptäckter av ädelgaserna.[10][11]J. E. Cederblom, dåvarande ordförande iKungliga Vetenskapsakademien,gav motiveringen; "upptäckten av en helt ny grupp av grundämnen, av vilken ingen medlem tidigare varit känd, är något verkligt unikt i kemins historia och ett framsteg av hög betydelse inom vetenskapen".[11]
Upptäckten av ädelgaserna hjälpte till att utveckla en grundläggande förståelse avatomstrukturen.1895 försökte den franske kemistenHenri Moissanfå till en reaktion mellanfluor,det mestelektronegativagrundämnet, och argon, en av ädelgaserna. Han misslyckades emellertid med detta och inte förrän i slutet av 1900-talet lyckades man bilda en kemisk förening innehållande argon, dessa försök hjälp dock till att utveckla nya teorier för atomstrukturen. Med utgångspunkt i dessa experiment föreslog den danska fysikernNiels Bohr1913 att atomernas elektroner var ordnade iskalsom omgärdadeatomkärnanoch att alla ädelgaser förutom helium hade ett yttersta skal innehållande åtta elektroner.[9]1916 skapadeGilbert N. Lewisden så kalladeoktettregeln,som slöt sig till att en oktett av elektroner var det mest stabila arrangemanget för en atom; detta gjorde att atomen ogärna reagerade med andra grundämnen då den inte behövde några fler elektroner för att fylla sitt yttre skal.[12]
Inte förrän 1962 upptäckteNeil Bartlettden första kemiska föreningen med en ädelgas,xenonhexafluorplatinat.[13]Föreningar med andra ädelgaser upptäcktes kort därpå; 1962 för radon,radonfluorid,[14]och 1963 för krypton,kryptondifluorid(KrF2).[15]Den första stabila föreningen med argon upptäcktes inte förrän 2000 dåargonfluorhydrid(HArF) bildades vid temperaturen 40 K (−233 °C).[16]
I december 1998 bombarderade en grupp forskare vidJoint Institute for Nuclear ResearchiDubna,Rysslandplutonium (Pu)medkalcium (Ca)för att skapa en atom av grundämne 114,[17]som senare fick namnetflerovium (Fl).[18]Tidiga kemiska experiment har påvisat att grundämnet kan vara den förstatransuranenatt ha egenskaper liknande de hos ädelgaserna, detta trots att det tillhörgrupp 14i det periodiska systemet.[19]I oktober 2006 lyckades forskare vid Joint Institute for Nuclear Research ochLawrence Livermore National Laboratoryatt framställa den första atomen avoganesson (Og),det sjunde grundämnet i grupp 18,[20]genom att bombarderacalifornium (Cf)medkalcium (Ca).[21]
Kemiska egenskaper
[redigera|redigera wikitext]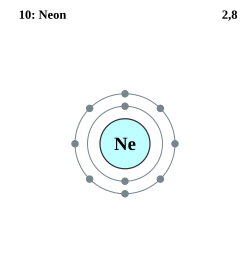
Ädelgaser utgör tillsammans grupp 18 i detperiodiska systemet.De grundämnen som bekräftats höra till den här gruppen ärhelium (He),neon (Ne),argon (Ar),krypton (Kr),xenon (Xe)ochradon (Rn).[22]Dessa grundämnen är färg-, lukt- och smaklösa, och svårantändliga under normala förhållanden. Gruppen kallades tidigare förgrupp 0då man trodde att dessa ämnen saknade valenselektroner, vilket skulle innebära attatomernainte kunde bildakemiska föreningar.Senare upptäckte man emellertid att även ädelgaserna kunde bilda föreningar och benämningen slutade användas.[9]Väldigt lite är idag känt om ädelgasernas senaste medlem,oganesson (Og).[23]
Ädelgaserna har fulla yttreelektronskal(valensskal).Valenselektronerär de ytterstaelektronernai en atom och är normalt sett de enda som är delaktiga ikemiska bindningar.Atomer med fulla valensskal är extremt stabila och bildar därför väldigt sällan kemiska föreningar och de har även väldigt svårt att ta till sig eller förlora elektroner.[24]På grund av den svagareelektromagnetiska kraftenhos tyngre ädelgaser kan elektroner avlägsnas lättare från t.ex. en radon-atom än från en lättare helium-atom.
Tack vare att ädelgaserna har ett fullt yttre skal kan de användas tillsammans med teckensystemet förelektronkonfigurationför att bilda ett "ädelgassystem". För att göra detta skrivs den närmsta ädelgasen som kommer före grundämnet i fråga först och sedan elektronkonfigurationen därifrån. Exempelvis är det klassiska elektronkonfigurationssystemet förkol1s²2s²2p² och ädelgassystemet [He]2s²2p². Detta teckensystem gör det enklare att identifiera grundämnen samtidigt som det är kortare att skriva än det fullständiga atomorbitalerna.[25]
På grund av det fulla valensskalet iargonanvänds gasen i glödlampor för att förhindra syretillförsel och för att strömmen i lampan inte ska bilda gnistor.
Referenser
[redigera|redigera wikitext]- Den här artikeln är helt eller delvis baserad på material frånengelskspråkiga Wikipedia.
Noter
[redigera|redigera wikitext]- ^Edward Renouf (15 februari 1901).” Noble gases”.Science13: sid. 268–270.
- ^Ozima 2002,s. 30.
- ^Ozima 2002,s. 4.
- ^"Argon".Encyclopædia Britannica.(2008).
- ^Oxford English Dictionary(1989), s.v. "helium". Hämtdatum16 december2006,från Oxford English Dictionary Online. Se även citat: Thomson, W. (1872).Rep. Brit. Assoc.xcix: "Frankland and Lockyer find the yellow prominences to give a very decided bright line not far from D, but hitherto not identified with any terrestrial flame. It seems to indicate a new substance, which they propose to call Helium."
- ^ [ab]Ozima 2002,s. 1.
- ^Mendeleev 1903,s. 497.
- ^J. R. Partington (May 1957).” Discovery of Radon”.Nature179 (4566): sid. 912.doi:.
- ^ [abc]"Noble Gas".Encyclopædia Britannica.(2008).
- ^J.E. Cederblom (1904).”The Nobel Prize in Physics 1904 Presentation Speech”.https://www.nobelprize.org/prizes/physics/1904/ceremony-speech/.
- ^ [ab]Fri översättning frånJ.E. Cederblom (1904).”The Nobel Prize in Chemistry 1904 Presentation Speech”.https://www.nobelprize.org/prizes/chemistry/1904/ceremony-speech/.
- ^Gillespie RJ, Robinson EA (2007).” Gilbert N. Lewis and the chemical bond: the electron pair and the octet rule from 1916 to the present day”.J Comput Chem28 (1): sid. 87–97.doi:.PMID 17109437.
- ^N. Bartlett (1962).” Xenon hexafluoroplatinate Xe+[PtF|6|]–”.Proceedings of the Chemical Society(6): sid. 218.doi:.
- ^”Radon Fluoride”.Journal of the American Chemical Society84 (21): sid. 4164–4165. 1962.doi:.
- ^Grosse, A. V.; Kirschenbaum, A. D.; Streng, A. G.; Streng, L. V. (1963).” Krypton Tetrafluoride: Preparation and Some Properties”.Science139: sid. 1047–1048.doi:.PMID 17812982.
- ^Khriachtchev, Leonid; Pettersson, Mika; Runeberg, Nino; Lundell, Jan; Räsänen, Markku (24 augusti 2000).” A stable argon compound”.Nature406 (406): sid. 874–876.doi:.
- ^Oganessian, Yu. Ts. (1999).” Synthesis of Superheavy Nuclei in the48Ca +244Pu Reaction”.Physical Review Letters(American Physical Society) 83: sid. 3154.doi:.
- ^Woods, Michael (6 maj 2003).”Chemical element No. 110 finally gets a name—darmstadtium”.Pittsburgh Post-Gazette.http://www.post-gazette.com/healthscience/20030506element0506p4.asp.Läst 26 juni 2008.
- ^”Gas Phase Chemistry of Superheavy Elements”.Texas A&M University.Arkiverad frånoriginaletden 28 maj 2008.https://web.archive.org/web/20080528125641/http://lch.web.psi.ch/pdf/TexasA%26M/TexasA%26M.pdf.Läst 31 maj 2008.
- ^Wilson, Elaine (2005).” Making Meaning in Chemistry Lessons”.Electronic Journal of Literacy through Science4 (2).
- ^Oganessian, Yu. Ts. (9 oktober 2006).” Synthesis of the isotopes of elements 118 and 116 in the249Cf and245Cm +48Ca fusion reactions”.Physical ReviewC74 (4): sid. 44602.doi:.
- ^Ozima 2002,s. 2.
- ^”Oganesson”.WebElements Periodic Table.https://www.webelements.com/oganesson/.Läst 19 december 2018.
- ^Ozima 2002,s. 35.
- ^CliffsNotes 2007,s. 15.
Källor
[redigera|redigera wikitext]- Bennett (1998).The Physiology and Medicine of Diving.SPCK Publishing.ISBN 0702024104
- CliffsAP Chemistry.CliffsNotes. 2007-12-05.ISBN 047013500X
- Greenwood (1997).Chemistry of the Elements.Oxford:Butterworth-Heinemann.ISBN 0-7506-3365-4
- Harding (2002).Elements of the P Block.Royal Society of Chemistry.ISBN 0854046909
- Holloway (1968).Noble-Gas Chemistry.Methuen Publishing.ISBN 0412211009
- Mendeleev (1902–1903).Osnovy Khimii (The Principles of Chemistry).http://www.archive.org/details/principlesofchem00menduoft
- Ozima (2002).Noble Gas Geochemistry.Cambridge University Press.ISBN 0521803667.http://books.google.com/books?id=CBM2LJDvRtgC
- Weinhold (2005).Valency and bonding.Cambridge University Press.ISBN 0521831288
