Tryptofan
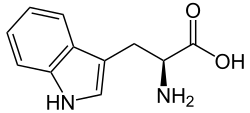

Tryptofan(förkortasTrpellerW) är inombiokemien av de 20aminosyrorsom är byggstenar iproteiner.Den tillhör gruppen opolära, hydrofoba aminosyror och är en av deessentiella aminosyrorna,[1]som kroppen inte själv kan tillverka, och som därför måste tillföras i födan. Bara L-stereoisomeren av tryptofan används som strukturellt enzymprotein; D-stereoisomeren är vanligast förekommande i naturligt produceradepeptider.Det utmärkande strukturella kännetecknet för tryptofan är att den har enindol-grupp.Den är en av de två aminosyror som motsvaras av endast ettkodon(UGG) i dengenetiska koden.
Tryptofan är också ett utgångsämne (substrat) vid kroppens tillverkning avserotonin[2]ochmelatoninsom har betydelse försömn,avslappning och stämningsläge och även blodkärlssammandragande. Tryptofan kan även användas för bildning avniacin.[3]I mat finns tryptofan i proteinrik föda, främst i kött och hårdost men även imjölkoch spannmål (sehavregryn). Vissa nötter och frön har en hög halt av tryptofan; särskilt kan nämnas pumpafrökärnor och chiafrön.Kynureninbildas i omsättningen av tryptofan.
Hos växter, svampar och bakterier är tryptofan substrat för biosyntesen avindolättiksyra.
Innehåll i olika livsmedel
[redigera|redigera wikitext]| Livsmedel | Protein [g/100 g livsmedel] |
Tryptofan [g/100 g livsmedel] |
Tryptofan/Protein [%] |
|---|---|---|---|
| kalkon |
|
|
|
| ostavcheddartyp |
|
|
|
| kyckling |
|
|
|
| nötkött |
|
|
|
| kotlettavlamm |
|
|
|
| kotlettavfläsk |
|
|
|
| lax |
|
|
|
| kolja |
|
|
|
| mjölk |
|
|
|
| sojabönor(råa) |
|
|
|
| ägg |
|
|
|
| vetemjöl |
|
|
|
| potatis |
|
|
|
| vittris |
|
|
|
KällaUSA:s jordbruksdepartementslivsmedelsdatabas
Fluorescensmätningar med hjälp av tryptofan
[redigera|redigera wikitext]Tryptofan ärluminiscentoch kan därför vara till hjälp vid koncentrationsbestämningar av proteinlösningar. De flestafluorescensemissionernaav ett veckat protein sker på grund av excitationen av tryptofan. En del emissioner sker på grund av de aromatiska aminosyrornatyrosinochfenylalanin.Man får dock se upp fördisulfidbryggor(cysteinkan bilda dessa) som också har ansenligabsorbansvid dessavåglängder.Tryptofan exciteras av fotoner med våglängderna 280–300 nm (nära UV) och erhåller en emissionstopp som ärsolvatokromatisk(möjligheten för en kemisk substans att ändra färg efter förändring i av lösningsmedlet, i detta fall polaritet hos lösningen) mellan 300 och 350 nm, beroende på lösningens polaritet. Ifall tryptofanerna är exponerade mot något polärt (till exempel ett lösningsmedel såsom vatten, etanol etcetera) kommer toppen på fluorescensen från tryptofan att närma sig våglängden 350 nm. Då tryptofan är ihydrofob(opolär) miljö (till exempel proteinets inre delar, ett denatureringsmedel etcetera) kommer toppen på fluorescensen att närma sig 300 nm (blåskift).
Det är därför man kan använda tryptofanfluorescens vid diagnos avkonformationen(tertiärstruktur) hos ett protein. Problemet är att tryptofans fluorescens är starkt påverkad av närliggande protoniserade grupper, som till exempelasparaginochglycin,som kan orsakautsläckningav tryptofans exciterade tillstånd. Ävenenergiöverföringmellan tryptofan och andra fluorescerande aminosyror är möjlig, vilket påverkar analysen, särskilt när syra använts. Tryptofan är ganska ovanlig i proteiner; oftast innehåller ett protein en eller kanske några stycken tryptofaner. Därför kan tryptofanfluorescens vara en väldigt känslig mätmetod vid konformationsbestämning av individuella tryptofaner. Det som är positivt är att man inte behöver ändra proteinets veckning vid mätningarna; man påverkar inte proteinets egenskaper.
Referenser
[redigera|redigera wikitext]Noter
[redigera|redigera wikitext]- ^”Nationalencyklopedin, essentiella aminosyror”.Nationalencyklopedin.http:// ne.se/uppslagsverk/encyklopedi/l%C3%A5ng/essentiella-aminosyror.Läst 21 juli 2017.
- ^”Kopplingen mellan autism, D-vitamin och serotonin”.nordicnutritioncouncil.Arkiverad frånoriginaletden 8 september 2017.https://web.archive.org/web/20170908024028/http:// nordicnutritioncouncil /kopplingen-mellan-autism-d-vitamin-och-serotonin/.Läst 21 juli 2017.
- ^”Niacin”.livsmedelsverket.se.https:// livsmedelsverket.se/livsmedel-och-innehall/naringsamne/vitaminer-och-antioxidanter/niacin.Läst 21 juli 2017.
Externa länkar
[redigera|redigera wikitext] Wikimedia Commons har media som rörTryptofan.
Wikimedia Commons har media som rörTryptofan.
| |||||||||||||||||||
|
