Fosfomisin
 | |
 | |
| Klinik verisi | |
|---|---|
| Ticari adlar | Monuril, Monurol, Ivozfo, diğerleri |
| Diğer adlar | Fosfomisin, fosfonomisin, fosfomisin trometamin |
| AHFS/Drugs.com | Monografi |
| MedlinePlus | a697008 |
| Lisans veri | |
| Uygulama yolu | İntravenöz,oral uygulama |
| ATC kodu | |
| Hukuki durum | |
| Hukuki durum |
|
| Farmakokinetikveri | |
| Biyoyararlanım | %30-37 (ağız yoluyla, fosfomisintrometamin); gıda alımına göre değişir |
| Protein bağlanma | Nil |
| Metabolizma | Nil |
| Eliminasyonyarı ömrü | 5,7 saat (ortalama) |
| Boşaltım | Böbrek,değişmemiş |
| Tanımlayıcılar | |
| |
| CAS Numarası |
|
| PubChemCID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Bilgi Paneli(EPA) | |
| ECHA Bilgi Kartı | 100.041.315 |
| Kimyasal ve fiziksel veriler | |
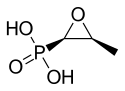
| Formül | C3H7O4P |
| Mol kütlesi | 138,059g·mol−1 |
| 3D model (JSmol) | |
| Erime noktası | 94 °C (201 °F) |
| |
Diğerlerinin yanı sıraMonurolmarkası altında satılanfosfomisin,öncelikle altidrar yolu enfeksiyonlarınıtedavi etmek için kullanılan birantibiyotiktir.[6]Böbrek enfeksiyonlarıiçinendikedeğildir.[6]Nadirenprostat enfeksiyonlarıiçin kullanılır.[6]Genellikle ağız yoluyla alınır.[6]
Yaygın yan etkiler arasındaishal,bulantı,baş ağrısıvevajinal mantar enfeksiyonlarıyer alır.[6]Ciddi yan etkiler arasındaanafilaksiveClostridioides difficileile ilişkiliishalsayılabilir.[6]Hamilelik sırasında kullanımın zararlı olduğu tespit edilmemiş olsa da bu tür bir kullanım önerilmemektedir.[7]Emzirme döneminde tek bir doz güvenli görünmektedir.[7]Fosfomisin,bakteri hücre duvarınınüretimine müdahale ederek çalışır.[6]
Fosfomisin 1969 yılında keşfedilmiş ve 1996 yılında Amerika Birleşik Devletleri'nde tıbbi kullanım için onaylanmıştır.[6][8]Dünya Sağlık Örgütünün Temel İlaçlar Listesi'nde yer almaktadır.[9]Dünya Sağlık Örgütüfosfomisini insan tıbbı için kritik öneme sahip olarak sınıflandırmaktadır.[10]Jenerik bir ilaçolarak mevcuttur.[11]Orijinal olarak belirliStreptomycestürleri tarafından üretilmiştir, ancak artık kimyasal olarak üretilmektedir.[8]
Tıbbi kullanımlar
[değiştir|kaynağı değiştir]Fosfomisin, genellikle ağız yoluyla tek doz olarak verildiğimesane enfeksiyonlarınıtedavi etmek için kullanılır.[12]
Oral fosfomisin 12 yaşın altındaki çocuklar için önerilmez.[13]
Ek kullanım alanları önerilmiştir.[14]Antimikrobiyal direncinilerlemesine ilişkin küresel sorun, son zamanlarda kullanımına yönelik ilginin yeniden artmasına yol açmıştır.[15]
Fosfomisin hem İYE'ler hem de akut piyelonefrit dahil komplike İYE'ler için etkili bir tedavi olarak kullanılabilir. Komplike İYE'ler için standart rejim, toplam 3 doz boyunca her 48 veya 72 saatte bir uygulanan oral 3 g doz veya fosfomisin IV formda verildiğinde 7-14 gün boyunca her 8 saatte bir 6 g dozdur.[16]
İntravenöz fosfomisin,çoklu ilaca dirençli bakterilerinneden olduğu enfeksiyonların tedavisinde, direnç oluşumunu önlemek ve diğer birçok antimikrobiyal ile sinerjik aktivitesinden yararlanmak için çoğunlukla ortak ilaç olarak giderek daha fazla kullanılmaktadır. Günlük yetişkin dozu genellikle 12 ila 24 gram arasında değişir.[17]Sürekli infüzyon halinde uygulandığında, 8 g fosfomisinyükleme dozunutakiben 16 g veya 24 g günlük doz uygulanır. Normal böbrek fonksiyonu olan hastalarda sürekli infüzyon önerilir.[18]
Bakteriyel duyarlılık
[değiştir|kaynağı değiştir]Fosfomisin molekülü, oldukça gergin ve dolayısıyla çok reaktif olan birepoksitveya oksiran halkasına sahiptir.[kaynak belirtilmeli]
Fosfomisin,E. faecalis,E. coliveCitrobacterveProteusgibi çeşitli Gram-negatiflere karşı yararlı aktivite ile hem Gram-pozitif hem de Gram-negatif patojenlere karşı geniş antibakteriyel aktiviteye sahiptir. Düşük pH ortamında daha fazla aktivite göstermesi ve idrarla aktif formda atılımının baskın olması nedeniyle fosfomisin, bu üropatojenlerin neden olduğu İYE'lerin profilaksisi ve tedavisinde kullanım alanı bulmuştur.S. saprophyticus,KlebsiellaveEnterobacter'e karşı aktivite değişkendir veminimum inhibitör konsantrasyontesti ile doğrulanmalıdır.Genişlemiş spektrumlu β-laktamazüreten patojenlere, özellikle de ESBL üretenE. coli'ye karşı aktivite iyi ila mükemmeldir, çünkü ilaç çapraz direnç sorunlarından etkilenmez. Mevcut klinik veriler, duyarlı organizmaların neden olduğu komplike olmayan İYE'lerde kullanımı desteklemektedir. Bununla birlikte, 64 mg/L'lik duyarlılık kırılma noktaları sistemik enfeksiyonlar için uygulanmamalıdır.[kaynak belirtilmeli]
Direnç
[değiştir|kaynağı değiştir]Tedavi altında bakteriyel direnç gelişimi sık görülen bir durumdur ve fosfomisini ciddi enfeksiyonların sürekli tedavisi için uygunsuz hale getirir. Gerekli olmayan gliserofosfat taşıyıcısını inaktive eden mutasyonlar bakterileri fosfomisine dirençli hale getirir.[19][20][21]
Fosfomisinin en az başka bir aktif ilaçla birlikte reçete edilmesi bakteriyel direnç gelişme riskini azaltır. Fosfomisin, aminoglikozidler, karbapenemler, sefalosporinler, daptomisin ve oritavansin dahil olmak üzere diğer birçok antibiyotikle sinerjik olarak etki eder.[17][22]
Fosfomisine direnç kazandıranenzimlerde tanımlanmıştır ve hemkromozomalolarak hem deplazmidlerüzerinde kodlanmaktadır.[23]
Üç ilgili fosfomisin direnç enzimi (FosA, FosB ve FosX olarak adlandırılır)glioksalazsüper ailesinin üyeleridir. Bu enzimler fosfomisinin 1 numaralı karbonuna nükleofilik saldırıda bulunarak epoksit halkasını açar ve ilacı etkisiz hale getirir.[kaynak belirtilmeli]
Enzimler, reaksiyonda kullanılan nükleofilin kimliğine göre farklılık gösterir: FosA içinglutatyon,FosB içinbakillitiol[24][25]ve FosX için su.[23]
Genel olarak, FosA ve FosX enzimleri Gram-negatif bakteriler tarafından üretilirken, FosB Gram-pozitif bakteriler tarafından üretilir.[23]
FosCATPkullanır ve fosfomisine birfosfatgrubu ekler, böylece özelliklerini değiştirir ve ilacı etkisiz hale getirir.[26]
Yan etkiler
[değiştir|kaynağı değiştir]İlaç iyi tolere edilir ve zararlı yan etki insidansı düşüktür.[12]
Etki mekanizması
[değiştir|kaynağı değiştir]Adına rağmen (-omisin ile biten) Fosfomisin birmakroliddeğil, yeni bir fosfonik antibiyotik sınıfının üyesidir. Fosfomisin bakterisidaldir ve MurA olarak da bilinenUDP-N-asetilglukozamin-3-enolpiruviltransferazenzimini inaktive ederek bakteriyel hücre duvarı biyogenezini inhibe eder.[27]Bu enzim,peptidoglikanbiyosentezinde,fosfoenolpiruvatın(PEP)UDP-N-asetilglukozaminin3'-hidroksil grubuna bağlanması gibi kararlı bir adımı katalize eder. Bu piruvat parçası, peptidoglikanın glikan ve peptit kısmı arasında köprü kuran bağlayıcıyı sağlar. Fosfomisin, bir aktif bölgesisteinkalıntısını (Escherichia colienziminde Cys 115) alkilleyerek MurA'yı inhibe eden bir PEP analoğudur.[28][29]
Fosfomisin bakteri hücresine gliserofosfat taşıyıcısı yoluyla girer.[30]
Tarihçe
[değiştir|kaynağı değiştir]Fosfomisin (orijinal adıyla fosfonomisin)Merck & Co.ve İspanya'nın Compañía Española de Penicilina y Antibióticos (CEPA) şirketinin ortak çalışmasıyla keşfedilmiştir. İlk olarak, toprak örneklerinden izole edilenStreptomyces fradiae'nin broth kültürlerinin, büyüyen bakteriler tarafındansferoplastoluşumuna neden olma yeteneği açısından taranmasıyla izole edilmiştir. Bu keşif 1969 yılında yayınlanan bir dizi makalede açıklanmıştır.[31]CEPA, 1971 yılında Aranjuez tesisinde endüstriyel ölçekte fosfomisin üretmeye başlamıştır.[32]
Üretim
[değiştir|kaynağı değiştir]Streptomyces fradiae'den fosfomisin biyosentetikgen kümesinintamamı klonlanıp dizilenmiş veS. lividans'ta fosfomisinin heterolog üretimiHuimin ZhaoveWilfred van der Donkaraştırma gruplarından Ryan Woodyer tarafından gerçekleştirilmiştir.[33]
Fosfomisinin büyük ölçekli üretimi,rasemik karışımfosfomisin elde etmek için cis-propenilfosfonik asidin birepoksitininyapılmasıyla elde edilir.[34]
Kaynakça
[değiştir|kaynağı değiştir]- ^"Prescription medicines: registration of new chemical entities in Australia, 2017".Therapeutic Goods Administration (TGA).21 Haziran 2022. 10 Nisan 2023 tarihinde kaynağındanarşivlendi.Erişim tarihi:9 Nisan2023.
- ^"Regulatory Decision Summary - Ivozfo".Health Canada.23 Ekim 2014. 7 Haziran 2022 tarihinde kaynağındanarşivlendi.Erişim tarihi:7 Haziran2022.
- ^"Monuril 3g granules for oral solution - Summary of Product Characteristics (SmPC)".(emc).1 Haziran 2021. 8 Mart 2022 tarihinde kaynağındanarşivlendi.Erişim tarihi:7 Haziran2022.
- ^"Fomicyt 40 mg/mL powder for solution for infusion - Summary of Product Characteristics (SmPC)".(emc).11 Şubat 2021. 7 Haziran 2022 tarihinde kaynağındanarşivlendi.Erişim tarihi:7 Haziran2022.
- ^"Monurol- fosfomycin tromethamine powder".DailyMed.24 Ekim 2019. 7 Haziran 2022 tarihinde kaynağındanarşivlendi.Erişim tarihi:7 Haziran2022.
- ^abcdefgh"Fosfomycin Tromethamine Monograph for Professionals".Drugs.com(İngilizce). 29 Ekim 2019 tarihinde kaynağındanarşivlendi.Erişim tarihi:29 Ekim2019.
- ^ab"Fosfomycin (Monurol) Use During Pregnancy".Drugs.com(İngilizce). 29 Ekim 2019 tarihinde kaynağındanarşivlendi.Erişim tarihi:29 Ekim2019.
- ^abFinch RG, Greenwood D, Whitley RJ, Norrby SR (2010).Antibiotic and Chemotherapy E-Book(İngilizce). Elsevier Health Sciences. s. 259.ISBN9780702047657.
- ^World Health Organization(2019).World Health Organization model list of essential medicines: 21st list 2019.Cenevre: World Health Organization.hdl:10665/325771.WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^World Health Organization(2019).Critically important antimicrobials for human medicine.6th revision. Cenevre: World Health Organization.hdl:10665/312266.ISBN9789241515528.
- ^British national formulary: BNF 76.76. Pharmaceutical Press. 2018. ss. 560-561.ISBN9780857113382.
- ^abPatel SS, Balfour JA, Bryson HM (April 1997). "Fosfomycin tromethamine. A review of its antibacterial activity, pharmacokinetic properties and therapeutic efficacy as a single-dose oral treatment for acute uncomplicated lower urinary tract infections".Drugs.53(4). ss. 637-656.doi:10.2165/00003495-199753040-00007.PMID9098664.
- ^"MONURIL SACHETS 3G".28 Mayıs 2014 tarihinde kaynağındanarşivlendi.Erişim tarihi: 26 Mayıs 2014.
- ^Falagas ME, Giannopoulou KP, Kokolakis GN, Rafailidis PI (April 2008). "Fosfomycin: use beyond urinary tract and gastrointestinal infections".Clinical Infectious Diseases.46(7). ss. 1069-1077.doi:10.1086/527442.PMID18444827.
- ^Falagas ME, Grammatikos AP, Michalopoulos A (October 2008). "Potential of old-generation antibiotics to address current need for new antibiotics".Expert Review of Anti-Infective Therapy.6(5). ss. 593-600.doi:10.1586/14787210.6.5.593.PMID18847400.
- ^Zhanel GG, Zhanel MA, Karlowsky JA (28 Mart 2020). "Oral and Intravenous Fosfomycin for the Treatment of Complicated Urinary Tract Infections".The Canadian Journal of Infectious Diseases & Medical Microbiology.Cilt 2020. Hindawi Limited. s. 8513405.doi:10.1155/2020/8513405.PMC7142339 $2.PMID32300381.
- ^abAntonello RM, Principe L, Maraolo AE, Viaggi V, Pol R, Fabbiani M, ve diğerleri. (August 2020). "Fosfomycin as Partner Drug for Systemic Infection Management. A Systematic Review of Its Synergistic Properties from In Vitro and In Vivo Studies".Antibiotics.9(8). s. 500.doi:10.3390/antibiotics9080500.PMC7460049 $2.PMID32785114.
- ^Antonello RM, Di Bella S, Maraolo AE, Luzzati R (June 2021). "Fosfomycin in continuous or prolonged infusion for systemic bacterial infections: a systematic review of its dosing regimen proposal from in vitro, in vivo and clinical studies".European Journal of Clinical Microbiology & Infectious Diseases.40(6). ss. 1117-1126.doi:10.1007/s10096-021-04181-x.PMC8139892 $2.PMID33604721.
- ^Kahan FM, Kahan JS, Cassidy PJ, Kropp H (May 1974). "The mechanism of action of fosfomycin (phosphonomycin)".Annals of the New York Academy of Sciences.235(1). ss. 364-386.Bibcode:1974NYASA.235..364K.doi:10.1111/j.1749-6632.1974.tb43277.x.PMID4605290.
- ^Castañeda-García A, Blázquez J, Rodríguez-Rojas A (April 2013). "Molecular Mechanisms and Clinical Impact of Acquired and Intrinsic Fosfomycin Resistance".Antibiotics.2(2). ss. 217-236.doi:10.3390/antibiotics2020217.PMC4790336 $2.PMID27029300.
- ^Lagatolla C, Mehat JW, La Ragione RM, Luzzati R, Di Bella S (September 2022). "In Vitro and In Vivo Studies of Oritavancin and Fosfomycin Synergism against Vancomycin-ResistantEnterococcus faecium".Antibiotics.11(10). s. 1334.doi:10.3390/antibiotics11101334.PMC9598191 $2.PMID36289992.
- ^abcRigsby RE, Fillgrove KL, Beihoffer LA, Armstrong RN (2005)."Fosfomycin resistance proteins: a nexus of glutathione transferases and epoxide hydrolases in a metalloenzyme superfamily".Gluthione [sic] Transferases and Gamma-Glutamyl Transpeptidases.Methods in Enzymology.401.ss.367-379.doi:10.1016/S0076-6879(05)01023-2.ISBN9780121828066.PMID16399398.
- ^Sharma SV, Jothivasan VK, Newton GL, Upton H, Wakabayashi JI, Kane MG, ve diğerleri. (July 2011). "Chemical and Chemoenzymatic syntheses of bacillithiol: a unique low-molecular-weight thiol amongst low G + C Gram-positive bacteria".Angewandte Chemie.50(31). ss. 7101-7104.doi:10.1002/anie.201100196.PMID21751306.
- ^Roberts AA, Sharma SV, Strankman AW, Duran SR, Rawat M, Hamilton CJ (April 2013). "Mechanistic studies of FosB: a divalent-metal-dependent bacillithiol-S-transferase that mediates fosfomycin resistance in Staphylococcus aureus".The Biochemical Journal.451(1). ss. 69-79.doi:10.1042/BJ20121541.PMC3960972 $2.PMID23256780.
- ^García P, Arca P, Evaristo Suárez J (July 1995)."Product of fosC, a gene from Pseudomonas syringae, mediates fosfomycin resistance by using ATP as cosubstrate".Antimicrobial Agents and Chemotherapy.39(7). ss. 1569-1573.doi:10.1128/aac.39.7.1569.PMC162783 $2.PMID7492106.
- ^Brown ED, Vivas EI, Walsh CT, Kolter R (July 1995)."MurA (MurZ), the enzyme that catalyzes the first committed step in peptidoglycan biosynthesis, is essential in Escherichia coli".Journal of Bacteriology.177(14). ss. 4194-4197.doi:10.1128/jb.177.14.4194-4197.1995.PMC177162 $2.PMID7608103.
- ^Zhu JY, Yang Y, Han H, Betzi S, Olesen SH, Marsilio F, Schönbrunn E (April 2012). "Functional consequence of covalent reaction of phosphoenolpyruvate with UDP-N-acetylglucosamine 1-carboxyvinyltransferase (MurA)".The Journal of Biological Chemistry.287(16). ss. 12657-12667.doi:10.1074/jbc.M112.342725.PMC3339971 $2.PMID22378791.
- ^Krekel F, Samland AK, Macheroux P, Amrhein N, Evans JN (October 2000). "Determination of the pKa value of C115 in MurA (UDP-N-acetylglucosamine enolpyruvyltransferase) from Enterobacter cloacae".Biochemistry.39(41). ss. 12671-12677.doi:10.1021/bi001310x.PMID11027147.
- ^Santoro A, Cappello AR, Madeo M, Martello E, Iacopetta D, Dolce V (December 2011). "Interaction of fosfomycin with the glycerol 3-phosphate transporter of Escherichia coli".Biochimica et Biophysica Acta (BBA) - General Subjects.1810(12). ss. 1323-1329.doi:10.1016/j.bbagen.2011.07.006.PMID21791237.
- ^Silver LL (2011). "Rational Approaches to Antibacterial Discovery: Pre-Genomic Directed and Phenotypic Screening". Dougherty T, Pucci MJ (Ed.).Antibiotic Discovery and Development.Springer. s. 46.doi:10.1007/978-1-4614-1400-1_2.ISBN978-1-4614-1400-1.
- ^"About us: Our history".Encros.14 Eylül 2011 tarihindekaynağındanarşivlendi.
- ^Woodyer RD, Shao Z, Thomas PM, Kelleher NL, Blodgett JA, Metcalf WW, ve diğerleri. (November 2006). "Heterologous production of fosfomycin and identification of the minimal biosynthetic gene cluster".Chemistry & Biology.13(11). ss. 1171-1182.doi:10.1016/j.chembiol.2006.09.007.PMID17113999.
- ^Marocco CP, Davis EV, Finnell JE, Nguyen PH, Mateer SC, Ghiviriga I, ve diğerleri. (2011). "Asymmetric synthesis of (−)-fosfomycin and its trans-(1S,2S)-diastereomer using a biocatalytic reduction as the key step".Tetrahedron: Asymmetry.22(18–19). Elsevier BV. ss. 1784-1789.doi:10.1016/j.tetasy.2011.10.009.ISSN0957-4166.
Dış bağlantılar
[değiştir|kaynağı değiştir]- "Fosfomycin".Drug Information Portal.U.S. National Library of Medicine. 18 Ağustos 2016 tarihindekaynağındanarşivlendi.
