Коваксин
Зауважте,Вікіпедія не дає медичних порад! Якщо у вас виникли проблеми зі здоров'ям — зверніться до лікаря. |
| |
| ? | |
| Ідентифікатори | |
| Номер CAS | ? |
| Код ATC | ? |
| PubChem | ? |
| DrugBank | |
| Хімічні дані | |
| Формула | ? |
| Мол. маса | ? |
| Фармакокінетичні дані | |
| Біодоступність | ? |
| Метаболізм | ? |
| Період напіврозпаду | ? |
| Виділення | ? |
| Терапевтичні застереження | |
| Кат. вагітності |
? |
| Лег. статус |
невідкладна реєстрація вІндії |
| Шляхи введення | в/м |
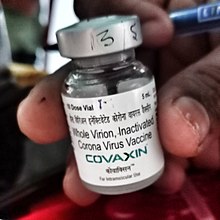
BBV152,відома також під назвоюКоваксин (Covaxin)— кандидат навакцину проти COVID-19,який створений на основі інактивованого вірусуSARS-CoV-2,яку виробляє індійська компанія«Bharat Biotech»у співпраці зІндійською радою з медичних досліджень.
У травні 2020 року Національний інститут вірусологіїІндійської ради з медичних дослідженьсхвалив і забезпечив штамами вірусів розробку повністю інактивованоївакцини проти COVID-19.[1][2]У червні 2020 року компанія«Bharat Biotech»отримала дозвіл на проведення досліджень на людях І та ІІ фази вакцини проти COVID-19, яка отримала назву «Covaxin», від державного агентства з контролю за ліками Індії.[3]Індійська рада з медичних досліджень обрала загалом 12 місць для проведення I та II фаз рандомізованих, подвійних сліпих та плацебо-контрольованих клінічних досліджень кандидата на вакцину.[4][5][6]
У грудні 2020 року компанія опублікувала звіт про I фазу клінічного дослідження та представила результати упрепринтіmedRxiv.[7][8][9]
У листопаді 2020 року компанія «Bharat Biotech» отримав дозвіл проводити III фази клінічного дослідження на людях кандидата на вакцину «Коваксин»[10]після завершення I і II фаз.[11]Це дослідження проводилось як рандомізоване, подвійне сліпе, плацебо-контрольоване дослідження серед добровольців вікової групи від 18 років, та розпочалось 25 листопада.[12]У III фазі дослідження брали участь близько 26 тисяч добровольців з усієї Індії.[13]III фаза клінічного дослідження охоплять загалом 22 місцевості в кількох штатах країни, включаючиДелі,Карнатаку,Західну Бенгалію,та низку інших штатів, які за очікуваннями, мають приєднатися до проведення дослідження за короткий час.[14]
Згідно результатів досліджень, у Bharat Biotech заявили, що вакцина Covaxin захищає від важких форм хвороби і штаму «Дельта» COVID-19[15][16].
Компанія«Bharat Biotech»виробляє кандидата на вакцину «Коваксин» на власному заводі за технологією її створення з клітинверо[17],на якому можна виробити близько 300 мільйонів доз вакцини.[18]Компанія перебуває в процесі створення другого заводу на своєму заводі в Геномній Долині вГайдарабадідля виробництва вакцини «Коваксин». Фірма веде переговори з іншими урядами штатів, зокрема штатуОдіша[19],щодо іншого місця в країні для виготовлення вакцини. Крім цього, також розглядається питання щодо вироблення вакцини в інших країнах світу.[20]У грудні 2020 року компанія «Ocugen Inc» уклала партнерські відносини з «Bharat Biotech» для спільного просування «Коваксину» на американському ринку.[21][22]
Компанія«Bharat Biotech»звернулася до державного агентства з контролю за ліками Індії та уряду Індії з проханням на дозвіл на екстрене використання вакцини «Коваксин».[23]Вона стала третьою компанією післяІнституту сироваток Індіїта компанії«Pfizer»,яка подала заявку на затвердження використання вакцини у надзвичайній ситуації.[24]
2 січня 2021 року центральний контрольний орган зі стандартизації ліків рекомендував надати дозвіл на екстрене використання вакцини «Коваксин»[25],який був наданий з 3 січня.[26]
- ↑ICMR teams up with Bharat Biotech to develop Covid-19 vaccine.Livemint(англ.).9 травня 2020. Архіворигіналуза 3 Травня 2021.Процитовано 9 Січня 2021.
- ↑Chakrabarti A (10 травня 2020).India to develop 'fully indigenous' Covid vaccine as ICMR partners with Bharat Biotech.ThePrint.Архіворигіналуза 3 Травня 2021.Процитовано 9 Січня 2021.(англ.)
- ↑India's First COVID-19 Vaccine Candidate Approved for Human Trials.The New York Times.29 червня 2020. Архіворигіналуза 13 Лютого 2021.Процитовано 9 Січня 2021.(англ.)
- ↑Human clinical trials of potential Covid-19 vaccine ‘COVAXIN’ started at AIIMS.DD News.Prasar Bharati, Ministry of I & B, Government of India. 25 липня 2020. Архіворигіналуза 24 Січня 2021.Процитовано 10 Січня 2021.(англ.)
- ↑Press, Associated (25 липня 2020).Asia Today: Amid new surge, India tests potential vaccine.Washington Post.Архіворигіналуза 16 Лютого 2021.Процитовано 17 грудня 2020.(англ.)
- ↑Delhi: 30-year-old is first to get dose of trial drug Covaxin.The Indian Express(англ.).25 липня 2020. Архіворигіналуза 16 Березня 2021.Процитовано 10 Січня 2021.
- ↑Ella, Raches; Mohan, Krishna; Jogdand, Harsh; Prasad, Sai; Reddy, Siddharth; Sarangi, Vamshi Krishna; Ganneru, Brunda; Sapkal, Gajanan; Yadav, Pragya; Panda, Samiran; Gupta, Nivedita; Reddy, Prabhakar; Verma, Savita; Rai, Sanjay; Singh, Chandraman; Redkar, Sagar; Gillurkar, ChandraSekhar; Kushwaha, Jitendra Singh; Rao, Venkat; Mohapatra, Satyajit; Guleria, Randeep; Ella, Krishna; Bhargava, Balram (15 грудня 2020).Safety and immunogenicity trial of an inactivated SARS-CoV-2 vaccine-BBV152: a phase 1, double-blind, randomised control trial.medRxiv(англ.).doi:10.1101/2020.12.11.20210419.Архіворигіналуза 22 Листопада 2021.Процитовано 10 Січня 2021.
- ↑Perappadan, Bindu Shajan (16 грудня 2020).Coronavirus | Covaxin phase-1 trial results show promising results.The Hindu(англ.).Архіворигіналуза 17 Грудня 2020.Процитовано 17 грудня 2020.
- ↑Sabarwal, Harshit (16 грудня 2020).Covaxin’s phase 1 trial result shows robust immune response, mild adverse events.Hindustan Times(англ.).Архіворигіналуза 16 Грудня 2020.Процитовано 17 грудня 2020.
- ↑Coronavirus | Covaxin Phase III trial from November.The Hindu(англ.).23 жовтня 2020. Архіворигіналуза 26 Січня 2021.Процитовано 10 Січня 2021.
- ↑Ganneru B, Jogdand H, Daram VK, Molugu NR, Prasad SD, Kannappa SV, Ella KM, Ravikrishnan R, Awasthi A, Jose J, Rao P (9 вересня 2020). Evaluation of Safety and Immunogenicity of an Adjuvanted, TH-1 Skewed, Whole Virion InactivatedSARS-CoV-2 Vaccine - BBV152.doi:10.1101/2020.09.09.285445.
{{cite journal}}:Недійсний|display-authors=6(довідка)(англ.) - ↑An Efficacy and Safety Clinical Trial of an Investigational COVID-19 Vaccine (BBV152) in Adult Volunteers.clinicaltrials.gov(Registry). United States National Library of Medicine. NCT04641481. Архіворигіналуза 26 Листопада 2020.Процитовано 26 листопада 2020.(англ.)
- ↑Bharat Biotech begins Covaxin Phase III trials.The Indian Express(англ.).18 листопада 2020. Архіворигіналуза 22 Січня 2021.Процитовано 10 Січня 2021.
- ↑Sen M (2 грудня 2020).List of states that have started phase 3 trials of India's first Covid vaccine.mint(англ.).Архіворигіналуза 13 Лютого 2021.Процитовано 10 Січня 2021.
- ↑India's Bharat Biotech says vaccine 93.4% effective against severe COVID-19.Reuters.3 липня 2021. Архіворигіналуза 5 Липня 2021.Процитовано 5 липня 2021.
- ↑Індійська вакцина Covaxin захищає від важких симптомів COVID і штаму "Дельта".РБК-Украина(рос.).Архіворигіналуза 5 Липня 2021.Процитовано 5 липня 2021.
- ↑Hoeksema F, Karpilow J, Luitjens A, Lagerwerf F, Havenga M, Groothuizen M, Gillissen G, Lemckert AA, Jiang B, Tripp RA, Yallop C (Квітень 2018). Enhancing viral vaccine production using engineered knockout vero cell lines - A second look.Vaccine.36(16): 2093—2103.doi:10.1016/j.vaccine.2018.03.010.PMID29555218.
{{cite journal}}:Недійсний|display-authors=6(довідка)(англ.) - ↑Coronavirus vaccine update: Bharat Biotech's Covaxin launch likely in Q2 of 2021, no word on pricing yet.businesstoday.in.India Today Group. Архіворигіналуза 11 Грудня 2020.Процитовано 13 грудня 2020.(англ.)
- ↑Odisha fast tracks coronavirus vaccine manufacturing unit.The New Indian Express.7 листопада 2020. Архіворигіналуза 22 Січня 2021.Процитовано 10 Січня 2021.(англ.)
- ↑Raghavan P (24 вересня 2020).Bharat Biotech exploring global tie-ups for Covaxin manufacturing.The Indian Express(англ.).Архіворигіналуза 22 Січня 2021.Процитовано 10 Січня 2021.
- ↑Reuters Staff (22 грудня 2020).Ocugen to co-develop Bharat Biotech's COVID-19 vaccine candidate for U.S.Reuters(англ.).Архіворигіналуза 26 Грудня 2020.Процитовано 5 січня 2021.
- ↑Bharat Biotech, Ocugen to co-develop Covaxin for US market.The Economic Times.Архіворигіналуза 5 Липня 2021.Процитовано 5 січня 2021.(англ.)
- ↑Ghosh N (7 грудня 2020).Bharat Biotech seeks emergency use authorization for Covid-19 vaccine.Hindustan Times(англ.).Архіворигіналуза 24 Грудня 2020.Процитовано 10 Січня 2021.
- ↑Coronavirus | After SII, Bharat Biotech seeks DCGI approval for Covaxin.The Hindu(англ.).7 грудня 2020. Архіворигіналуза 24 Грудня 2020.Процитовано 10 Січня 2021.
- ↑Expert panel recommends granting approval for restricted emergency use of Bharat Biotech’s Covaxin.The Indian Express(англ.).2 січня 2021. Архіворигіналуза 26 Січня 2021.Процитовано 10 Січня 2021.
- ↑Coronavirus: India approves vaccines from Bharat Biotech and Oxford/AstraZeneca.BBC News(англ.).3 січня 2021. Архіворигіналуза 3 Січня 2021.Процитовано 3 січня 2021.
- How Bharat Biotech's Vaccine Works[Архівовано3 Серпня 2021 уWayback Machine.](англ.)