Hóa sinh
| Đây là một trong loạt bài về |
| Hóa sinh |
|---|
 |
| Các nét quan trọng |
| Lịch sử và chủ đề |
| Thuật ngữ |
| Lĩnh vực:Sinh học,Sinh học phân tử, tế bào |
Hóa sinh(tiếng Anh:Biochemistryhaybiological chemistry) là phân ngành nghiên cứu cácquá trình hóa họcbên trong và liên quan tớisinh vậtsống.[1]Là một phân ngành của cảhóa họcvàsinh học,hóa sinh có thể thể được chia làm ba lĩnh vực:sinh học cấu trúc,enzymvàtrao đổi chất.Suốt những thập niên cuối của thế kỷ 20, ngành hóa sinh đã thành công trong việc giải thích các quá trình sống nhờ ba phân ngành kể trên. Hầu hết mọilĩnh vực của các môn khoa học sự sốngđang được khám phá và phát triển nhờ nghiên cứu và phương pháp hóa sinh học.[2]Hóa sinh chú trọng vào vốn hiểu biết về cơ sở hóa học cho phép nhữngphân tử sinh họctạo nên các quá trình xảy trongtế bàosống và giữa các tế bào,[3]đổi lại liên quan mật thiết tới vốn hiểu biết vềmôvàcơ quan,cũng như cấu trúc và chức năng của sinh vật.[4]Hóa sinh có mối quan hệ mật thiết tớisinh học phân tử,ngành nghiên cứu các cơ chếphân tửcủa hiện tượng sinh học.[5]
Phần lớn hóa sinh liên quan tới các cấu trúc, liên kết, chức năng, tương tác của nhữngđại phân tửsinh học, chẳng hạn nhưprotein,acid nucleic,carbohydratevàlipid.Chúng cung cấp cấu trúc của tế bào và thực hiện nhiều chức năng liên quan tới sự sống.[6]Mảng hóa học của tế bào còn phụ thuộc vào phản ứng của nhữngphân tửvàionnhỏ. Chúng có thể làhợp chất vô cơ(ví dụ nhưnướcvà ionkim loại) hoặchữu cơ(ví dụacid amin,chất được dùng đểtổng hợp các protein).[7]Những cơ chế màtế bào sử dụng để chuyển hóa năng lượngtừ môi trường thông qua cácphản ứng hóa họcđược gọi làtrao đổi chất.Những phát hiện trong môn hóa sinh được ứng dụng chủ yếu trongy học,dinh dưỡngvànông nghiệp.Trong y học, các nhà hóa sinh nghiên cứu nguyên nhân gây bệnh vàcác liều thuốctrịbệnh.[8]Dinh dưỡng thì nghiên cứu cách duy trì sức khỏe và thể trạng và cả những hệ quả củakém dinh dưỡng.[9]Trong nông nghiệp, các nhà hóa sinh nghiên cứuđấtvàphân bón,bên cạnh đó là các mục tiêu cải thiện canh tác, bảo quản cây trồng vàkiểm soát loài gây hại.
Lịch sử
[sửa|sửa mã nguồn]
Theo định nghĩa bao hàm trọn vẹn nhất, hóa sinh có thể được xem là ngành nghiên cứu các thành phần và cấu tạo của sinh vật, cách chúng kết hợp với nhau để trở thành sự sống. Theo nghĩa này, do đó lịch sử hóa sinh có thể truy ngược về thờiHy Lạp cổ đại.[10]Tuy nhiên, hóa sinh dưới dạng mộtphân ngành khoa họcchuyên biết bắt đầu vào khoảng thế kỷ 19 (hoặc sớm hơn một chút), phụ thuộc vào khía cạnh nào mà hóa sinh đang chú trọng tới. Một số người cho rằng khởi đầu của hóa sinh có thể là phát hiệnenzymeđầu tiên,diastase(nay được gọi làamylase) củaAnselme Payenvào năm 1833,[11]trong khi một bộ phận khác xem màn trình bày một quá trìnhlên men rượuhóa sinh phức tạp củaEduard Buchnertrong các chiết xuất không tế bào vào năm 1897 là sự ra đời của hóa sinh.[12][13][14]Một số người khác cũng chỉ ra rằng hóa sinh khởi đầu bằng một công trình giàu ảnh hưởng củaJustus von Liebigvào năm 1842,Animal chemistry, or, Organic chemistry in its applications to physiology and pathology- tác phẩm trình bày lý thuyết hóa học về trao đổi chất,[10]hay thậm chí sớm hơn nữa là những nghiên cứu vềlên menvàhô hấpcủaAntoine Lavoisiervào thế kỷ 18.[15][16]Nhiều nhà tiên phong trong mảng hóa sinh đã giúp tầng phức tạp của hóa sinh và họ được xem là những người đặt nền móng cho hóa sinh hiện đại.Emil Fischer(tác giả nghiên cứu hóa học của protein)[17]vàF. Gowland Hopkins(tác giả nghiên cứu enzyme và bản chất động lực học của hóa sinh) là hai ví dụ đại diện cho hóa sinh thời kì đầu.[18]
Bản thân thuật ngữ "biochemistry" (hóa sinh) xuất phát từ sự kết hợp giữasinh họcvàhóa học.Năm 1877,Felix Hoppe-Seylersử dụng thuật ngữ (biochemietrongtiếng Đức) như một từ đồng nghĩa vớihóa sinh lýtrong phần lời tựa đầu cho số đầu tiên củaZeitschrift für Physiologische Chemie(Tạp chí hóasinh lý học), nơi ông lập luận cho việc thành lập các viện nghiên cứu dành riêng cho lĩnh vực này.[19][20]Tuy nhiên nhà hóa học người ĐứcCarl Neubergthường được xem là người đặt ra từ này vào năm 1903,[21][22][23]trong khi ấy một số người lại ghi công choFranz Hofmeister.[24]
Người ta thường tin rằng sự sống và các vật chất có một số thuộc tính hoặc chất thiết yếu (thường được xem là "sinh lực luận"), khác với bất kì thứ gì được tìm thấy ở vật thể không sống, và người ta cho rằng chỉ vật thể sống mới có thể tạo ra các phân tử của sự sống.[26]Năm 1828,Friedrich Wöhlerxuất bản một bài báo về quá trìnhtổng hợpuretình cờ của ông từ potassium cyanat và ammonium sulfat; một số người coi đấy là bàn đạp đổ trực tiếp lên sinh lực luận và thành lập nênhóa học hữu cơ.[27][28]Tuy nhiên, phép tổng hợp của Wöhler gây tranh cãi vì một số người bác bỏ cái chết của sinh lực luận trên bàn tay ông.[29]Kể từ ấy, hóa sinh đã tiến bộ vượt bậc, đặc biệt từ giữa thế kỷ 20, với sự phát triển của những kỹ thuật mới nhưsắc ký,tinh thể học tia X,phép đo giao thoa phân cực kép,quang phổ NMR,dán nhãn đồng vị,dùngkính hiển vi điện tửvà mô phỏngđộng lực học phân tử.Những kỹ thuật này cho phép khám phá và phân tích chi tiết nhiều phân tử và các conđường trao đổi chấtcủatế bào,ví dụ nhưđường phânvàchu trình Krebs(chu trình acid citric), và dẫn tới vốn hiểu biết hóa sinh ở cấp độ phân tử.
Một sự kiện bước ngoặt khác trong lịch sử hóa sinh là việc khám phá ragenvà vai trò của nó trong việc truyền thông tin trong tế bào. Ở thập niên 1950,James D. Watson,Francis Crick,Rosalind FranklinvàMaurice Wilkinslà những người có công trong việc giải cấu trúc DNA và trình bày mối quan hệ của nó với vận chuyển thông tin di truyền.[30]Năm 1958,George BeadlevàEdward Tatumnhậngiải Nobelvì công trình nghiên cứu nấm thể hiệnmột gen tạo ra một enzym.[31]Năm 1988,Colin Pitchforklà người đầu tiên bị kết tội ám sát bằng bằng chứngDNA,dẫn tới sự phát triển của ngànhkhoa học pháp y.[32]Gần đây hơn,Andrew Z. FirevàCraig C. Mellonhậngiải Nobel 2006vì phát hiện ra vai tròcan thiệp RNA(RNAi), trong việc làm vô hiệubiểu hiện gen.[33]
Nguyên vật liệu khởi đầu: những nguyên tố hóa học của sự sống
[sửa|sửa mã nguồn]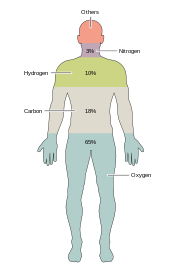
Khoảng hai tánguyên tố hóa họclà thiết yếu với nhiều kiểusống sinh học.Hầu hết các nguyên tố hiếm trên Trái Đất không cần thiết đối với sự sống (ngoại trừselenivàiod),[34]trong khi một số ít loại nguyên tố thông thường (nhômvàtitani) không được dùng đến. Hầu hết sinh vật có chung nhu cầu dùng tới nguyên tố, song có một số ít khác biệt giữathực vậtvàđộng vật.Ví dụ, tảo biển sử dụngbrom,nhưng thực vật trên cạn và động vật dường như không cần tới nguyên tố ấy. Tất cả động vật đều cầnnatri,nhưng một vài thực vật thì không. Thực vật cần đếnborvàsilic,nhưng thực vật có thể không cần (hoặc có thể cần một lượng rất ít).
Chỉ có 6 nguyên tố—carbon,hydro,nitro,oxy,calcivàphosphor—chiếm gần 99% khối lượng tế bào sống, tính cả những tế bào ở cơ thể người (xem danh sách hoàn chỉnh ở bàithành phần cơ thể người). Ngoài 6 nguyên tố chính cấu thành nên phần lớn cơ thể người, thì con người cần tới một lượng nhỏ gồm 18 nguyên tố trở lên.[35]
Phân tử sinh học
[sửa|sửa mã nguồn]4 lớp phân tử chính trong ngành hóa sinh (thường gọi làphân tử sinh học) làcarbohydrat,lipid,proteinvàacid nucleic.[36]Nhiều phân tử sinh học là cácpolymer:theo thuật ngữ này,monomerlà những đại phân tử tương đối nhỏ liên kết với nhau để tạo rađại phân tửlớn còn gọi là các polymer. Khi các monomer liên kết với nhau để tổng hợp mộtpolymer sinh học,chúng trải qua một quá trình gọi làtổng hợp khử nước.Những đại phân tử khác nhau có thể tập hợp ở các phức hợp to hơn, thường để phục vụhoạt tính sinh học.
Carbohydrat
[sửa|sửa mã nguồn]Hai trong số những chức năng chính của carbohydrat là dự trữ năng lượng và cung cấp cấu trúc. Một trong những loạiđườngphổ biến nhất, glucose là carbohydrat, nhưng không phải tất cả carbohydrat đều là đường. Có nhiều carbohydrat trên Trái Đất hơn bất kì loại phân tử sinh học nào được biết tới; chúng được dùng để dự trữ năng lượng vàthông tin di truyền,cũng như đóng vai trò quan trọng trong cáctương tácvàliên hệcủa tế bào.
Loại carbohydrat đơn giản nhất làmonosaccharide,với đặc tính chứa carbon, hydro và oxyg, chủ yếu theo tỷ lệ 1:2:1 (công thức tổng quát là CnH2nOn,nít nhất từ 3 trở lên).Glucose(C6H12O6) là một trong những carbohydrat quan trọng nhất; những loại khác gồmfructose(C6H12O6) – loại đường thường liên quan tớivị ngọtcủatrái cây,[37][a]vàdeoxyribose(C5H10O4), một thành phần củaDNA.Một monosaccharide có thể chuyển đổi giữa dạngmạch hởvàmạch vòng.Dạng mạch hở có thể biến thành một vòng nguyên tử carbon, với cầu nối là một nguyên tửoxygenđược tạo ra từnhóm chức carbonylcủa nguyên tử cuối và nhómhydroxylcủa một nguyên tử nữa. Phân tử mạch vòng mang nhóm chứchemiacetalhoặchemiketal,phụ thuộc vào dạng mạch thẳng là mộtaldosehay mộtketose.[38]
Ở những dạng mạch vòng này, vòng thường có5hoặc6nguyên tử. Những dạng này được gọi làfuranosevàpyranose— lần lượt tương đương vớifuranvàpyran,những hợp chất đơn giản nhất cùng mang vòng carbon-oxy (mặc dù chúng thiếuliên kết đôicarbon-carbon của hai phân tử này). Ví dụ, aldohexoseglucosecó thể hình thành một liên kết hemiacetal giữa nhóm hydroxyl trên carbon 1 và oxy trên carbon 4, tạo ra phân tử mang vòng 5-cạnh, gọi làglucofuranose.Phản ứng tương tự có thể xảy ra giữa các carbon 1 và 5 để hình thành nên một phân tử mang vòng 6-cạnh, gọi làglucopyranose.Những dạng mạch vòng có 7-cạnh gọi làheptosesthì hiếm.
Lipid
[sửa|sửa mã nguồn]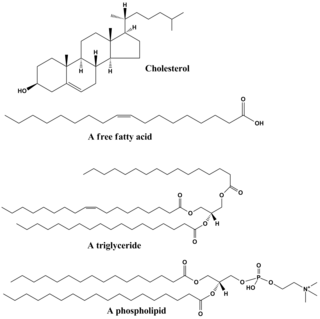
Lipidtập hợp một lượng lớnphân tửvà ở mức độ nào đấy là chất xúc tác đối với các hợp chất không tan trong nước hoặcphi phân cựccó nguồn gốc sinh học, bao gồmsáp,acid béo,phospholipid,sphingolipid,glycolipidvàterpenoidbắt nguồn từ acid béo (ví dụ,retinoidvàsteroid). Một số lipid là các phân tửkhông vòng,mạch hở và thẳng, trong khi số khác có cấu trúc mạch vòng. Một vài làchất thơm(mang cấu trúc mạch vòng và mạch thẳng) trong khi số khác thì không. Một số chất thì ling hoạt, trong khi số khác thì cố định.
Lipid thường được làm một phân tửglycerolkết hợp với các phân tử khác. Trongtriglyceride(nhóm chính của lipid lớn), có một phân tử glycerol và baacid béo.Trong trường hợp ấy, các acid béo được xem là monomer, và có thể làhợp chất bão hòa(khôngliên kết đôitrong chuỗi carbon) hoặc không bão hòa (một hoặc nhiều liên kết đôi trong chuỗi carbon).
Hầu hết lipid có vài đặc tínhphân cựcngoài đa phần là phi phân cực. Nhìn chung, số lượng lớn cấu trúc của chúng là phi phân cực hoặc làchất kị nước,tức là nó không tương tác tốt với cácdung môiphân cực như nước. Phần khác trong cấu trúc của chúng là phân cực hoặcchất ưa nướcvà sẽ có xu hướng liên kết với các dung môi phân cực như nước. Điều này biến chúng thành các phân tửlưỡng phần(tức có cả phần ưa nước lẫn kị nước). Trong trường hợp củacholesterol,nhóm phân cực chỉ là –OH (hydroxyl hoặc alcohol). Trong trường hợp của phospholipid, nhóm phân cực lớn hơn đáng kể và có tính phân cực hơn.
Protein
[sửa|sửa mã nguồn]Proteinlà những phân tử rất lớn—đại-polymer sinh học—được tạo ra từ những monomer làamino acid.Một amino acid tập hợp gồm một nguyên tử alpha carbon gắn với một nhómamino,–NH2,một nhómcarboxylic acid,–COOH (mặc dù chúng tồi tại dưới dạng –NH3+và –COO−trong điều kiện sinh lý), một nguyên tử hydro đơn giản, và một nhánh bên ghi là "–R". Nhánh bên "R" khác nhau với từng amino acid vốn có tới 20nhóm chuẩn.Chính nhóm "R" này làm từng amino acid khác biệt, và đặc tính của các nhánh bên có ảnh hưởng rất lớn tớihình dạng ba chiềucủa một protein. Một vài amino acid tự mang chức năng hoặc ở dạng biến đổi; ví dụ, chức năng củaglutamiclà mộtchất dẫn truyền thần kinhquan trọng. Những amino acid có thể tương tác thông qua mộtliên kết peptide.Trong phép tổng hợpkhử nướcnày, một phân tử nước bị loại bỏ và liên kết peptide kết nối nitơ của một nhóm amino thuộc amino tới carbon thuộc nhóm acid carboxylic của một amino acid khác. Phân tử ra đời được gọi là mộtdipeptide,còn các đoạn ngắn của amino acid (thông thường từ 30 trở xuống) được gọi là cácpeptidehay polypeptide. Những đoạn dài hơn thì được chọn làm cácproteinchủ đạo. Lấy ví dụ,albuminproteinhuyết tươngchứa 585 gốc amino acid.[41]
Tham khảo
[sửa|sửa mã nguồn]- ^“Biological/Biochemistry”.acs.org.
- ^Voet(2005), tr. 3.
- ^Karp(2009), tr. 2.
- ^Miller(2012). tr. 62.
- ^Astbury(1961), p. 1124.
- ^Eldra(2007), tr. 45.
- ^Marks(2012), Chương 14.
- ^Finkel(2009), tr. 1–4.
- ^UNICEF(2010), tr. 61, 75.
- ^abHelvoort(2000), tr. 81.
- ^Hunter(2000), tr. 75.
- ^Srinivasan, Bharath (27 tháng 9 năm 2020).“Words of advice: teaching enzyme kinetics”.The FEBS Journal.288(7): 2068–2083.doi:10.1111/febs.15537.ISSN1742-464X.PMID32981225.
- ^Hamblin(2005), tr. 26.
- ^Hunter(2000), tr. 96–98.
- ^Berg(1980), tr. 1–2.
- ^Holmes(1987), tr. xv.
- ^Feldman(2001), tr. 206.
- ^Rayner-Canham(2005), tr. 136.
- ^Ziesak(1999), tr. 169.
- ^Kleinkauf(1988), tr. 116.
- ^Ben-Menahem(2009), tr. 2982.
- ^Amsler(1986), tr. 55.
- ^Horton(2013), tr. 36.
- ^Kleinkauf(1988), tr. 43.
- ^Edwards(1992), pp. 1161–1173.
- ^Fiske(1890), tr. 419–20.
- ^Wöhler, F. (1828).“Ueber künstliche Bildung des Harnstoffs”.Annalen der Physik und Chemie.88(2): 253–256.Bibcode:1828AnP....88..253W.doi:10.1002/andp.18280880206.ISSN0003-3804.
- ^Kauffman(2001), pp. 121–133.
- ^Lipman, Timothy O. (tháng 8 năm 1964).“Wohler's preparation of urea and the fate of vitalism”.Journal of Chemical Education.41(8): 452.Bibcode:1964JChEd..41..452L.doi:10.1021/ed041p452.ISSN0021-9584.
- ^Tropp(2012), tr. 19–20.
- ^Krebs(2012), tr. 32.
- ^Butler(2009), tr. 5.
- ^Chandan(2007), tr. 193–194.
- ^Cox, Nelson, Lehninger (2008).Lehninger Principles of Biochemistry.Macmillan.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- ^Nielsen(1999), pp. 283–303.
- ^Slabaugh(2007), pp. 3–6.
- ^Whiting(1970), pp. 1–31.
- ^Voet(2005), pp. 358–359.
- ^Stryer(2007), p. 328.
- ^Voet(2005), Ch. 12 Lipids and Membranes.
- ^Metzler(2001), tr. 58.
Sách tham khảo
[sửa|sửa mã nguồn]- Amsler, Mark (1986).The Languages of Creativity: Models, Problem-solving, Discourse.University of Delaware Press.ISBN978-0874132809.
- Astbury, W.T. (1961).“Molecular Biology or Ultrastructural Biology?”(PDF).Nature.190(4781): 1124.doi:10.1038/1901124a0.PMID13684868.Truy cập ngày 4 tháng 1 năm 2016.
- Ben-Menahem, Ari (2009).Historical Encyclopedia of Natural and Mathematical Sciences.Springer. tr. 2982.ISBN978-3-540-68831-0.
- Burton, Feldman (2001).The Nobel Prize: A History of Genius, Controversy, and Prestige.Arcade Publishing.ISBN978-1559705929.
- Butler, John M. (2009).Fundamentals of Forensic DNA Typing.Academic Press.ISBN978-0-08-096176-7.
- Chandan, Sen K.; Sashwati Roy (2007). “miRNA: Licensed to kill the messenger”.DNA Cell Biology.26(4).doi:10.1089/dna.2006.0567.PMID17465885.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- Clarence, Peter Berg (1980).“The University of Iowa and Biochemistry from Their Beginnings”.ISBN9780874140149.Chú thích journal cần
|journal=(trợ giúp) - Edwards K.J., Brown D.G., Spink, N., Skelly J.V., Neidle S. (1992).“Molecular structure of the B-DNA dodecamer d(CGCAAATTTGCG)2. An examination of propeller twist and minor-groove water structure at 2.2 A resolution”.J.Mol.Biol.226:1161–1173.PMID1518049.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- Eldra P. Solomon, Linda R. Berg, Diana W. Martin (2007).Biology, 8th Edition, International Student Edition.Thomson Brooks/Cole.ISBN978-0495317142.Bản gốclưu trữ ngày 4 tháng 3 năm 2016.Truy cập ngày 17 tháng 5 năm 2016.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- Fariselli, Piero; Rossi, Ivan; Capriotti, Emidio; Casadio, Rita (2007).“The WWWH of remote homolog detection: the state of the art”.Briefings in Bioinformatics.8(2).doi:10.1093/bib/bbl032.PMID17003074.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)

- Fiske, John (1890).Outlines of Cosmic Philosophy Based on the Doctrines of Evolution, with Criticisms on the Positive Philosophy, Volume 1.Boston and New York: Houghton, Mifflin.Truy cập ngày 16 tháng 2 năm 2015.
- Finkel, Richard; Cubeddu, Luigi; Clark, Michelle (2009).Lippencott's Illustrated Reviews: Pharmacology(ấn bản 4). Lippencott Williams & Wilkins.ISBN978-0-7817-7155-9.
- Krebs, Jocelyn E.; Goldstein, Elliott S.; Lewin, Benjamin; Kilpatrick, Stephen T. (2012).Essential Genes.Jones & Bartlett Publishers.ISBN978-1-4496-1265-8.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- Fromm, Herbert J.; Hargrove, Mark (2012).Essentials of Biochemistry.Springer.ISBN978-3-642-19623-2.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- Hamblin, Jacob Darwin (2005).Science in the Early Twentieth Century: An Encyclopedia.ABC-CLIO.ISBN978-1-85109-665-7.
- Helvoort, Ton van (2000). Arne Hessenbruch (biên tập).Reader's Guide to the History of Science.Fitzroy Dearborn Publishing.ISBN188496429X.
- Holmes, Frederic Lawrence (1987).Lavoisier and the Chemistry of Life: An Exploration of Scientific Creativity.University of Wisconsin Press.ISBN978-0299099848.
- Horton, Derek biên tập (ngày 28 tháng 11 năm 2013).Advances in Carbohydrate Chemistry and Biochemistry, Volume 70.Academic Press.ASINB00H7E78BG.
- Hunter, Graeme K. (2000).Vital Forces: The Discovery of the Molecular Basis of Life.Academic Press.ISBN978-0-12-361811-5.
- Karp, Gerald (ngày 19 tháng 10 năm 2009).Cell and Molecular Biology: Concepts and Experiments.John Wiley & Sons.ISBN9780470483374.
- Kauffman, G.B.; Chooljian, S.H. (2001).“Friedrich Wöhler (1800–1882), on the bicentennial of his birth”.The Chemical Educator.6(2).doi:10.1007/s00897010444a.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- Kleinkauf, Horst; Döhren, Hans von; Jaenicke Lothar (1988).The Roots of Modern Biochemistry: Fritz Lippmann's Squiggle and its Consequences.Walter de Gruyter & Co. tr. 116.ISBN9783110852455.Quản lý CS1: sử dụng tham số tác giả (liên kết)
- Knowles JR (1980).“Enzyme-catalyzed phosphoryl transfer reactions”.Annu. Rev. Biochem.49:877–919.doi:10.1146/annurev.bi.49.070180.004305.PMID6250450.
- Metzler, David Everett; Metzler, Carol M. (2001).Biochemistry: The Chemical Reactions of Living Cells.1.Academic Press.ISBN978-0-12-492540-3.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- Miller G; Spoolman Scott (2012).Environmental Science - Biodiversity Is a Crucial Part of the Earth's Natural Capital.Cengage Learning.ISBN1-133-70787-4.Truy cập ngày 4 tháng 1 năm 2016.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- Nielsen, Forrest H. (1999).Ultratrace minerals; Modern nutrition in health and disease.Baltimore: Williams & Wilkins. tr. 283–303.
- Peet, Alisa (2012). Marks, Allan; Lieberman Michael A. (biên tập).Marks' Basic Medical Biochemistry (Lieberman, Marks's Basic Medical Biochemistry)(ấn bản 4).ISBN160831572X.Quản lý CS1: nhiều tên: danh sách biên tập viên (liên kết)
- Rayner-Canham, Marelene F.; Rayner-Canham, Marelene; Rayner-Canham, Geoffrey (2005).Women in Chemistry: Their Changing Roles from Alchemical Times to the Mid-Twentieth Century.Chemical Heritage Foundation.ISBN978-0941901277.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- Rojas-Ruiz, Fernando A; Vargas-Méndez, Leonor; Kouznetsov, Vladimir V (2011).“Challenges and Perspectives of Chemical Biology, a Successful Multidisciplinary Field of Natural Sciences”.Molecules.16:2672–2687.doi:10.3390/molecules16032672.ISSN1420-3049.Bản gốclưu trữ ngày 5 tháng 12 năm 2015.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- Saenger, Wolfram (1984).Principles of Nucleic Acid Structure.New York: Springer-Verlag.ISBN0-387-90762-9.
- Slabaugh, Michael R., and Seager, Spencer L. (2013).Organic and Biochemistry for Today(ấn bản 6). Pacific Grove: Brooks Cole.ISBN1133605141.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- Sherwood, Lauralee; Klandorf, Hillar; Yancey, Paul H. (2012).Animal Physiology: From Genes to Organisms.Cengage Learning.ISBN978-0-8400-6865-1.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- Stryer L, Berg JM, Tymoczko JL (2007).Biochemistry(ấn bản 6). San Francisco: W.H. Freeman.ISBN978-0-7167-8724-2.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- Tropp, Burton E. (2012).Molecular Biology(ấn bản 4). Jones & Bartlett Learning.ISBN978-1-4496-0091-4.
- UNICEF (2010).Facts for life(PDF)(ấn bản 4). New York: United Nations Children's Fund.ISBN978-92-806-4466-1.Bản gốc(PDF)lưu trữ ngày 12 tháng 12 năm 2018.Truy cập ngày 17 tháng 5 năm 2016.
- Ulveling, Damien; Francastel, Claire; Hubé, Florent (2011).“When one is better than two: RNA with dual functions”.Biochimie.93(4).doi:10.1016/j.biochi.2010.11.004.PMID21111023.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- Varki A, Cummings R, Esko J, Jessica Freeze, Hart G, Marth J (1999).Essentials of glycobiology.Essentials of glycobiology.Cold Spring Harbor Laboratory Press.ISBN0-87969-560-9.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- Voet, D. and Voet, J, G. (2005).Biochemistry(ấn bản 3). Hoboken, NJ: John Wiley & Sons Inc.ISBN9780471193500.Bản gốclưu trữ ngày 4 tháng 2 năm 2016.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
- Whiting, G.C (1970). “Sugars”. Trong A.C. Hulme (biên tập).The Biochemistry of Fruits and their Products.1.London & New York: Academic Press.ISBN0123612012.
- Ziesak, Anne-Katrin; Cram Hans-Robert (ngày 18 tháng 10 năm 1999).Walter de Gruyter Publishers, 1749-1999.Walter de Gruyter & Co.ISBN978-3110167412.Quản lý CS1: nhiều tên: danh sách tác giả (liên kết)
Đọc thêm
[sửa|sửa mã nguồn]- Keith Roberts, Martin Raff, Bruce Alberts, Peter Walter, Julian Lewis and Alexander Johnson,Molecular Biology of the Cell
- 4th Edition, Routledge, March, 2002, hardcover, 1616 pages, 7.6 pounds,ISBN 0-8153-3218-1
- 3rd Edition, Garland, 1994,ISBN 0-8153-1620-8
- 2nd Edition, Garland, 1989,ISBN 0-8240-3695-6
- Fruton, Joseph S.Proteins, Enzymes, Genes: The Interplay of Chemistry and Biology.Yale University Press: New Haven, 1999.ISBN 0-300-07608-8
- Kohler, Robert.From Medical Chemistry to Biochemistry: The Making of a Biomedical Discipline.Cambridge University Press, 1982.
Liên kết ngoài
[sửa|sửa mã nguồn]| Wikibookscó thêm thông tin về Hóa sinh |
| Wikimedia Commons có thêm hình ảnh và phương tiện truyền tải vềHóa sinh. |
- “Biochemical Society”.Bản gốclưu trữ ngày 22 tháng 5 năm 2016.Truy cập ngày 17 tháng 5 năm 2016.
- The Virtual Library of Biochemistry and Cell Biology
- Biochemistry, 5th ed.Full text of Berg, Tymoczko, and Stryer, courtesy ofNCBI.
- SystemsX.ch - The Swiss Initiative in Systems Biology
- Full text of Biochemistryby Kevin and Indira, an introductory biochemistry textbook.
