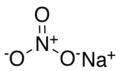Natri nitrat
| Natri nitrat | |||
|---|---|---|---|
| |||
| Danh pháp IUPAC | Natri nitrat | ||
| Tên khác | Caliche Diêm tiêu Chile Nitrat soda Nitratine Diêm tiêu Peru Soda niter cubic niter | ||
| Nhận dạng | |||
| Số CAS | |||
| PubChem | |||
| Số RTECS | WC5600000 | ||
| ẢnhJmol-3D | ảnh | ||
| SMILES | đầy đủ
| ||
| InChI | đầy đủ
| ||
| UNII | |||
| Thuộc tính | |||
| Công thức phân tử | NaNO3 | ||
| Khối lượng mol | 84,9932 g/mol | ||
| Bề ngoài | bột trắng hay tinh thể không màu có vị ngọt | ||
| Khối lượng riêng | 2,257 g/cm³, rắn | ||
| Điểm nóng chảy | 308 °C (581 K; 586 °F) | ||
| Điểm sôi | 380 °C (653 K; 716 °F) (phân huỷ) | ||
| Độ hòa tantrong nước | 730 g/L (0°C) 921 g/L (25°C) 1800 g/L (100°C) | ||
| Độ hòa tan | tan rất tốt trongamonia;tan được trongcồn | ||
| Chiết suất(nD) | 1,587 (dạng tam giác) 1,336 (trực thoi) | ||
| Cấu trúc | |||
| Cấu trúc tinh thể | tam giác và trực thoi | ||
| Nhiệt hóa học | |||
| Enthalpy hình thànhΔfH | −468 kJ/mol | ||
| Entropy mol tiêu chuẩnS | 117 J·mol−1 K−1 | ||
| Các nguy hiểm | |||
| MSDS | ICSC 0185 | ||
| Chỉ mục EU | không có trong danh sách | ||
| Nguy hiểm chính | chất oxi hoá, gây kích thích | ||
| NFPA 704 |
| ||
| Điểm bắt lửa | không cháy | ||
| LD50 | 3236 mg/kg | ||
| Các hợp chất liên quan | |||
| Anion khác | Natri nitrit | ||
| Cation khác | Lithi nitrat Kali nitrat Rubidi nitrat Caesi nitrat | ||
| Hợp chất liên quan | Natri sunfat Natri chloride | ||
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trongtrạng thái tiêu chuẩncủa chúng (ở 25 °C [77 °F], 100 kPa). | |||
Natri nitratlà hợp chất hoá học có công thứcNaNO3.Muối này còn được biết đến với cái têndiêm tiêu Chilehaydiêm tiêu Peru(do hai nơi này có lượng trầm tích lớn nhất) để phân biệt vớikali nitrat,là một chất rắn màu trắng tan trongnước.Dạng khoáng vật còn có tên lànitratin,nitratithaysodaniter.
Natri nitrat được dùng như một chất nguyên liệu; trongphân bón,nghề làm pháo hoa, nguyên liệu củabom khói,chất bảo quản,và như mộttên lửa đẩy,cũng nhưthủy tinhvàmen gốm.Hợp chất này đang được khai thác cho các mục đích trên.
Lịch sử
[sửa|sửa mã nguồn]Những chuyến hàng natri nitrat đầu tiên đến châu Âu cập bến ở Anh vào khoảng những năm 1820-1825, nhưng không tìm được khách hàng nào và bị đổ xuống biển để tránh thuế.[1][2]Tuy nhiên, cùng với thời gian, các mỏ muối ở Nam Mỹ đã trở thành một nguồn kinh doanh màu mỡ (năm 1859, cả nước Anh tiêu thụ tổng cộng 47.000 tấn[2]).Chiletiến hành cuộc chiến với liên minhPeruvàBoliviatrong cuộc chiến tranh Thái Bình Dương 1879-1884 và tiếp quản nguồn quặng lớn nhất. Năm 1919,Ralph Walter Graystone Wyckoffkhám phá ra cấu trúc tinh thể của nó nhờ dùng phương pháptinh thể học tia X.
Nguồn tài nguyên
[sửa|sửa mã nguồn]Nguồn natri nitrat tự nhiên lớn nhất được tìm thấy ởChilevàPeru,nơi các muối nitrat kết rắn lại trong các trầm tích gọi là quặngcaliche.[3]Trong hơn một thế kỷ, nguồn cung cấp chủ yếu cho thế giới được khai thác bằng thuốc nổ từhoang mạc Atacamaở bắc Chile cho đến khi, sang thế kỷ 20, hai nhà hoá học người ĐứcFritz HabervàCarl Boschphát triển một quá trình sản xuấtamoniatừ không khí theo quy trình công nghiệp (xemquy trình Haber). Khichiến tranh thế giới thứ nhấtbùng nổ, nước Đức bắt đầu biến đổi amonia từ quy trình này sangdiêm tiêu Chilenhân tạo, rất thiết thực như nguồn nguyên liệu tự nhiên trong việc sản xuấtthuốc súngvà các loại vũ khí khác. Vào thập niên 1940, quá trình chuyển đổi này gây nên một kết quả đầy kịch tính trong nhu cầu natri nitrat trong tự nhiên.
Chile vẫn là nguồn dự trữ caliche lớn nhất, với nhiều mỏ đang hoạt động ở các vùngPedro de Valdivia,María ElenavàPampa Blanca,và ở đó nó thường được mệnh danh làvàng trắng.Natri nitrat,kali nitrat,natri sunfatvàiodvẫn được khai thác bằng quá trình caliche. Cộng đồng dân cư vùng mỏHumberstone và Santa Laurađược tuyên bố làdi sản thế giớivào năm 2005.
Natri nitrat được sản xuất trong công nghiệp bằng phản ứng trung hoàaxit nitricvớinatri cacbonat.
Ứng dụng
[sửa|sửa mã nguồn]Natri nitrat được dùng trong phạm vi rộng như là một loại phân bón và nguyên liệu thô cho quá trình sản xuất thuốc súng vào cuối thế kỷ 19. Nó có thể kết hợp với sắt hydroxide để tạo nhựa thông.
Natri nitrat không nên bị lầm lẫn với hợp chất liên quan,natri nitrit.
Nó có thể dùng trong sản xuấtaxit nitrickhi phản ứng vớiaxit sunfuricrồi tách axit nitric ra thông qua quá trìnhchưng cất phân đoạn,còn lại là bãnatri hydrosunfat.Những người săn vàng dùng natri nitrat để điều chếnước cường toancó thể hoà tan vàng và các kim loại quý khác.
Ứng dụng ít gặp hơn là một chất oxi hoá thay thế trong pháo hoa như là một sự thay thếkali nitratchủ yếu có trongthuốc nổ đenvà như một thành phần cấu tạo trong túi lạnh.[4]
Natri nitrat còn được dùng chung vớikali nitratcho việc bảo quản nhiệt, và gần đây, cho việcchuyển đổi nhiệttrong các thápnăng lượng mặt trời.
Ngoài ra nó còn dùng trong công nghiệp nước thải cho sự hô hấp tuỳ ý của vi sinh vật.Nitrosomonas,một loàivi sinh vật,hấp thụ nitrat thay vì oxi, làm cho loài này có thể phát triển tốt trong nước thải cần xử lý.
Mối quan tâm về sức khoẻ
[sửa|sửa mã nguồn]Giông nhưnatri nitrit,natri nitrat tạonitrosamin,một chất gây ung thư ở người, gây nên sự phá huỷ DNA và làm gia tăng thoái hoá tế bào. Các nghiên cứu đã chỉ ra mối liên quan giữa hàm lượng nitrat và nguy cơ chết do Alzheimer, đái tháo đường, và Parkinson, có thể thông qua ảnh hưởng của nitrosamin lên DNA.[5]Nitrosamin, hình thành từ thịt được xử lý bằng natri nitrat và nitrit, có liên quan đếnung thư dạ dàyvàung thư thực quản.[6]Natri nitrat và nitrit có liên quan đến nguy cơ cao mắc ung thư đại trực tràng.[7]Quỹ Nghiên cứu ung thư Vương quốc Anh[8]tuyên bố rằng một trong những nguyên nhân mà thịt chế biến làm tăng nguy cơung thư ruột kếtlà lượng nitrat chứa trong đó. Một lượng nhỏ nitrat trong thịt như chất bảo quản bị phân tích thành nitrit, thêm vào đó là lượng nitrit có sẵn trong thịt. Nitrit này sau đó phản ứng với các thức ăn giàu protein (như thịt) để tạo ra các hợp chất N-nitroso. Một vài hợp chất này được biết có khả năng gây ung thư. N-nitroso không chỉ hình thành khi thịt được xử lý mà còn khi thịt được tiêu hoá trong cơ thể.
Xem thêm
[sửa|sửa mã nguồn]- Chiến tranh Thái Bình Dương(haychiến tranh diêm tiêu)
Tham khảo
[sửa|sửa mã nguồn]- ^S. H. Baekeland "Några sidor af den kemiska industrien" (1914)Svensk Kemisk Tidskrift,p. 140.
- ^abFriedrich Georg Wieck,Uppfinningarnas bok(1873, Swedish translation ofBuch der Erfindungen),vol. 4, p. 473.
- ^Stephen R. Bown, A Most Damnable Invention: Dynamite, Nitrates, and the Making of the Modern World, Macmillan, 2005,ISBN 0-312-32913-X,p. 157
- ^Albert A. Robbins "Chemical freezing package"Bằng sáng chế Hoa Kỳ số 2.898.744,Issue date: August 1959
- ^[1]
- ^“Nitrosamine and related food intake and gastric and oesophageal cancer risk: a systematic review of the epidemiological evidence”.Bản gốclưu trữ ngày 14 tháng 10 năm 2018.Truy cập 8 tháng 7 năm 2015.
- ^[2]
- ^"Why does processed meat increase bowel cancer risk?"Lưu trữ2010-03-26 tạiWayback Machine,World Cancer Research Fund (2010) accessdate 2010-03-06
Đọc thêm
[sửa|sửa mã nguồn]- Barnum, Dennis (2003).“Some History of Nitrates”.Journal of Chemical Education.80:1393–.doi:10.1021/ed080p1393.
Liên kết ngoài
[sửa|sửa mã nguồn]- ATSDR — Case Studies in Environmental Medicine - Nitrate/Nitrite ToxicityU.S.Department of Health and Human Services(public domain)
- FAO/WHO report