Cellulose
| Cellulose[1] | |
|---|---|
 Cellulose, một polymer tuyến tính của các đơn vị D-glucose (được hiển thị hai đơn vị) liên kết bởi các liên kết β(1→4)-glycosidic | |
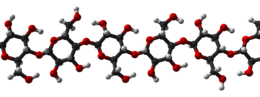 Cấu trúc ba chiều của cellulose | |
| Nhận dạng | |
| Số CAS | |
| PubChem | |
| KEGG | |
| ChEMBL | |
| UNII | |
| Thuộc tính | |
| Công thức phân tử | (C 12H 20O 10) n |
| Khối lượng mol | 162.1406 g/mol cho mỗi đơn vị glucose |
| Bề ngoài | bột trắng |
| Khối lượng riêng | 1.5 g/cm3 |
| Điểm nóng chảy | 260–270 °C; 533–543 K; 500–518 °F Phân hủy[2] |
| Điểm sôi | |
| Độ hòa tantrong nước | không tan |
| Nhiệt hóa học | |
| Enthalpy hình thànhΔfH | −963,000 kJ/mol[cần giải thích] |
| DeltaHc | −2828,000 kJ/mol[cần giải thích] |
| Các nguy hiểm | |
| NFPA 704 |
|
| PEL | TWA 15 mg/m3(tổng) TWA 5 mg/m3(hô hấp)[2] |
| REL | TWA 10 mg/m3(tổng) TWA 5 mg/m3(hô hấp)[2] |
| IDLH | N.D.[2] |
| Các hợp chất liên quan | |
| Hợp chất liên quan | Starch |
Trừ khi có ghi chú khác, dữ liệu được cung cấp cho các vật liệu trongtrạng thái tiêu chuẩncủa chúng (ở 25 °C [77 °F], 100 kPa). | |
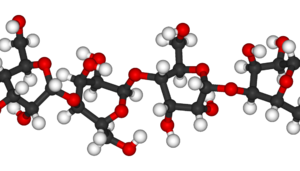
Celluloselà mộthợp chất hữu cơvớicông thức(C6H10O5)nmộtpolysaccharidegồm chuỗi tuyến tính của hàng trăm đến hàng nghìn đơn vịD-glucoseliên kếtβ(1→4)[3][4]Cellulose là thành phần cấu trúc quan trọng củabức bình di chấtchính củathực vật lục,nhiều dạngtảovà cácoomycete.Một số loàivi khuẩntiết ra nó để hình thànhbiofilms.[5]Cellulose làpolymer hữu cơphổ biến nhất trên Trái Đất.[6]Hàm lượng cellulose trong sợibônglà 90%, tronggỗlà 40–50%, và tronggai dầuđã khô là khoảng 57%.[7][8][9]
Cellulose chủ yếu được sử dụng để sản xuất giấy và bìa cứng. Một phần nhỏ được chuyển đổi thành các sản phẩm phái sinh khác nhưcellophanevà tơ tổng hợp. Hiện nay, người ta đang phát triển việc chuyển đổicellulosetừ cây trồng năng lượng thành nhiên liệu sinh học như ethanol từcellulose,để tạo ra một nguồn nhiên liệu tái tạo. Cellulose thường được thu thập từ bột giấy từ gỗ và bông để sử dụng trong công nghiệp.
Một số loài động vật, như động vật nhai lại và mối, có thể tiêu hóacellulosenhờ sự hỗ trợ từ vi sinh vật sống trong ruột của chúng, nhưTrichonympha.Trong dinh dưỡng con người, cellulose là một thành phần không tiêu hóa của chất xơ không hòa tan, có tác dụng làm cho phân người dễ chảy và có thể hỗ trợ quá trình đại tiện.
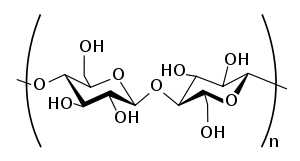
Cellulose do các mắt xích β-D-Glucose liên kết với nhau bằng liên kết 1,4-glycosidedo vậy liên kết này thường không bền trong các phản ứngthủy phân.
Cellulose được tạo thành trong cây xanh nhờ quá trìnhquang hợpcủacây:
6nCO2+5nH2OClorophin,ánh sáng→(C6H10O5)n+6nO2
Phản ứng thủy phân
[sửa|sửa mã nguồn]Đun nóng lâu cellulose với dung dịch acid sulfuric, các liên kết β-glycoside bị đứt tạo thành sản phẩm cuối cùng làglucose:
(C6H10O5)n+ nH2O → nC6H12O6(xúc tác H+,to)
Phản ứng này áp dụng trong sản xuấtalcohol etyliccông nghiệp, xuất phát từ nguyên liệu chứa cellulose (vỏ bào, mùn cưa, tre, nứa, v.v...).
Phản ứng thủy phân cellulose có thể xảy ra nhờ tác dụng xúc tác củaenzymecellulasecó trong cơ thểđộng vật nhai lại(trâu, bò...). Cơ thể người không có enzyme này nên không thể tiêu hóa được cellulose.
Tác dụng với một số tác nhân base
[sửa|sửa mã nguồn]Cho cellulose tác dụng với NaOH người ta thu được sản phẩm gọi là "cellulose kiềm", đem chế hóa tiếp vớicarbon disulfidesẽ thu được dung dịch cellulose xantogenat:
[C6H7O2(OH)3]n(Cellulose) → [C6H7O2(OH)2ONa]n(Cellulose kiềm) → [C6H7O2(OH)2O-CS2Na]n(Cellulose xantogenat)
Cellulose xantogenat tan trong kiềm tại thành dung dịch rất nhớt gọi là visco. Khi bơm dung dịch nhớt này qua những ống có các lỗ rất nhỏ (φ < 0,1mm) ngâm trong dung dịch H2SO4,cellulose xantogenat sẽ bị thủy phân cho ta cellulose hidrat ở dạng óng nuột gọi là tơ visco:
[C6H7O2(OH)2O-CS2Na]n(Cellulose xantogenat) + n/2H2SO4→ [C6H7O2(OH)3]n(Cellulose hydrate) + nCS2+ Na2SO4
Cellulose hydrate có công thức hóa học tương tự cellulose, nhưng do quá trình chế biến hóa học như trên, mạch polymer trở nên ngắn hơn, độ bền hóa học kém đi và háo nước hơn.
- Tác dụng của dung dịch Cu(OH)2trong amonia:
Cellulose tan được trong dung dịch Cu(OH)2trong amonia có tên là "nước Svayde" (Schweitzer's Reagent), trong đó Cu2+tồn tại chủ yếu ở dạng phức chất Cu(NH3)n(OH)2.Khi ấy sinh ra phức chất của cellulose với ion đồng ở dạng dung dịch nhớt. Nếu ta bơm dung dịch nhớt này đi qua ống có những lỗ rất nhỏ ngâm trong nước, phức chất sẽ bị thủy phân thành cellulose hydrate ở dạng sợi, gọi làtơ đồng - amonia.
Phản ứng với một số acid hoặc anhydride acid tạo thành este
[sửa|sửa mã nguồn]- Tác dụng củaHNO3:
Đun nóng cellulose với hỗn hợp HNO3và H2SO4đậm đặc, tùy theo điều kiện phản ứng mà một, hai hay cả ba nhóm -OH trong mỗi mắt xích C6H10O5được thay thế bằng nhóm -ONO2tạo thành các este cellulose nitrat:
[C6H7O2(o...H)3]n+ nHNO3→ [C6H7O2(OH)2ONO2]n(Cellulose mononitrat) + nH2O
[C6H7O2(OH)3]n+ 2nHNO3→ [C6H7O2(OH)(ONO2)2]n(Cellulose dinitrat) + 2nH2O
[C6H7O2(OH)3]n+ 3nHNO3→ [C6H7O2(ONO2)3]n(Cellulose trinitrat) + 3nH2O
Hỗn hợp cellulose mononitrat và cellulose dinitrat (gọi là coloxilin) được dùng để tạo màng mỏng tại chỗ trên da nhằm bảo vệ vết thương, và dùng trong công nghệ cao phân tử (chế tạo nhựa xenluloit, sơn, phim ảnh...). Cellulose trinitrat thu được (có tên gọi piroxilin) là một sản phẩm dễ cháy và nổ mạnh, được dùng làm chất nổ cho mìn, lựu đạn... và chế tạo thuốc súng không khói.
- Tác dụng của (CH3CO)2O: Cellulose tác dụng với anhydride acetic có H2SO4xúc tác có thể tạo thành cellulose mono- hoặc di- hoặc triacetat. Ví dụ:
[C6H7O2(OH)3]n+ 3n(CH3CO)2O → [C6H7O2(OCOCH3)3]n(cellulose triacetat) + 3nCH3COOH
Trong công nghiệp cellulose triacetat và cellulose diacetat được dùng hỗn hợp hoặc riêng rẽ để sản xuất phim ảnh vàtơ acetat.Chẳng hạn hòa tan hai este trên trong hỗn hợpacetonvàethanolrồi bơm dung dịch thu được qua những lỗ nhỏ thành chùm tia đồng thời thổi không khí nóng (55 - 70oC) qua chùm tia đó để làm bay hơi aceton sẽ thu được những sợi mảnh khảnh gọi là tơ acetat. Tơ acetat có tính đàn hồi, bền bỉ và đẹp.
Xem thêm
[sửa|sửa mã nguồn]Tham khảo
[sửa|sửa mã nguồn]- ^Nishiyama, Yoshiharu; Langan, Paul; Chanzy, Henri (2002). “Cấu trúc tinh thể và hệ liên kết hydro trong cellulose Iβ từ tia X và sợi neutron”.J. Am. Chem. Soc.124(31): 9074–9082.doi:10.1021/ja0257319.PMID12149011.
- ^abcd“NIOSH Pocket Guide to Chemical Hazards #0110”.Viện An toàn và Sức khỏe Nghề nghiệp Quốc gia Hoa Kỳ(NIOSH).
- ^Crawford, R. L. (1981).Lignin biodegradation and transformation.New York: John Wiley and Sons.ISBN978-0-471-05743-7.
- ^Updegraff D. M. (1969). “Semimicro determination of cellulose in biological materials”.Analytical Biochemistry.32(3): 420–424.doi:10.1016/S0003-2697(69)80009-6.PMID5361396.
- ^Romeo, Tony (2008).Bacterial biofilms.Berlin: Springer. tr. 258–263.ISBN978-3-540-75418-3.
- ^Klemm, Dieter; Heublein, Brigitte; Fink, Hans-Peter; Bohn, Andreas (2005). “Cellulose: Fascinating Biopolymer and Sustainable Raw Material”.Angew. Chem. Int. Ed.44(22): 3358–3393.doi:10.1002/anie.200460587.PMID15861454.
- ^Cellulose. (2008). InEncyclopædia Britannica.Retrieved January 11, 2008, from Encyclopædia Britannica Online.
- ^Chemical Composition of Wood.Lưu trữ2018-10-13 tạiWayback Machine.ipst.gatech.edu.
- ^Piotrowski, Stephan and Carus, Michael (May 2011)Multi-criteria evaluation of lignocellulosic niche crops for use in biorefinery processesLưu trữ2021-04-03 tạiWayback Machine.nova-Institut GmbH, Hürth, Germany.
Liên kết ngoài
[sửa|sửa mã nguồn]| Wikimedia Commons có thêm hình ảnh và phương tiện truyền tải vềCellulose. |
- Cellulose (plant cell structure)tạiEncyclopædia Britannica(tiếng Anh)
- "Cellulose".Encyclopædia Britannica. Vol. 5 (11th ed.). 1911.
- Structure and morphology of celluloseby Serge Pérez and William Mackie, CERMAV-CNRS
- Cellulose,by Martin Chaplin,London South Bank University
- Clear description of a cellulose assay methodat the Cotton Fiber Biosciences unit of theUSDA.
- Cellulose films could provide flapping wings and cheap artificial muscles for robots– TechnologyReview