- +1
【 tiền duyên tiến triển 】 chuyên gia điểm bình Nat Methods cổn trần linh linh tổ lợi dụng CRISPR-dCas12 hệ thống thật hiện phi trọng phục cơ…
Điểm bình | trần khuông thời ( bắc kinh đại học ), mã hàm tuệ ( thượng hải khoa kỹ đại học )
Hoạt tế bào truy tung DNA, RNA đẳng hạch toan đích không gian phân bố hòa động thái biến hóa đối vu liễu giải cơ nhân biểu đạt điều khống cơ chế cụ hữu thập phân trọng yếu đích ý nghĩa. Lai nguyên vu tế khuẩn hòa cổ tế khuẩn thể nội đích hoạch đắc tính miễn dịch hệ thống CRISPR-Cas hệ thống do vu kỳ đặc dị tính bá hướng DNA/RNA đích năng lực, dĩ bị quảng phiếm khai phát thành đa chủng tế bào nội DNA/RNA đích di truyện thao tác hòa kiểm trắc tiêu ký đích công cụ.
Trung quốc khoa học viện phân tử tế bào khoa học trác việt sang tân trung tâm ( sinh vật hóa học dữ tế bào sinh vật học nghiên cứu sở ) trần linh linh nghiên cứu tổ tiền kỳ cấu kiến liễu cơ vu CRISPR-dCas13 đích RNA tiêu ký hệ thống, tịnh thật hiện liễu hoạt tế bào hòa ban mã ngư phôi thai nội RNA đích thành tượng truy tung dĩ cập hoạt tế bào RNA đa sắc thành tượng (Yang et al., Mol Cell, 2019; Huang et al., Genome Bio, 2023; Yang et al., Cell Insight, 2022). Nhi bá hướng DNA đích CRISPR-Cas9 hệ thống kinh cải tạo hậu khả dụng vu hoạt tế bào DNA thành tượng tiêu ký (Chen et al., Cell, 2013; Ma et al., Nat Biotechnol, 2016). Giá ta CRISPR hệ thống tại tiêu ký nội nguyên hạch toan tự liệt phương diện hiển kỳ xuất kỳ độc đặc đích ưu thế, nhiên nhi đối vu phi trọng phục DNA/RNA tự liệt đích hoạt tế bào đặc dị tính thành tượng mục tiền hoàn tồn tại trứ chư đa hạn chế.
2024 niên 7 nguyệt 4 nhật, trần linh linh nghiên cứu tổ tại Nature Methods thượng phát biểu liễu văn chương CRISPR array-mediated imaging of non-repetitive and multiplex genomic loci in living cells. Cai nghiên cứu đối hiện hữu CRISPR-dCas12a hệ thống tiến hành si tuyển ưu hóa, cấu kiến liễu khả dụng vu phi trọng phục tự liệt DNA hoạt tế bào thành tượng đích CRISPRdelight hệ thống; tiến nhất bộ sử dụng CRISPRdelight hệ thống, yết kỳ liễu cơ nhân vị điểm tại tế bào hạch nội định vị dữ kỳ vận động năng lực hòa chuyển lục hoạt tính đích tương quan tính; đồng thời lợi dụng RNA thích phối thể tu sức đích CRISPR xuyến liên tự liệt thật hiện liễu đối 4 chủng vệ tinh DNA đích hoạt tế bào đa sắc thành tượng.

CRISPR-Cas12a hệ thống chúc vu loại hình V đích CRISPR-Cas gia tộc, tại bá hướng DNA đích đồng thời hoàn cụ bị tương CRISPR xuyến liên tự liệt gia công thành đa điều thành thục crRNA đích năng lực ( Zetsche, B. et al., Cell, 2015 ). Nhân thử CRISPR-Cas12a hệ thống lý luận thượng khả dĩ thông quá CRISPR xuyến liên tự liệt tại đồng nhất tế bào nội biểu đạt túc cú sổ lượng crRNA tòng nhi thật hiện phi trọng phục tự liệt DNA đích tiêu ký.
Vi liễu nghiệm chứng giá nhất sai tưởng, nghiên cứu nhân viên tuyển thủ liễu dĩ báo đạo năng hiển trứ đề cao cơ nhân biên tập hiệu suất đích tam chủng dLbCas12a đột biến thể, tịnh đối tha môn tiêu ký vi vệ tinh DNA Sat I hòa Sat III năng lực tiến hành liễu bỉ giác, phát hiện hyperdLbCas12a đột biến thể ( D156R, D235R, D292R, D350R ) khả dĩ thật hiện canh cao đích tiêu ký hiệu suất hòa tín hào chất lượng. Nghiên cứu nhân viên tiến nhất bộ phát hiện hyperdLbCas12a khả dĩ gia công CRISPR xuyến liên tự liệt tịnh duy trì dữ trực tiếp biểu đạt thành thục crRNA cận tự đích DNA tiêu ký năng lực, đồng thời si tuyển xuất liễu năng cú biểu đạt trường đạt 50 thứ crRNA trọng phục tự liệt đích CAG khải động tử, tịnh cơ vu thử kiến lập liễu dụng vu hoạt tế bào DNA thành tượng đích CRISPRdelight hệ thống.
Nghiên cứu nhân viên châm đối CCAT1 chuyển lục khởi thủy vị điểm thượng du 10kb đích khu vực thiết kế liễu 48 điều gRNA, sử dụng CRISPRdelight hệ thống thành công thật hiện liễu CCAT1 cơ nhân vị điểm đích hoạt tế bào tiêu ký. Dĩ đồng dạng đích phương thức, CRISPRdelight hệ thống tại kỳ tha 6 cá phi trọng phục tự liệt cơ nhân vị điểm quân đắc đáo liễu hữu hiệu nghiệm chứng, tịnh thả cai hệ thống tại HCT116, U2OS dĩ cập tiểu thử phôi thai càn tế bào ( R1 ) trung đồng dạng hữu hiệu. CRISPRdelight hệ thống tương giác vu chi tiền báo đạo đích cơ vu CRISPR-dCas9 đích CARGO hoạt tế bào tiêu ký hệ thống ( Gu, B. et al., Science, 2018 ), cụ hữu chất lạp cấu kiến thành bổn đê, chu kỳ đoản, khả biểu đạt gRNA sổ lượng đa, tiêu ký hệ thống tổ thành canh giản khiết đẳng đa phương diện ưu điểm.
Nghiên cứu nhân viên lợi dụng CRISPRdelight hệ thống tiến nhất bộ phân tích liễu CCAT1 tại tế bào hạch nội đích phân bố đặc điểm hòa vận động đặc chinh, phát hiện vị vu tế bào hạch mô xử Lamin đản bạch tằng đích CCAT1 vị điểm vận động năng lực minh hiển nhược vu vị vu tế bào hạch nội đích CCAT1 vị điểm, tiến nhất bộ kiểm trắc CCAT1 đích nội hàm tử biểu đạt tín hào phát hiện Lamin đản bạch tằng đích CCAT1 vị điểm chuyển lục hoạt tính dã canh nhược. Đồng thời nghiên cứu nhân viên đối HSPH1, HSPA1A đẳng nhiệt hưu khắc cơ nhân tiến hành liễu tiêu ký, tại hướng tế bào thi gia 42°C hoặc á thân toan nột thứ kích hậu, phát hiện định vị vu hạch ban đích HSPH1 cơ nhân vị điểm hội minh hiển tăng đa, tịnh thả vị vu hạch ban đích cơ nhân vị điểm chuyển lục hoạt tính dã minh hiển canh cường. Giá ta kết quả biểu minh liễu cơ nhân tổ DNA đích tế bào hạch nội không gian vị trí dữ kỳ vận động năng lực hòa biểu đạt hoạt tính đích tương quan tính.
Tối hậu, nghiên cứu nhân viên thông quá RNA kết cấu ưu hóa, thành công tương BoxB, Pepper, PP7 hòa MS2 đẳng RNA thích phối tử nguyên kiện sáp nhập chí gRNA trung, lợi dụng CRISPRdelight hệ thống hòa giá ta nguyên kiện đối ứng đích dung hợp huỳnh quang đản bạch, thật hiện liễu vi vệ tinh DNA Sat I, Sat II, Sat III hòa Sat α đích hoạt tế bào tứ sắc tiêu ký ( đồ 1 ). CRISPRdelight hệ thống vi nghiên cứu hoạt tế bào trung DNA vị điểm đích không gian vị trí hòa động lực học đặc chinh, đề cung liễu canh giản đan hòa tiện lợi đích tân thủ đoạn.
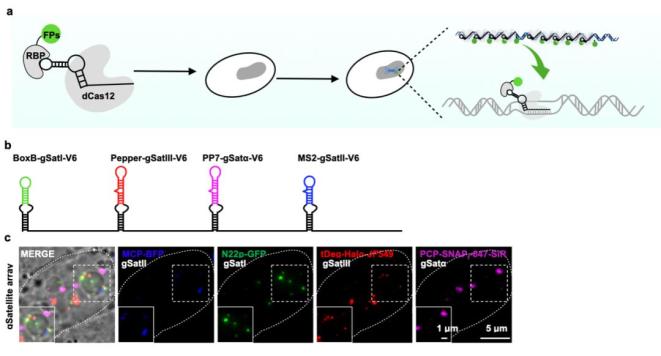
Đồ 1. Sử dụng CRISPRdelight đồng thời tiêu ký đa cá cơ nhân tổ DNA vị điểm
Cai nghiên cứu công tác chủ yếu do phân tử tế bào trác việt trung tâm trần linh linh tổ dương lương trung bác sĩ ( dĩ tất nghiệp ), mẫn dật huy thạc sĩ, lưu dục hân bác sĩ sinh cộng đồng hoàn thành, trần linh linh nghiên cứu viên vi cai luận văn đích thông tấn tác giả. Cai hạng công tác đắc đáo hoắc hoa đức hưu tư y học nghiên cứu sở Zhe (James) Liu giáo thụ, phục đán đại học sinh vật y học nghiên cứu viện / phục đán đại học phụ chúc nhi khoa y viện dương lực nghiên cứu viên, thanh hoa đại học vương hải phong bác sĩ đích đại lực chi trì.
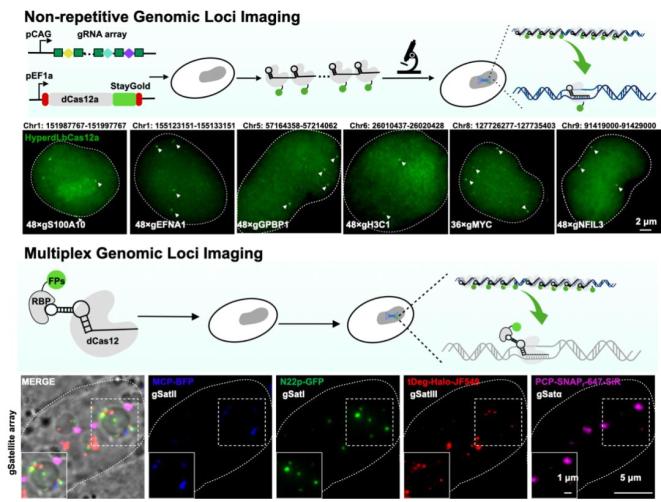
Graphical Abstract
Chuyên gia điểm bình
Trần khuông thời ( bắc kinh đại học, nghiên cứu viên )
CRISPR/dCas9 thành tượng hệ thống đích phát triển sử đắc đối nhậm ý nhiễm sắc chất vị điểm tiến hành thành tượng thành vi khả năng. Cai hệ thống lợi dụng thất khứ thiết cát hoạt tính đích Cas9 đản bạch đột biến thể ( dCas9 ), thông quá đối dCas9 tiến hành huỳnh quang tiêu ký, hoặc giả cải tạo single guide RNA (sgRNA) ( như sáp nhập MS2, pepper đẳng thích phối thể ) sử kỳ năng cú bị huỳnh quang tiêu ký, tòng nhi thật hiện đối mục tiêu nhiễm sắc chất vị điểm đích thành tượng. Tẫn quản CRISPR/dCas9 thể hệ thị mục tiền tối quảng phiếm ứng dụng vu hoạt tế bào cơ nhân tổ thành tượng đích hệ thống, đãn kỳ tại đa trọng kiểm trắc ( multiplexing, tức lợi dụng bá hướng bất đồng tự liệt đích đa cá sgRNA tiêu ký đồng nhất cá cơ nhân vị điểm hoặc đa cá cơ nhân vị điểm ) phương diện tồn tại nhất định đích cục hạn tính. Cụ thể lai thuyết, lợi dụng CRISPR/dCas9 tiến hành đa trọng kiểm trắc thông thường nhu yếu cấu kiến đa cá đái hữu bất đồng sgRNA đích chất lạp hoặc mạn bệnh độc lai thật hiện đa chủng sgRNA tại đồng nhất cá tế bào trung đích đồng thời chuyển lục. Nhiên nhi, giá loại phương pháp khả năng đạo trí bất đồng tế bào trung sgRNA sổ lượng hòa chủng loại đích cá thể soa dị, tòng nhi ảnh hưởng đối mục tiêu cơ nhân tổ tại đa cá tế bào trung đích cao hiệu kiểm trắc. Tiến nhất bộ nghiên cứu hiển kỳ, thông quá đan nhất chất lạp chuyển lục đa cá sgRNA đích phương pháp, như CARGO thể hệ, khả dĩ khắc phục giá nhất vấn đề. Nhiên nhi, giá loại phương pháp nhu yếu tương đa cá sgRNA biểu đạt nguyên kiện ( như U6-sgRNA chuyển lục đan nguyên ) dẫn nhập đồng nhất cá chất lạp trung, hợp thành bộ sậu phục tạp thả hiệu suất đê. Thử ngoại, đa cá khải động tử đích đồng thời tồn tại hoàn khả năng sử đắc mỗi cá sgRNA đích chuyển lục tương hỗ cạnh tranh, đạo trí đa cá bá hướng đích sgRNA vô pháp đồng thời tồn tại, tiến nhi ảnh hưởng mục tiêu cơ nhân vị điểm đích cao hiệu tiêu ký.
Vi liễu phát triển canh thích dụng vu đa trọng kiểm trắc đích hoạt tế bào cơ nhân tổ thành tượng công cụ, trần linh linh khóa đề tổ cơ vu lai nguyên vu CRISPR hệ thống V hình đích CRISPR-Cas12a (Cpf1) thể hệ, phát triển liễu nhất chủng danh vi CRISPRdelight đích tân hình tiêu ký kỹ thuật. Dữ CRISPR-Cas9 bất đồng, CRISPR-Cas12a cụ bị gia công tự thân CRISPR RNA (crRNA) đích năng lực, nhi giá nhất năng lực tại khứ trừ CRISPR-Cas12a đích DNA thiết cát hoạt tính hậu nhưng nhiên đắc dĩ bảo lưu. Khóa đề tổ dĩ hyperdLbCas12a giá nhất biến thể tác vi CRISPR-delight đích hiệu ứng đản bạch, tịnh cấu kiến đái hữu đa cá năng dữ hyperdLbCas12a kết hợp đích crRNA đích đan nhất trận liệt RNA, chứng thật liễu huỳnh quang tiêu ký đích hyperdLbCas12a tại đan cơ nhân vị điểm đích kiểm trắc linh mẫn độ hòa tiêu ký hiệu suất phương diện, tương giác vu cơ vu CRISPR-dCas9 đích CARGO thành tượng thể hệ canh cụ ưu thế. Thử ngoại, trừ liễu đối hyperdLbCas12a tiến hành huỳnh quang tiêu ký, khóa đề tổ hoàn chứng thật liễu khả dĩ thông quá cải tạo crRNA, sử kỳ hàm hữu bất đồng chủng loại đích thích phối thể ( bao quát MS2, PP7, Pepper hòa BoxB ) tòng nhi thật hiện tứ sắc thành tượng.
Tổng thể lai thuyết, CRISPRdelight kỹ thuật bất cận cụ bị ngận cao đích thác triển tính, tại đa trọng kiểm trắc phương diện dã bỉ cơ vu CRISPR/dCas9 đích thể hệ canh hữu ưu thế. Thông quá tiến nhất bộ ưu hóa CRISPRdelight kỹ thuật trung đích huỳnh quang đoàn tuyển trạch, crRNA kết cấu dĩ cập Cas12a đích thoát bá hiệu ứng đẳng phương diện, hữu vọng sử kỳ thành vi thôi động tam duy cơ nhân tổ học, tế bào sinh vật học đẳng nghiên cứu lĩnh vực phát triển đích trọng yếu công cụ.
Chuyên gia điểm bình
Mã hàm tuệ ( thượng hải khoa kỹ đại học, nghiên cứu viên )
Nhân loại cơ nhân tổ trung hàm hữu 2 vạn đa cá biên mã cơ nhân dĩ cập đại lượng đích phi biên mã cơ nhân hòa điều khống nguyên kiện. Cơ nhân tổ DNA đích tam duy kết cấu dữ động thái biến hóa tại cơ nhân chuyển lục điều khống, tế bào phân hóa, cá thể phát dục dĩ cập tật bệnh phát sinh quá trình trung chí quan trọng yếu. Dụng vu nghiên cứu cơ nhân tổ DNA tam duy kết cấu đích phương pháp chúng đa, bỉ như cơ vu cao thông lượng DNA trắc tự đích Hi-C, cơ vu siêu phân biện suất hiển vi kính đích MERFISH đẳng, mục tiền dĩ kinh tích luy liễu đại lượng đích sổ cư dụng vu phân tích hòa tham tác cơ nhân tổ DNA tam duy kết cấu dữ công năng đích quan hệ. Đãn cơ nhân tổ DNA tại hoạt tế bào trung động thái biến hóa cập kỳ công năng nghiên cứu nghiêm trọng trệ hậu, chủ yếu nguyên nhân thị khuyết phạp nhất cá cao hiệu, thật thời thành tượng phi trọng phục tự liệt DNA ( bao quát cơ nhân hoặc cơ nhân đích điều khống nguyên kiện ) đích công cụ. Mỹ quốc quốc lập vệ sinh nghiên cứu viện tư trợ đích 4D hạch thể kế hoa II kỳ ( 4D Nucleome Program ) bả cơ nhân tổ thật thời động thái biến hóa hòa công năng tác vi nhu yếu đột phá đích trọng điểm nội dung chi nhất.
Cơ vu CRISPR đích hoạt tế bào DNA thành tượng kỹ thuật khả dĩ hữu hiệu địa kỳ tung cơ nhân tổ trung trọng phục tự liệt đích động thái biến hóa, đãn thị thật thời thành tượng phi trọng phục tự liệt DNA nhưng phi thường khốn nan, chủ yếu đích bình cảnh tại vu kỳ tín táo bỉ ( Signal-to-Noise Ratio ) đê, á tế bào định vị hòa trường thời gian kỳ tung đô phi thường cụ hữu thiêu chiến tính. Nhân thử giá nhất lĩnh vực nghiên cứu nhân viên nhất trực trí lực vu như hà đề cao tín hào hòa hàng đê táo âm, kỳ đãi thật hiện cao hiệu, thật thời thành tượng cơ nhân tổ DNA cập kỳ tại cơ nhân điều khống quá trình trung đích động thái biến hóa. Trung quốc khoa học viện phân tử tế bào khoa học trác việt trung tâm đích trần linh linh khóa đề tổ hòa kỳ hợp tác giả cận kỳ khai phát đích CRISPRdelight, xảo diệu địa giải quyết đích giá nhất nan đề.
Đề cao tín hào đích phương pháp chủ yếu thông quá tăng gia đặc định khu vực nội bá hướng vị điểm đích sổ lượng ( tiling array of gRNAs ) bỉ như CARGO hệ thống, hoặc đối đan cá bá hướng vị điểm đích tín hào phóng đại bỉ như Casilio hoặc CRISPR FISHer. Giá ta hệ thống đô thị cơ vu CRISPR-dCas9, kỳ trung CARGO hệ thống nhu yếu chí thiếu 12 cá sgRNAs đích trận liệt, mỗi cá sgRNA nhu yếu đan độc U6 khải động tử khống chế chuyển lục, tối hậu tổ trang tại nhất cá chất lạp tái thể lí, đạo trí chế bị quá trình phục tạp, nhi mỗi cá sgRNA biểu đạt lượng đích quân nhất độ dã một pháp bảo chứng. CRISPRdelight thị cơ vu CRISPR-dCas12a, sung phân lợi dụng liễu Cas12a khả dĩ xử lý lai tự CRISPR trận liệt trung đan cá chuyển lục bổn đích đa cá sgRNAs, giản hóa liễu sgRNA trận liệt đích chế bị quá trình, bảo chứng liễu sgRNA trận liệt đích quân nhất tính, cực đại địa đề cao liễu cơ vu CRISPR DNA thành tượng đích hiệu suất hòa linh mẫn độ.
Cơ nhân tại tế bào hạch nội đích định vị hòa động thái biến hóa dữ cơ nhân chuyển lục hoạt tính hòa chuyển lục hậu gia công đích quan hệ nhất trực bội sổ quan chú. Hạch ban ( Nuclear speckles ) hòa cơ nhân hoạt tính hữu quan, phú hàm đại lượng RNA tiễn tiếp nhân tử, bị nhận vi tham dữ tiễn tiếp công năng dữ điều khống. Thông quá CRISPRdelight hệ thống phát hiện hữu nội hàm tử đích cơ nhân tại cơ nhân kích hoạt đích thời hầu hội trọng định vị đáo hạch ban biểu diện, vi cơ nhân chuyển lục dữ RNA tiễn tập đích ngẫu liên cơ chế đề cung liễu tân đích chứng cư, ám kỳ trứ thông quá DNA đích trọng định vị sử tân sinh pre-mRNA bị vận tống ( sorting ) đáo tiễn thiết cơ khí phú tập đích hạch ban tiến hành chuyển lục hậu gia công.
Thông quá dữ RNA thích phối thể ( RNA aptamers ) kết hợp, CRISPRdelight hoàn khả dĩ thành vi đa sắc hệ thống dụng vu đồng thời quan sát đa cá DNA vị điểm, vi tiến nhất bộ nghiên cứu DNA hoàn tương hỗ tác dụng ( DNA loop interactions ) bỉ như tăng cường tử - khải động tử, tăng cường tử - tăng cường tử, khải động tử - khải động tử, khải động tử - chung chỉ tử đẳng tương hỗ tác dụng cập kỳ công năng điện định liễu lương hảo đích cơ sở. Tiến nhất bộ điệt đại CRISPRdelight đa sắc hệ thống, tương lai dã khả dĩ tại hoạt tế bào trung kỳ tung hoàn tễ áp ( loop extrusion ) quá trình. Giám vu kỳ quảng phiếm đích ứng dụng tiền cảnh, CRISPRdelight hệ thống tương thành vi thôi động tam duy cơ nhân tổ học đáo tứ duy cơ nhân tổ học ( thời gian vi đệ tứ duy độ ) đích hữu lực công cụ chi nhất.
Nguyên văn liên tiếp:
https://www.nature.com/articles/s41592-024-02333-3
Nguyên tiêu đề: 《【 tiền duyên tiến triển 】 chuyên gia điểm bình Nat Methods cổn trần linh linh tổ lợi dụng CRISPR-dCas12 hệ thống thật hiện phi trọng phục cơ nhân tổ vị điểm hòa cơ nhân tổ vị điểm đa sắc tiêu ký 》
Bổn văn vi bành phái hào tác giả hoặc cơ cấu tại bành phái tân văn thượng truyện tịnh phát bố, cận đại biểu cai tác giả hoặc cơ cấu quan điểm, bất đại biểu bành phái tân văn đích quan điểm hoặc lập tràng, bành phái tân văn cận đề cung tín tức phát bố bình đài. Thân thỉnh bành phái hào thỉnh dụng điện não phóng vấn http://renzheng.thepaper.cn.





Tảo mã hạ táiBành phái tân văn khách hộ đoan
- Bành phái tân văn vi bác
- Bành phái tân văn công chúng hào

- Bành phái tân văn đẩu âm hào
- IP SHANGHAI
- SIXTH TONE
- Báo liêu nhiệt tuyến: 021-962866
- Báo liêu bưu tương: [email protected]
Hỗ công võng an bị 31010602000299 hào
Hỗ liên võng tân văn tín tức phục vụ hứa khả chứng: 31120170006
Tăng trị điện tín nghiệp vụ kinh doanh hứa khả chứng: Hỗ B2-2017116
© 2014-2024Thượng hải đông phương báo nghiệp hữu hạn công tư


