Kim chúc đản bạch

Kim chúc đản bạch( anh ngữ:Metalloprotein) thị nhất loại hàm hữuPhối vịKết hợp đíchKim chúcLy tửTác viPhụ nhân tửĐíchĐản bạch chất[1][2].Sở hữu đản bạch chất trung hữu đại lượng thị chúc vu giá nhất loại. Lệ như, tẫn quản khả năng hữu đa đạt 3000 chủng nhân loại đích tử kim chúc đản bạch chất[3] , đãn chí thiếu hữu 1000 chủng nhân loại đản bạch chất ( tổng sổ ước 20,000 chủng ) hàm hữu tử kết hợp đíchĐản bạch chất kết cấu vực[4].
Phong độ
[Biên tập]Cư cổ kế, sở hữu đản bạch chất trung hữu đại ước nhất bán hàm hữu kim chúc[5].Cư lánh nhất cá cổ kế, đại ước tứ phân chi nhất đáo tam phân chi nhất đích sở hữu đản bạch chất bị đề nghị yếu cầu hữu kim chúc chấp hành kỳ công năng[6].Nhân thử, kim chúc đản bạch tạiTế bàoTrung cụ hữu hứa đa chủng bất đồng đích công năng, lệ như đản bạch chất đích trữ tồn hòa vận thâu,MôiHòaTín hào chuyển đạoĐản bạch. Kim chúc ly tử tại cảm nhiễm tính tật bệnh trung đích tác dụng dĩ kinh bị thẩm tra[7].Kim chúc kết hợp đản bạch đích phong độ khả năng thị đản bạch chất sử dụng đích an cơ toan sở cố hữu đích, nhân vi tức sử một hữu tiến hóa sử đích nhân công đản bạch chất dã ngận dung dịch kết hợp kim chúc[8].
Nhân thểTrung đích đại đa sổ kim chúc đô dữ đản bạch chất kết hợp. Lệ như, nhân thể trungThiếtĐích tương đối giác cao nùng độ chủ yếu quy nhân vuHuyết hồng đản bạchTrung đích thiết.
| Can tạng | Thận tạng | Phế tạng | Tâm tạng | Đại não | Cơ nhục | |
|---|---|---|---|---|---|---|
| Mn (Mạnh) | 138 | 79 | 29 | 27 | 22 | <4-40 |
| Fe (Thiết) | 16,769 | 7,168 | 24,967 | 5530 | 4100 | 3,500 |
| Co (Cỗ) | <2-13 | <2 | <2-8 | --- | <2 | 150 (?) |
| Ni (Niết) | <5 | <5-12 | <5 | <5 | <5 | <15 |
| Cu (Đồng) | 882 | 379 | 220 | 350 | 401 | 85-305 |
| Zn (Tử) | 5,543 | 5,018 | 1,470 | 2,772 | 915 | 4,688 |
Phối vị hóa học nguyên lý
[Biên tập]Kim chúc đản bạch trung đích kim chúc ly tử nhất bàn thị dữ đa thái liên thượngAn cơ toanTàn cơ trung đíchĐạm,DưỡngHoặcLưuNguyên tử hoặc dữ đản bạch chất tương kết hợp đích đại hoàn phối thể tương phối vị. Do vu kim chúc ly tử đích đặc thùDưỡng hóa hoàn nguyênTính chất, kim chúc môi thường dụng tác thôi hóa sinh dưỡng hóa hoàn nguyên phản ứng đích thôi hóa tề.
Trừ liễu do an cơ toan tàn cơ đề cung đích cung thể cơ đoàn ngoại, hứa đa hữu cơPhụ nhân tửHoàn khởi phối thể đích tác dụng. Dã hứa tối trứ danh đích thị tịnh nhậpHuyết cơ chấtĐản bạch trung đích tứ xỉ N4Đại hoànPhối thể.Vô cơ phối thể như lưu hóa vật hòa dưỡng hóa vật dã thị thường kiến đích.
Tồn trữ dữ vận thâu tương quan đích kim chúc đản bạch
[Biên tập]Dưỡng tái thể
[Biên tập]Tác vi nhân loại chủ yếu dưỡng tái thể đíchHuyết hồng đản bạchCụ hữu tứ cá á cơ, kỳ trungThiết( II ) ly tử do bình diện đại hoàn phối thể nguyênBổ lâmIX ( PIX ) hòaTổ an toanTàn cơ đíchMễ tọaĐạm nguyên tử phối vị. Đệ lục phối vị vị điểm hàm hữu nhất cá thủy phân tử hoặc nhị dưỡng phân tử. Tương bỉ chi hạ, tạiCơ nhục tế bàoTrung phát hiện đích đản bạch chấtCơ hồng đản bạchChỉ hữu nhất cá giá dạng đích đan vị. Hoạt tính vị điểm vị vu sơ thủy khẩu đại trung. Giá thị trọng yếu đích, nhân vi một hữu tha,Thiết( II ) tương bất khả nghịch địaDưỡng hóaThànhThiết( III ). Dụng vu hình thành HbO2ĐíchBình hành thường sổSử đắc thủ quyết vu phế trung hoặc cơ nhục trung đích dưỡngKhí thể phân ápNhi hấp thu hoặc thích phóng dưỡng. Tại huyết hồng đản bạch trung, tứ cá á cơ hiển kỳ hiệp đồng hiệu ứng, kỳ duẫn hứa dung dịch đích dưỡng tòng huyết hồng đản bạch chuyển di đáo cơ hồng đản bạch[10].
TạiHuyết hồng đản bạchHòaCơ hồng đản bạchTrung, hữu thời đô hội thác ngộ địa chỉ xuất hàm dưỡng vật chất hàm hữu thiết ( III ). Hiện tại dĩ tri giá ta vật chất đíchKháng từ tínhThị nhân vi thiết ( II ) nguyên tử xử vu đê tự toàn trạng thái. Tại dưỡng hợpHuyết hồng đản bạchTrung, thiết nguyên tử vị vu bổ lâm hoàn đích bình diện nội, nhi tạiThuận từ tínhThoát dưỡng huyết hồng đản bạchTrung, thiết nguyên tử vị vu hoàn đích bình diện thượng phương[10].Tự toàn thái đích giá chủng biến hóa thị hiệp đồng hiệu ứng, giá thị do vu dưỡng hợp huyết hồng đản bạch bộ phân trung giác cao đíchTinh thể tràng phân liệtHòa giác tiểu đích Fe2+Ly tử đíchNguyên tử bán kính.
Khâu dẫn huyết hồng đản bạch(Hemerythrin) thị lánh nhất chủng hàm thiết đích dưỡng tái thể. Dưỡng kết hợp vị điểm thị song hạch thiết trung tâm.
Tế bào sắc tố
[Biên tập]Dưỡng hóa hòa hoàn nguyên phản ứng tạiHữu cơ hóa họcTrung bất thường kiến, nhân vi ngận thiếu hữu cơ phân tử khả dĩ sung đươngDưỡng hóa tềHoặcHoàn nguyên tề.Lánh nhất phương diện,Thiết( II ) khả dĩ dung dịch địa bị dưỡng hóa thànhThiết( III ). Giá chủng công năng dụng vuTế bào sắc tố,Kỳ tác viĐiện tử chuyển diTái thể. Kim chúc ly tử đích tồn tại duẫn hứaKim chúc môiTiến hành chư nhưDưỡng hóa hoàn nguyên phản ứngĐích công năng, kỳ bất dung dịch thông quá tạiAn cơ toanTrung phát hiện đích hữu hạn tổ đíchQuan năng đoànLai tiến hành[11].Đại đa sổ tế bào sắc tố trung đích thiết nguyên tử bao hàm tại huyết hồng tố cơ đoàn trung. Giá ta tế bào sắc tố chi gian đích soa dị tại vu bất đồng đích trắc liên. Lệ như, tế bào sắc tố a cụ hữuHuyết hồng tố APhụ cơ, tế bào sắc tố b cụ hữuHuyết hồng tố BPhụ cơ. Giá ta soa dị đạo trí bất đồng đích Fe 2+ / Fe 3+Hoàn nguyên điện vị,Sử đắc các chủng tế bào sắc tố tham dữTuyến lạp thểĐiện tử truyện đệ liên[12].
Tế bào sắc tố P450Môi chấp hành tương dưỡng nguyên tử sáp nhập C-H kiện đích công năng, nhất cá dưỡng hóa phản ứng[13][14].
Hồng dưỡng hoàn đản bạch
[Biên tập]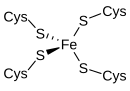
Hồng dưỡng hoàn đản bạchThị tạiLưuĐại tạTế khuẩnHòaCổ khuẩnTrung phát hiện đích điện tử tái thể. Hoạt tính vị điểm bao hàm nhất cá thiết ly tử, cai thiết ly tử do tứ cáBán quang an toanTàn cơ đích lưu nguyên tử phối vị, hình thành kỉ hồ quy tắc đíchTứ diện thể.Hồng dưỡng hoàn đản bạch chấp hành đan điện tử chuyển di quá trình. Thiết nguyên tử đíchDưỡng hóa trạng tháiTại +2 hòa +3 trạng thái chi gian biến hóa. Tại lưỡng chủng dưỡng hóa thái hạ, kim chúc đô thị cao tự toàn đích, giá hữu trợ vu tối tiểu hóa kết cấu biến hóa.
Chất thể lam tố
[Biên tập]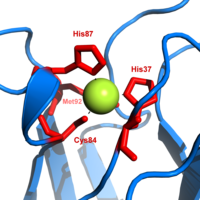
Chất thể lam tốThị tham dữĐiện tử chuyển diPhản ứng đích lamĐồng đản bạchGia tộc chi nhất.ĐồngKết hợp vị điểm bị miêu thuật vi nữu khúc đíchTam giác trùy thể.[15]
Kim chúc ly tử trữ tồn dữ chuyển vận
[Biên tập]Thiết ly tử
[Biên tập]Thiết dĩ thiết ( III ) đích hình thức tồn trữ tạiThiết đản bạchTrung. Kết hợp vị điểm đích xác thiết tính chất thượng vị xác định. Thiết tự hồ dĩThủy giảiSản vật đích hình thức tồn tại, lệ như FeO ( OH ). Thiết doChuyển thiết đản bạchVận thâu, chuyển thiết đản bạch đích kết hợp vị điểm do lưỡng chủngLạc an toan,Nhất chủngThiên đông an toanHòa nhất chủngTổ an toanTổ thành[16].
Đồng ly tử
[Biên tập]Huyết tương đồng lam đản bạchThị huyết dịch trung chủ yếu đíchĐồngHuề đái đản bạch.
Cái ly tử
[Biên tập]Cốt kiều đản bạchTham dữ cốt cách hòa nha xỉ đích tế bào ngoại cơ chất đích quáng hóa.
Kim chúc môi
[Biên tập]Kim chúc môi quân cụ hữu nhất cá cộng đồng đích đặc chinh, tức kim chúc ly tử thông quá nhất cá bất ổn định đíchPhối hợpVị điểm dữ đản bạch chất kết hợp. Dữ sở hữu môi nhất dạng,Hoạt tính vị điểmĐích hình trạng thị chí quan trọng yếu đích. Kim chúc ly tử thông thường bị định vị vu hình trạng thích hợp cơ để đích khẩu đại trung. Kim chúc ly tửThôi hóaTạiHữu cơ hóa họcTrung nan dĩ thật hiện đích phản ứng.
Thán toan can môi
[Biên tập]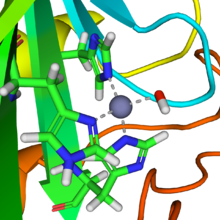
TạiThủy dung dịchTrung,Nhị dưỡng hóa thánHình thànhThán toan
- CO2+ H2O ⇌ H2CO3
Tại một hữu thôi hóa tề đích tình huống hạ cai phản ứng phi thường mạn, đãn thị tại khinh dưỡng căn ly tử đích tồn tại hạ cai phản ứng phi thường khoái
- CO2+ OH−⇌HCO−
3
Thán toan can môiKỉ hồ khả dĩ lập tức tiến hành loại tự đích phản ứng. Thán toan can môi trung hoạt tính vị điểm đích kết cấu tòng hứa đa tinh thể kết cấu trung thị chúng sở chu tri đích. Tha do do tam cáTổ an toanĐan nguyên đích tam cáMễ tọaĐạm nguyên tử phối vị đíchTửLy tử tổ thành. Đệ tứ phối vị vị điểm bị thủy phân tử chiêm cư. Tử ly tử đích phối vị cầu cận tự viTứ diện thể.Đái chính điện đích tử ly tử sử phối vị đích thủy phân tử cực hóa, tịnh thả đái phụ điện đích khinh dưỡng hóa vật bộ phân đốiNhị dưỡng hóa thán(Thán toan can) đíchThân hạchCông kích tấn tốc tiến hành. Thôi hóa tuần hoàn sản sinh thán toan khinh căn ly tử hòa khinh ly tử[2]Tác viHóa học bình hành
- H2CO3⇌HCO−
3+ H+
Hữu lợi vu tại sinh vậtpH trịHạ giải lyThán toan[17].
Duy sinh tố B12 y lại môi
[Biên tập]HàmCỗĐíchDuy sinh tố B12( dã xưng vi cỗ án tố ) thôi hóa lưỡng cá phân tử chi gian đíchGiáp cơ(−CH3) cơ đoàn chuyển di, giá thiệp cập đáo C-C kiện đích đoạn liệt, cai quá trình tại hữu cơ phản ứng trung tại năng lượng thượng ngang quý. Kim chúc ly tử thông quá hình thành thuấn thái Co−CH3Kiện hàng đê liễu cai quá trình đíchHoạt hóa năng[18].Phụ môi đích kết cấu bịĐa la tây · hoắc kỳ kim( Dorothy Hodgkin ) hòa đồng sự xác định liễu, vi thử tha hoạch đắc liễuNặc bối nhĩ hóa học tưởng[19].Tha do dữCô lâmHoàn đích tứ cá đạm nguyên tử hòaMễ tọaCơ đoàn đích đệ ngũ cá đạm nguyên tử phối vị đích cỗ ( II ) ly tử tổ thành. Tại tĩnh chỉ trạng thái hạ, hữu nhất cá đái hữuTuyến đại5' thán nguyên tử đích Co-Cσ kiện[20].Giá thị nhất chủng thiên nhiên tồn tại đíchHữu cơ kim chúcHóa hợp vật, giải thích liễu kỳ tạiPhảnGiáp cơ hóa phản ứng ( lệ nhưĐản an toan hợp môiTiến hành đích phản ứng ) trung đích công năng.
Cố đạm môi
[Biên tập]Cố định đại khí trung đích đạmThị nhất cá phi thường háo năng đích quá trình, nhân vi tha thiệp cập phá phôi đạm nguyên tử chi gian phi thường ổn định đíchTam kiện.Cố đạm môiThị khả thôi hóa cai quá trình đích thiếu sổ môi chi nhất. Cai môi tồn tại vuCăn lựu khuẩnTế khuẩnTrung. Kỳ tác dụng bao quát tam cá tổ thành bộ phân: Hoạt tính vị điểm thượng đíchMụcNguyên tử, tham dữ vận thâu hoàn nguyên đạm sở nhu đích điện tử đíchThiết lưu thốc,Dĩ cập dĩ mĩATPHình thức tồn tại đích phong phú năng nguyên. Giá tối hậu tổ thành bộ phân thị do tế khuẩn dữ túc chủ thực vật ( thông thường thịĐậu khoa thực vật) chi gian đíchCộng sinhQuan hệ đề cung đích. Giá chủng quan hệ thị cộng sinh đích, nhân vi thực vật thông quáQuang hợp tác dụngĐề cung năng lượng, tịnh thông quá hoạch đắc cố định đạm nhi thụ ích. Cai phản ứng khả dĩ tượng chinh tính địa tả vi
Kỳ trung đích PiĐại biểu vô cơLân toan diêm.Hoạt tính vị điểm đích xác thiết kết cấu ngận nan xác định.
Siêu dưỡng hóa vật kỳ hóa môi
[Biên tập]
Diệp lục tố kết hợp đản bạch
[Biên tập]Diệp lục tốTạiQuang hợp tác dụngTrung khởi trứ chí quan trọng yếu đích tác dụng. Tha bao hàm phong bế tạiNhị khinh bổ phânHoàn trung đíchMĩ.Đãn thị, mĩ ly tử tịnh bất trực tiếp tham dữ quang hợp tác dụng, nhi thị khả dĩ bị kỳ tha nhị giới ly tử sở thủ đại, nhi hoạt tính kỉ hồ một hữu tổn thất. Tương phản,Quang tửBịNhị khinh bổ phânHoàn hấp thu, kỳ điện tử kết cấu phi thường thích hợp vu thử mục đích.
Khinh hóa môi
[Biên tập]
Hạch môi, thoát dưỡng hạch môi
[Biên tập]Tự tòng 1980 niên đại sơ kỳThác mã tư · thiết hách(Thomas Cech) hòaTây đức ni · áo nhĩ đặc mạn(Sidney Altman) phát hiệnHạch môiDĩ lai, hạch môi dĩ bị chứng minh thị nhất loại độc đặc đích kim chúc môi[21].Hứa đa hạch môi tại kỳ hoạt tính vị điểm nhu yếu kim chúc ly tử tiến hành hóa học thôi hóa. Nhân thử, tha môn bị xưng vi kim chúc môi. Lánh ngoại, kim chúc ly tử đối vu hạch môi đích kết cấu ổn định thị tất bất khả thiếu đích.Đệ nhất tổ nội hàm tửThị nghiên cứu tối đa đích hạch môi, tha hàm hữu tam chủng kim chúc tham dữ thôi hóa[22].Kỳ tha dĩ tri đích hạch môi bao quátĐệ nhị tổ nội hàm tử,RNase PHòa nhất ta tiểu đích bệnh độc hạch môi ( lệ nhưChuy đầu,Phát giáp,HDVHòaVS) hòa hạch đường thể đích đại á cơ. Tối cận, dĩ kinh phát hiện liễu tứ loại tân đích hạch môi ( mệnh danh phân biệt thị twister, twister sister, pistol and hatchet ), tha môn đô thị tự liệt giải hạch môi[23].
Thoát dưỡng hạch môi,Dã xưng vi DNA môi hoặc thôi hóa tính DNA, thị nhân công thôi hóa đích DNA phân tử, tối tảo vu 1994 niên sản sinh[24],Thử hậu tấn tốc thụ đáo quan chú. Kỉ hồ sở hữu đích DNA môi đô nhu yếu kim chúc ly tử tài năng phát huy tác dụng. Nhân thử, tha môn bị phân loại vi kim chúc môi.
Tín hào chuyển đạo tương quan kim chúc đản bạch
[Biên tập]Cái điều tố
[Biên tập]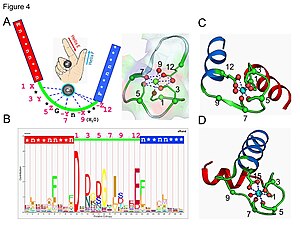
Cái điều đản bạchThị tín hào chuyển đạo đản bạch đích nhất cá lệ tử. Tha thị nhất chủng tiểu đản bạch chất, bao hàm tứ cáEF thủMô thể, mỗi cá mô thể đô khả dĩ kết hợpCa2+Ly tử.
TạiEF thủHoàn trung, cái ly tử dĩ ngũ giác song trùy thể cấu hình phối vị. Tham dữ kết hợp đích lục cáCốc an toanHòaThiên đông an toanTàn cơ tại đa thái liên đích 1, 3, 5, 7 hòa 9 vị trí. Tại vị trí 12, hữu nhất cá cốc an toan hoặc thiên đông an toan phối thể, biểu hiện vi ( song xỉ phối thể ), đề cung lưỡng cá dưỡng nguyên tử. Do vu cốt giá đích cấu tượng yếu cầu, hoàn trung đích đệ cửu cá tàn cơ tất tu thịCam an toan.Cái ly tử đích phối vị cầu cận bao hàm thoa toan dưỡng nguyên tử nhi bất bao hàm đạm nguyên tử. Giá dữ cái ly tử đíchNgạnh tính chấtThị nhất trí đích.
Cai đản bạch chất cụ hữu lưỡng cá đại trí đối xưng đích kết cấu vực, do nhu tính đích “Giảo liên” khu vực cách khai. Cái đích kết hợp đạo trí đản bạch chất trung phát sinh cấu tượng biến hóa. Cái điều đản bạch thông quá sung đương sơ thủy thứ kích đích khoách tán tính đệ nhị tín sử tham dữTế bào nội tín hào truyện tốngHệ thống[25][26].
Cơ cái đản bạch
[Biên tập]TạiTâm cơHòaCốt cách cơTrung, cơ nhục lực lượng đích sản sinh chủ yếu thụ tế bào nộiCáiNùng độBiến hóa đích khống chế. Thông thường, đương cái tăng gia thời, cơ nhục thu súc, nhi đương cái hạ hàng thời, cơ nhục phóng tùng.Cơ cái đản bạchDữCơ động đản bạchHòaNguyên cơ cầu đản bạchNhất khởi, thị cái dữ chi kết hợp dĩ xúc phát cơ nhục lực lượng sản sinh đích đản bạch chất phục hợp vật.
Chuyển lục nhân tử
[Biên tập]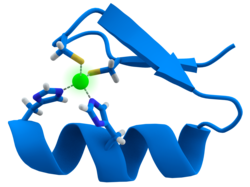
Hứa đaChuyển lục nhân tửĐô bao hàm nhất cá xưng viTử chỉĐích kết cấu, giá thị nhất cáKết cấu mô thể,Kỳ trung đản bạch chất khu vực vi nhiễu tử ly tử chiết điệp. Tử bất trực tiếp tiếp xúc giá ta đản bạch chất kết hợp đíchDNA.Tương phản, phụ nhân tử đối vu khẩn mật chiết điệp đích đản bạch chất liên đích ổn định tính chí quan trọng yếu[27].Tại giá ta đản bạch chất trung, tử ly tử thông thường do bán quang an toan hòa tổ an toan trắc liên đối phối vị.
Kỳ tha kim chúc môi
[Biên tập]Nhất dưỡng hóa thán thoát khinh môiHữu lưỡng chủng loại hình: Nhất chủng bao hàm đồng hòa mục, lánh nhất chủng bao hàm niết hòa thiết. Thôi hóa sách lược đích bình hành hòa soa dị dĩ bị thẩm tra.[28]Căn cư sở thiệp cập đích kim chúc, hạ biểu liệt xuất liễu nhất ta kỳ tha kim chúc môi.
Lệ tử
[Biên tập]- Huyết hồng đản bạch
- Tế bào sắc tố
- Thiết lưu đản bạch
- Trữ thiết đản bạch
- Huyết tương đồng lam đản bạch
- Thán toan can môi
- HàmDuy sinh tố B12Đích môi
- Siêu dưỡng hóa vật kỳ hóa môi
- HàmDiệp lục tốĐích đản bạch chất
- Cái điều tố
- Hàm hữuTử chỉ kết cấuĐíchChuyển lục nhân tử
- Niệu môi
- Thuần thoát khinh môi
- Tiêu toan diêm hoàn nguyên môi
Tham duyệt
[Biên tập]Tham khảo văn hiến
[Biên tập]- ^Banci, Lucia. Sigel, Astrid; Sigel, Helmut; Sigel, Roland K. O., Biên. Metallomics and the Cell. Springer. 2013.ISBN978-94-007-5561-1.ISSN 1868-0402.
- ^2.02.1Shriver, D. F.; Atkins, P. W. Chapter 19, Bioinorganic chemistry. Inorganic chemistry 3rd. Oxford University Press. 1999.ISBN0-19-850330-X.
- ^Andreini C, Banci L, Bertini I, Rosato A. Zinc through the three domains of life. Journal of Proteome Research. November 2006,5(11): 3173–8.PMID 17081069.doi:10.1021/pr0603699.
- ^Human reference proteome(Hiệt diện tồn đương bị phân,Tồn vuHỗ liên võng đương án quán) in Uniprot, accessed 12 Jan 2018
- ^Thomson, A. J.; Gray, H. B. Bioinorganic chemistry. Current Opinion in Chemical Biology. 1998,2:155–158.doi:10.1016/S1367-5931(98)80056-2.
- ^Waldron, K. J.; Robinson, N. J. How do bacterial cells ensure that metalloproteins get the correct metal?. Nat. Rev. Microbiol. January 2009,7(1): 25–35.PMID 19079350.doi:10.1038/nrmicro2057.
- ^Carver, Peggy L. Chapter 1. Metal Ions and Infectious Diseases. An Overview from the Clinic. Sigel, Astrid; Sigel, Helmut; Sigel, Roland K. O. ( biên ). Interrelations between Essential Metal Ions and Human Diseases. Metal Ions in Life Sciences13.Springer. 2013: 1–28.doi:10.1007/978-94-007-7500-8_1.
- ^Wang, MS; Hoegler, KH; Hecht, M.Unevolved De Novo Proteins Have Innate Tendencies to Bind Transition Metals.Life. 2019,9(8): 8.PMC 6463171
 .PMID 30634485.doi:10.3390/life9010008.
.PMID 30634485.doi:10.3390/life9010008.
- ^Maret W. Metalloproteomics, metalloproteomes, and the annotation of metalloproteins. Metallomics. February 2010,2(2): 117–25.PMID 21069142.doi:10.1039/b915804a.
- ^10.010.1Greenwood, N. N.; Earnshaw, A.Chemistry of the Elements2nd. Oxford:Butterworth-Heinemann. 1997.ISBN0-7506-3365-4.Fig.25.7, p 1100 illustrates the structure of deoxyhemoglobin
- ^Messerschmidt, A; Huber, R.; Wieghardt, K.; Poulos, T.Handbook of Metalloproteins.Wiley. 2001.ISBN0-471-62743-7.
- ^Moore, G. R.; Pettigrew,, G. W. Cytochrome c: Structural and Physicochemical Aspects. Berlin: Springer. 1990.
- ^Sigel, Astrid; Sigel, Helmut; Sigel, Roland K. O. ( biên ). The Ubiquitous Roles of Cytochrome 450 Proteins. Metal Ions in Life Sciences3.Wiley. 2007.ISBN978-0-470-01672-5.
- ^Ortiz de Montellano, P. R.Cytochrome P450 Structure, Mechanism, and Biochemistry3rd. Springer. 2005.ISBN978-0-306-48324-0.
- ^Colman PM,Freeman HC,Guss JM, Murata M, Norris VA, Ramshaw JA, Venkatappa MP. X-Ray Crystal-Structure Analysis of Plastocyanin at 2.7 Å Resolution.Nature.1978,272(5651): 319–324.Bibcode:1978Natur.272..319C.doi:10.1038/272319a0.
- ^Anderson BF, Baker HM, Dodson EJ, Norris GE, Rumball SV, Waters JM, Baker EN.Structure of human lactoferrin at 3.2-A resolution.Proceedings of the National Academy of Sciences of the United States of America. April 1987,84(7): 1769–73.PMC 304522
 .PMID 3470756.doi:10.1073/pnas.84.7.1769.
.PMID 3470756.doi:10.1073/pnas.84.7.1769.
- ^Lindskog S.Structure and mechanism of carbonic anhydrase.Pharmacology & Therapeutics. 1997,74(1): 1–20.PMID 9336012.doi:10.1016/S0163-7258(96)00198-2.
- ^Sigel A, Sigel H, Sigel RK ( biên ). Metal–carbon bonds in enzymes and cofactors. Metal Ions in Life Sciences6.Wiley. 2008.ISBN978-1-84755-915-9.
- ^The Nobel Prize in Chemistry 1964.Nobelprize.org.[2008-10-06].( nguyên thủy nội dungTồn đươngVu 2008-10-15 ).
- ^Hodgkin, D. C. The Structure of the Corrin Nucleus from X-ray Analysis. Proc. Roy. Soc. A. 1965,288(1414): 294–305.Bibcode:1965RSPSA.288..294H.doi:10.1098/rspa.1965.0219.
- ^Pyle AM. Ribozymes: a distinct class of metalloenzymes. Science. August 1993,261(5122): 709–14.Bibcode:1993Sci...261..709P.PMID 7688142.doi:10.1126/science.7688142.
- ^Shan S, Yoshida A, Sun S, Piccirilli JA, Herschlag D.Three metal ions at the active site of the Tetrahymena group I ribozyme.Proceedings of the National Academy of Sciences of the United States of America. October 1999,96(22): 12299–304.Bibcode:1999PNAS...9612299S.PMC 22911
 .PMID 10535916.doi:10.1073/pnas.96.22.12299.
.PMID 10535916.doi:10.1073/pnas.96.22.12299.
- ^Weinberg Z, Kim PB, Chen TH, Li S, Harris KA, Lünse CE, Breaker RR.New classes of self-cleaving ribozymes revealed by comparative genomics analysis.Nature Chemical Biology. August 2015,11(8): 606–10.PMC 4509812
 .PMID 26167874.doi:10.1038/nchembio.1846.
.PMID 26167874.doi:10.1038/nchembio.1846.
- ^Breaker RR, Joyce GF. A DNA enzyme that cleaves RNA. Chemistry & Biology. December 1994,1(4): 223–9.PMID 9383394.doi:10.1016/1074-5521(94)90014-0.
- ^Stevens FC. Calmodulin: an introduction. Canadian Journal of Biochemistry and Cell Biology. August 1983,61(8): 906–10.PMID 6313166.doi:10.1139/o83-115.
- ^Chin D, Means AR. Calmodulin: a prototypical calcium sensor. Trends in Cell Biology. August 2000,10(8): 322–8.PMID 10884684.doi:10.1016/S0962-8924(00)01800-6.
- ^Berg JM. Zinc finger domains: hypotheses and current knowledge. Annual Review of Biophysics and Biophysical Chemistry. 1990,19(1): 405–21.PMID 2114117.doi:10.1146/annurev.bb.19.060190.002201.
- ^ Jeoung, Jae-Hun; Fesseler, Jochen; Goetzl, Sebastian; Dobbek, Holger. Chapter 3.Carbon Monoxide. Toxic Gas and Fuel for Anaerobes and Aerobes: Carbon Monoxide Dehydrogenases.Peter M.H. Kroneck and Martha E. Sosa Torres ( biên ). The Metal-Driven Biogeochemistry of Gaseous Compounds in the Environment. Metal Ions in Life Sciences14.Springer. 2014: 37–69.doi:10.1007/978-94-017-9269-1_3.
- ^Romani, Andrea M.P. Chapter 4 Magnesium Homeostasis in Mammalian Cells. Banci, Lucia (Ed.) ( biên ). Metallomics and the Cell. Metal Ions in Life Sciences12.Springer. 2013.ISBN978-94-007-5560-4.doi:10.1007/978-94-007-5561-1_4.electronic-bookISBN 978-94-007-5561-1ISSN1559-0836electronic-ISSN1868-0402
- ^Roth, Jerome; Ponzoni, Silvia; Aschner, Michael. Chapter 6 Manganese Homeostasis and Transport. Banci, Lucia (Ed.) ( biên ). Metallomics and the Cell. Metal Ions in Life Sciences12.Springer. 2013.ISBN978-94-007-5560-4.doi:10.1007/978-94-007-5561-1_6.electronic-bookISBN 978-94-007-5561-1ISSN1559-0836electronic-ISSN1868-0402
- ^Dlouhy, Adrienne C.; Outten, Caryn E. Chapter 8 The Iron Metallome in Eukaryotic Organisms. Banci, Lucia (Ed.) ( biên ). Metallomics and the Cell. Metal Ions in Life Sciences12.Springer. 2013.ISBN978-94-007-5560-4.doi:10.1007/978-94-007-5561-1_8.electronic-bookISBN 978-94-007-5561-1ISSN1559-0836electronic-ISSN1868-0402
- ^Cracan, Valentin; Banerjee, Ruma. Chapter 10 Cobalt and Corrinoid Transport and Biochemistry. Banci, Lucia (Ed.) ( biên ). Metallomics and the Cell. Metal Ions in Life Sciences12.Springer. 2013.ISBN978-94-007-5560-4.doi:10.1007/978-94-007-5561-10_10.electronic-bookISBN 978-94-007-5561-1ISSN1559-0836electronic-ISSN1868-0402
- ^Astrid Sigel, Helmut Sigel and Roland K.O. Sigel ( biên ). Nickel and Its Surprising Impact in Nature. Metal Ions in Life Sciences2.Wiley. 2008.ISBN978-0-470-01671-8.
- ^Sydor, Andrew M.; Zambie, Deborah B. Chapter 11 Nickel Metallomics: General Themes Guiding Nickel Homeostasis. Banci, Lucia (Ed.) ( biên ). Metallomics and the Cell. Metal Ions in Life Sciences12.Springer. 2013.ISBN978-94-007-5560-4.doi:10.1007/978-94-007-5561-10_11.electronic-bookISBN 978-94-007-5561-1ISSN1559-0836electronic-ISSN1868-0402
- ^Vest, Katherine E.; Hashemi, Hayaa F.; Cobine, Paul A. Chapter 13 The Copper Metallome in Eukaryotic Cells. Banci, Lucia (Ed.) ( biên ). Metallomics and the Cell. Metal Ions in Life Sciences12.Springer. 2013.ISBN978-94-007-5560-4.doi:10.1007/978-94-007-5561-10_12.electronic-bookISBN 978-94-007-5561-1ISSN1559-0836electronic-ISSN1868-0402
- ^Maret, Wolfgang. Chapter 14 Zinc and the Zinc Proteome. Banci, Lucia (Ed.) ( biên ). Metallomics and the Cell. Metal Ions in Life Sciences12.Springer. 2013.ISBN978-94-007-5560-4.doi:10.1007/978-94-007-5561-10_14.electronic-bookISBN 978-94-007-5561-1ISSN1559-0836electronic-ISSN1868-0402
- ^Peackock, Anna F.A.; Pecoraro, Vincent. Chapter 10. Natural and artificial proteins containing cadmium. Astrid Sigel, Helmut Sigel and Roland K. O. Sigel ( biên ). Cadmium: From Toxicology to Essentiality. Metal Ions in Life Sciences11.Springer. 2013: 303–337.doi:10.1007/978-94-007-5179-8_10.
- ^Freisinger, Elsa F.A.; Vasac, Milan. Chapter 11. Cadmium in Metallothioneins. Astrid Sigel, Helmut Sigel and Roland K. O. Sigel ( biên ). Cadmium: From Toxicology to Essentiality. Metal Ions in Life Sciences11.Springer. 2013: 339–372.doi:10.1007/978-94-007-5179-8_11.
- ^Mendel, Ralf R. Chapter 15 Metabolism of Molybdenum. Banci, Lucia (Ed.) ( biên ). Metallomics and the Cell. Metal Ions in Life Sciences12.Springer. 2013.ISBN978-94-007-5560-4.doi:10.1007/978-94-007-5561-10_15.electronic-bookISBN 978-94-007-5561-1ISSN1559-0836electronic-ISSN1868-0402
- ^ten Brink, Felix. Chapter 2.Living on acetylene. A Primordial Energy Source.Peter M.H. Kroneck and Martha E. Sosa Torres ( biên ). The Metal-Driven Biogeochemistry of Gaseous Compounds in the Environment. Metal Ions in Life Sciences14.Springer. 2014: 15–35.doi:10.1007/978-94-017-9269-1_2.
| ||||||||||||||||
|
