Phối hợp vật
Này điều mụcYêu cầu bổ sung càng nhiềuNơi phát ra.(2014 năm 5 nguyệt 17 ngày) |
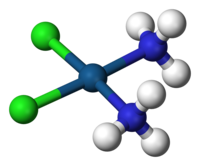
Một cái bạc nguyên tử có 4 cáiXứng thể

Xứng vị hoá chất( tiếng Anh:coordination complex) lại xưngXứng vị lạc hợp vật,Tên gọi tắtPhối hợp vật,Lạc hợp vật,Hợp chất,Lạc muối,Là từ một cái trung tâmNguyên tửHoặcLy tửHơn nữa chung quanh phối trí mấy cái kết hợpPhần tửHoặc ly tử sở tạo thànhHoá chất;Người trước ( trung tâm ) xưng làXứng vị trung tâm( tiếng Anh:coordination center), thông thường làKim loại;Người sau ( chung quanh ) tắc xưng làXứng thể( tiếng Anh:ligand) hoặcLạc thuốc nước( tiếng Anh:comple xing agent)[1][2][3].Xứng vị trung tâm cùng xứng thể lấyXứng vị kiệnTương kết hợp mà hình thành phức tạp phần tử hoặc ly tử cấu thành một cái đơn nguyên, xưng là “Xứng vị đơn nguyên”; mà bất luận cái gì đựng xứng vị đơn nguyên hoá chất, đều xưng là xứng vị hoá chất[4].Nghiên cứu phối hợp vật hóa học chi nhánh xưng làXứng vị hóa học.
Rất nhiều hàm kim loại hoá chất, đặc biệt là đựngQuá độ kim loại( thuộc vềNguyên tố bảng chu kỳd khu nguyên tố,Tỷ nhưThái) hoá chất, đều là xứng vị hoá chất[5].Phối hợp vật làHoá chấtTrung trọng đại một cái tử phân loại, rộng khắp ứng dụng với sinh hoạt hằng ngày, công nghiệp sinh sản cậpSinh mệnh khoa họcTrung, mấy năm gần đây tới phát triển đặc biệt nhanh chóng. Nó không chỉ có cùngVô cơ hoá chất,Hữu cơ kim loại hoá chấtTương quan liên, hơn nữa cùng hiện nay hóa học tuyến đầuNguyên tử thốc hóa học,Xứng vịThôi hóaCậpPhần tử sinh vật họcĐều có rất lớn trùng điệp.
Tường thuật tóm lược[Biên tập]
Phản ứng vật đã chịu hoạt hoá có thể đạt tới thấp hạn có thể khi sinh ra vật chất xưng là sai hợp thể, thảo luận kinh điển xứng vị hoá chất khi, hội nghị thường kỳ nhắc tới dưới thuật ngữ[6]:
- Xứng vị kiện,Xứng vị cộng giới kiện:Xứng vị hoá chất trung tồn tạiLiên kết hoá học,Từ một cái nguyên tử cung cấp thành kiện hai cái điện tử, trở thành điện tử cho thể, một cái khác thành kiện nguyên tử tắc trở thành điện tử tiếp thu thể. Tham kiếnToan kiềm phản ứngCùngLouis toan kiềm lý luận.
- Xứng vị đơn nguyên:Hoá chất đựng xứng vị kiện một bộ phận, có thể là phần tử hoặc ly tử.
- Xứng ly tử:Đựng xứng vị kiện ly tử, có thể là dương ly tử hoặc i-on âm.
- Nội giới,Ngoại giới:Nội giới chỉ xứng vị đơn nguyên, ngoại giới cùng nội giới tương đối.
- Xứng thể,Xứng vị thể,Xứng vị cơ:Cung cấp điện tử đối phần tử hoặc ly tử.
- Xứng vị nguyên tử:Xứng thể trung, cung cấp điện tử đối nguyên tử.
- Trung tâm nguyên tử,Kim loại nguyên tử:Giống nhau chỉ tiếp thu điện tử đối nguyên tử.
- Xứng vị số:Trung tâm nguyên tử chung quanh xứng vị nguyên tử cái số.
- Ngao hợp vật:ĐựngNgao hợpXứng thể phối hợp vật.
Ngoài ra, đựng nhiều trung tâm nguyên tử phối hợp vật xưng làNhiều hạch phối hợp vật,Liên tiếp hai cái trung tâm nguyên tử xứng thể xưng làKiều liên xứng thể,LấyGốc OHKiều liên xưng làThưởng liên,Lấy oxy cơ kiều liên xưng làOxy liên.
Lịch sử[Biên tập]
Mọi người rất sớm liền bắt đầu tiếp xúc xứng vị hoá chất, lúc ấy phần lớn dùng làm sinh hoạt hằng ngày sử dụng, nguyên liệu cũng trên cơ bản là từ thiên nhiên lấy được, tỷ như sát trùng tềChalcanthiteCùng dùng làm thuốc nhuộmPhổ lam.Sớm nhất đối phối hợp vật nghiên cứu bắt đầu với 1798 năm. Nước Pháp nhà hóa họcTháp tát ách ngươiLần đầu dùng nhị giớiCobanMuối,Clo hóa AmoniCùngDung dịch amoniacChế bị ra CoCl3.6NH3,Đồng phát hiệnCác,Nickel,Đồng,BạcChờ kim loại cùng với Cl−,H2O, CN−,COCùngC2H4Cũng đều có thể sinh thành cùng loại hoá chất. Lúc ấy cũng không pháp giải thích này đó hoá chất thành kiện cập tính chất, sở tiến hành đại bộ phận thực nghiệm cũng chỉ cực hạn với phối hợp vật nhan sắc sai biệt quan sát, thủy dung dịch nhưng bịBạcLy tử lắng đọng lại Moore số cùng vớiDẫn điệnTrắc định. Đối với này đó phối hợp vật trung thành kiện tình huống, lúc ấy tương đối thịnh hành cách nói mượnHoá học hữu cơTư tưởng, cho rằng loại này phần tử vì liên trạng, chỉ có phía cuối kho ly tử có thể ly giải ra tới, mà bị bạc ly tử lắng đọng lại. Nhưng mà loại này cách nói thực gượng ép, không thể thuyết minh sự thật rất nhiều.
1893 năm, Thụy Sĩ nhà hóa họcDuy ngươi nạpTổng kết tiền nhân lý luận, lần đầu đưa ra hiện đạiXứng vị kiện,Xứng vị sốCùng xứng vị hoá chất kết cấu chờ một loạt cơ bản khái niệm, thành công giải thích rất nhiều phối hợp vật dẫn điện tính chất,Dị cấu hiện tượngCậpTừ tính.Từ đây,Xứng vị hóa họcMới có bản chất phát triển. Duy ngươi nạp cũng bị xưng là “Xứng vị hóa học chi phụ”, cũng bởi vậy đạt được 1913 nămNobel hóa học thưởng.
1923 năm, Anh quốc nhà hóa họcTây quý uy khắcĐưa ra “Hữu hiệu nguyên tử số”Pháp tắc ( EAN ), nhắc nhở trung tâm nguyên tử điện tử số cùng nó xứng vị số chi gian quan hệ. Rất nhiều phối hợp vật, đặc biệt làCacbonyl phối hợp vật,Đều là phù hợp nên pháp tắc, nhưng cũng có rất nhiều không phù hợp ví dụ. Tuy rằng cái này pháp tắc chỉ là bộ phận phản ánh phối hợp vật hình thành thực chất, nhưng này tư tưởng lại cũng thúc đẩy xứng vị hóa học phát triển.
Hiện đại xứng vị hóa học không hề câu nệ với điện tử đối thi chịu quan hệ, mà là rất lớn trình độ thượng mượn dùng vớiPhần tử quỹ đạo lý luậnPhát triển, bắt đầu nghiên cứu tân loại hình phối hợp vật nhưCó nhân phối hợp vậtCùngThốc hợp vật.Trong đó một cái điển hình ví dụ đó làThái thị muối—K[Pt(C2H4)Cl3]. Tuy rằng nên hoá chất sớm tại 1827 năm liền đã chế đến, nhưng thẳng đến 1950 năm mới nghiên cứu rõ ràng trong đóPhản hồi π kiệnTính chất.
Phân loại[Biên tập]
Xứng vị hoá chất nhưng phân thành truyền thống xứng vị hoá chất cậpHữu cơ kim loại hoá chất.
- Truyền thống xứng vị hoá chất từ một cái trở lên xứng ly tử ( cũng kêu ly tử hợp chất ) hình thành, xứng vị kiện trung điện tử “Cơ hồ” toàn bộ từ xứng thể cung cấp. Điển hình xứng thể bao gồmH2O,NH3,Cl−,CN−Cùngen.
- Ví dụ: [Co(EDTA)]−,[Co(NH3)6]Cl3,[K3Fe(C2O4)3]Cùng [Cr(H2O)6]Cl3.
- Hữu cơ kim loại hoá chất chỉ đựng kim loại - chưng khô học kiện hoá chất, xứng thể vì hữu cơGốc( nhưAnken,Khuyết hydrocarbon,Hoàn cơ,Hương thơm hoàn) hoặc tính chất cùng loại hóa học phẩm, như膦,Hydro mang điện âm,Carbon monoxit.
- Ví dụ:((C5H5)Fe(CO)2)2,Fe(CO)5,Cp2TiMe2.
Cùng xứng vị hóa học có giao cái hóa học chi nhánh như:
- Sinh vật hoá học vô cơ—— trong đó phối hợp vật xứng thể tồn tại với trong giới tự nhiên, thường vìAxit aminSườn liên cùngCoenzyme,NhưPorphyria.Ví dụ bao gồmHuyết hồng tố.
- Nguyên tử thốc hóa học—— dùng kim loại nguyên tử làm xứng thể, nhưRu3(CO)12.
Kết cấu[Biên tập]
Cấu hình[Biên tập]
Xứng vị hoá chất cấu hình từXứng vị sốSở quyết định, cũng chính là hoá chất trung tâm nguyên tử chung quanh xứng vị nguyên tử cái số. Xứng vị số cùng kim loại ly tử cùng xứng thể bán kính, điện tích số cùngĐiện tử cấu hìnhCó quan hệ, giống nhau ở 2-9 chi gian,Lan hệ nguyên tốCùngA hệ nguyên tốPhối hợp vật trung bình sẽ xuất hiện 10 trở lên xứng vị số.
Đem quay chung quanh trung tâm nguyên tử xứng vị nguyên tử coi như điểm, lấy sợi dây gắn kết tiếp các điểm, phải đến xứng vị hình đa diện. Xứng vị số cùng phối hợp vật cấu hình quan hệ liệt tại hạ biểu:[7]
| Xứng vị số | Cấu hình | Đồ hình | 3D | Ví dụ thực tế |
|---|---|---|---|---|
| 2 | Thẳng tắp hình D∞h |
HgCl2,Ag(NH3)2+,[Au(CN)2]− | ||
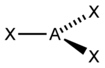
| 3 | Mặt bằng hình tam giác |
 |

|
HgI3−,Pt(PPh3)3,Fe[N(Si(CH3)3)2]3 |
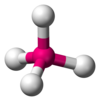
| 4 | Tứ phía thể |
 |
|
Ni(CO)4,MnO4−,SnCl4 |
| Mặt bằng hình vuông |
 |

|
PtCl42−,Ni(CN)42− | |
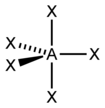
| 5 | Tam giác song trùy |
 |

|
Fe(CO)5,CdCl53− |
| Tứ phương trùy |
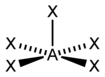 |

|
[InCl5]2−,SbF52− | |
| 6 | Khối bát diện |  |
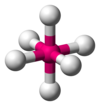
|
[Ti(H2O)6]3+,[Co(en)3]3+,[Cu(NH3)6]2+,[Fe(CN)6]3- |
| 7 | Ngũ giác song trùy |
 |
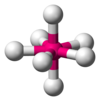
|
[ZrF7]2−,[UO2F5]3− |
Năm xứng vị trung, thường thường đề cập đếnTam giác song trùyCùngTứ phương trùyHai loại cấu hình lẫn nhau biến, bởi vậy, rất lớn một bộ phận năm xứng vị hoá chất kết cấu là xen vào này hai cái kết cấu chi gian một loại trung gian kết cấu. Sáu xứng vị hoá chất trừ cực kỳ thường thấyKhối bát diệnNgoại, cũng có khả năng làTam giác hình lăng trụKết cấu, tỷ như đơn hạch phối hợp vật [Re(S2C2Ph2)3] tức thuộc về này một loại. Bảy xứng vị trung, phối hợp vật còn có thể là đơn mũ khối bát diện hoặc đơn mũ tam giác hình lăng trụ thể kết cấu.
Càng cao xứng vị số hoá chất trung, tám xứng vị có thể là tứ phươngPhản hình lăng trụ thể,Mười hai mặt thể,Hình lập phương,Song mũ tam giác hình lăng trụ thể hoặc sáu giác song trùy kết cấu; chín xứng vị có thể là tam mũ tam giác hình lăng trụ thể hoặc đơn mũ tứ phương phản hình lăng trụ thể kết cấu; mười xứng vị có thể là song mũ tứ phương phản hình lăng trụ thể hoặc song mũ mười hai mặt thể kết cấu; mười một xứng vị hoá chất rất ít, có thể là đơn mũ ngũ giác hình lăng trụ thể hoặc đơn mũ ngũ giác phản hình lăng trụ thể; mười hai xứng vị như [Ce(NO3)6]3−,Vì lý tưởngHai mươi mặt thể;Mười bốn xứng vị vì song mũ sáu giác phản hình lăng trụ thể. Lại cao xứng vị số phi thường hiếm thấy, như gần nhất nghiên cứu PbHe152+,Nên ly tử trungChìXứng vị số ít nhất vì 15.[8]
Trở lên chỉ là phối hợp vật cấu hình lý tưởng tình huống. Thực tế trung phối hợp vật kết cấu hội nghị thường kỳ phát sinh cơ biến, nguyên nhân có thể làVị trở hiệu ứng,Điện tử hiệu ứng( tham kiếnKhương - Taylor hiệu ứng) hoặc xứng thể chủng loại duyên cớ chờ.
Dị cấu hiện tượng[Biên tập]
Dị cấuHiện tượng là phối hợp vật có tầm quan trọng chất chi nhất. Nó không chỉ có ảnh hưởng phối hợp vậtVật lýCùngTính chất hoá học,Hơn nữa cùng với ổn định tính, phản ứng tính cùng sinh vật hoạt tính cũng có chặt chẽ quan hệ. Quan trọng phối hợp vật dị cấu hiện tượng bao gồmLập thể dị cấuCùngKết cấu dị cấu.
Lập thể dị cấu[Biên tập]
Lập thể dị cấuLàCông thức hoá họcCùng nguyên tử sắp hàng thứ tự đều tương đồng, chỉ nguyên tử ở không gian sắp hàng bất đồng dị cấu hiện tượng. Lập thể dị cấu chủ yếu chia làmBao nhiêu dị cấuCùngQuang học dị cấu.
- Bao nhiêu dị cấu
Bao nhiêu dị cấuLà tạo thành tương đồng phối hợp vật bất đồng xứng thể ở không gian bao nhiêu sắp hàng bất đồng mà trí dị cấu hiện tượng, chủ yếu xuất hiện ở xứng vị số vì 4Mặt bằng hình vuôngCùng xứng vị số vì 6Khối bát diệnKết cấu trung, lấyThuận thức - phản thức dị cấuThể cùngMặt thức - kinh thức dị cấuThể hình thức tồn tại.
Từ không gian quan hệ thượng suy xét, thuận thức (cis- ) là chỉ tương đồng xứng thể ở vào lân vị, phản thức (trans- ) là chỉ tương đồng xứng thể ở vào đối âm. Khối bát diện [MA3B3] hai loại dị cấu thể trung, mặt thức (fac- ) hoặc thuận - thuận thức chỉ 3 cái A cùng 3 cái B các chiếm khối bát diện tam giác mặtĐỉnh điểm,Kinh thức (mer- ) hoặc thuận - phản thức là chỉ 3 cái A cùng 3 cái B ở khối bát diệnNgoại tiếp cầuKinh tuyếnThượng song song. Thấy hạ đồ:
-
cis-[CoCl2(NH3)4]+ -
trans-[CoCl2(NH3)4]+ -
fac-[CoCl3(NH3)3] -
mer-[CoCl3(NH3)3]
Không đối xứngSong răngXứng thể mặt bằng hình vuông phối hợp vật [M(AB)2] cũng có khả năng có bao nhiêu dị cấu hiện tượng, kết cấu cùng loại với mặt trên thuận bạc, thấy hạ đồ:
 |
 |
Nhiều hạch phối hợp vật cũng có bao nhiêu dị cấu hiện tượng. Tỷ như,Pt(II) song hạch phối hợp vật [Pt2(PPr3)2(SEt)2Cl2] thuận phản dị cấu thể đều đã chế đến, thả nhiệt độ phòng hạ nàyBenzenDung dịch đều là ổn định. Nhưng phản thức ở nhiệt hoặc lãnh benzen dung dịch trung gia nhập ngân lượngTam Bính cơ 膦LàmChất xúc tácLà có thể hoàn toàn chuyển biến vì thuận thức.[7]
- Quang học dị cấu
Quang học dị cấuLà lập thể dị cấu một loại khác hình thức, hai loại quang học dị cấu thể hội sửMặt bằng ánh sáng phân cựcPhát sinh ngang nhau nhưng bất đồng phương hướng độ lệch, bởi vậy lại xưng toàn quang dị cấu hoặc đối ánh dị cấu. Đại đa số phối hợp vật ở dung dịch trung đều sẽ dần dần mất điTính chuyển hướng ánh sáng,Này một quá trình xưng làTiêu toàn tác dụng.Căn cứ cụ thể tình huống bất đồng, tiêu toànCơ chếCó thể là phần tử thỉnh thoảng phần tử nội.
Đơn giản nhất phối hợp vật quang học dị cấu thể vì tứ phía hình thể, trung tâm nguyên tử cùng bốn cái bất đồng gốc tương liên, phần tử không thể cùng cảnh trong gương trùng hợp. Tỷ như [BeII(C6H5COCHCOCH3)2]. Mà đối với khối bát diện cấu hình phối hợp vật mà nói, quang học dị cấu chủ yếu phát sinh ở dưới vài loại dưới tình huống:
- [M(AA)3] hình, như tam -(Axit oxalic căn) hợpCác(III), [Co{(OH)2Co(NH3)4}3]Cl6( cái thứ nhất chế đến có tính chuyển hướng ánh sáng thả không chứa than hoá chất —Hexol).
- [M(AA)2X2] hình, như [Rh(en)2Cl2]+.
- [M(AB)3] hình, như [Co(gly)3].
- [M(AA)B2X2] hình, như [Co(en)(NH3)2Cl2]+.
- Đề cập nhiều răng xứng thể, như [Co(edta)]−.
-
Λ-[Fe(ox)3]3− -
Δ-[Fe(ox)3]3− -
Λ-cis-[CoCl2(en)2]+ -
Δ-cis-[CoCl2(en)2]+
Kết cấu dị cấu[Biên tập]
Kết cấu dị cấuLàCông thức hoá họcTương đồng, nhưng nguyên tử sắp hàng thứ tự bất đồng dị cấu thể, chủ yếu nhưng chia làm dưới mấy loại:

- Kiện hợp dị cấu:Xứng thể thông qua bất đồng xứng vị nguyên tử cùng trung tâm nguyên tử xứng vị. Xứng thể gọi cái nào cũng được xứng thể, này loại xứng thể đựng hai cái trở lên hàmCô đối điện tửNguyên tử, nhưng phân biệt cùng trung tâm nguyên tử xứng vị. Thường thấy cái nào cũng được xứng thể có:NO2−,SCN−CùngCN−.
- Cấu hình dị cấu:Phối hợp vật có thể áp dụng một loại trở lên cấu hình. Tỷ như [NiCl2(Ph2PCH2Ph)2] nhưng phân biệt trình tứ phía thể hoà bình mặt tứ giác cấu hình. Thường thấy cấu hình dị cấu có năm xứng vị hoá chấtTam giác song trùyCùngTứ phương trùyCấu hình chi gian dị cấu, cùng với tám xứng vị hoá chấtMười hai mặt thểCùngTứ phương phản hình lăng trụ thểCấu hình chi gian dị cấu.
- Xứng vị thể dị cấu:Lẫn nhau vìCùng phân dị cấu thểXứng thể sở hình thành cùng loại phối hợp vật, như 1,3- nhị gốc amin Bính hoàn cùng 1,2- nhịGốc aminBính hoànPhân biệt hình thành coban phối hợp vật [Co(H2N-CH2-CH2-CH2-NH2)Cl2], [Co(H2N-CH2-CH(-NH2)-CH3)Cl2].
- Ly tử dị cấu:Phối hợp vật có tương đồng công thức phân tử nhưng bất đồng xứng vị i-on âm, bởi vậy thủy dung dịch trung sinh ra ly tử bất đồng, như [Co(NH3)5SO4]Br cùng [Co(NH3)5Br]SO4.
- Dung môi hợp dị cấu:Phối hợp vật trung thủy vị trí vị trí bất đồng, có nội giới cùng ngoại giới sai biệt, tỷ như [Co(H2O)6]Cl3Cùng [Cr(H2O)5Cl]Cl·H2O.
- Xứng vị dị cấu:Dương ly tửCùngI-on âmĐều là xứng ly tử, thả xứng thể có thể cho nhau trao đổi thành phần. Ví dụ có: [Co(NH3)6][Cr(CN)6] cùng [Cr(NH3)6][Co(CN)6], [Cr(NH3)6][Cr(SCN)6] cùng [Cr(SCN)2(NH3)4][Cr(SCN)4(NH3)2], cùng với [PtII(NH3)4][PtIVCl6] cùng PtIV(NH3)4Cl2][PtIICl4].
- Tụ hợp dị cấu:Là xứng vị dị cấu một loại, dùng để tỏ vẻ phối hợp vậtTương đối phần tử chất lượngThượng bội số quan hệ, cùngTụ hợp phản ứngTrung “Tụ hợp” cũng không cùng loại. Tỷ như, [Co(NH3)6][Co(NO2)6] nhưng coi như [Co(NH3)3(NO2)3]Nhị tụ thể.
Lý luận[Biên tập]
Xứng vị hoá chấtLiên kết hoá họcLý luận, chủ yếu nghiên cứu trung tâm nguyên tử cùng xứng thể chi gian kết hợp lực bản tính, dùng để thuyết minh phối hợp vật vật lý cậpTính chất hoá học,Như từ tính, ổn định tính, phản ứng tính, xứng vị số cùng bao nhiêu cấu hình chờ. Phối hợp vật lý luận lúc đầu vớiTĩnh điệnLý luận. Rồi sau đó tây quý uy khắc cùngBào lâmĐưa ra xứng vịCộng giớiMô hình, cũng chính là ứng dụng phối hợp vật trungGiới kiện lý luận,Thống trị này một lĩnh vực hơn hai mươi năm, có thể tương đối tốt mà giải thích xứng vị số, bao nhiêu cấu hình, từ tính chờ một ít tính chất, nhưng đối phối hợp vật nhan sắc cùng quang phổ lại bất lực.
Giới kiện lý luận cho rằng, xứng thể cung cấpCô đối điện tửTiến vào trung tâm ly tử khôngNguyên tử quỹ đạo,Khiến cho xứng thể cùng trung tâm ly tử cùng chung này hai cái điện tử. Xứng vị kiện hình thành đã trải qua ba cái quá trình: ( kích phát ), tạp hóa cùng thành kiện, trong đó tạp hóa cũng xưngQuỹ đạo tạp hóa,Là năng lượng gần nguyên tử quỹ đạoTuyến tính tổ hợpTrở thành chờ số lượng thả năng lượngGiản cũngTạp hóa quỹ đạo quá trình. Bởi vậy còn nhưng diễn sinh xuất ngoại quỹ / nội quỹ hình phối hợp vật khái niệm, do đó thông qua phán đoán phối hợp vật điện tử cấu hình cập tạp hóa loại hình, liền có thể đến ra phối hợp vật từ tính,Oxy hoá hoàn nguyên phản ứngTính chất cùng với bao nhiêu cấu hình. Đối với rất nhiều kinh điển phối hợp vật tới nói, giới kiện lý luận đến ra kết quả vẫn là tương đối gần sát sự thật.
Trừ bỏ giới kiện lý luận ở ngoài, rồi sau đó phát triểnTinh thể tràng lý luậnCùngLigand field theory lý luậnCũng là tương đối quan trọng phối hợp vật lý luận.
Tinh thể tràng lý luậnĐem xứng thể coi như điểm điện tích, cũng đem xứng vị kiện làm nhưLy tử kiệnXử lý, nhưng coi như là tĩnh điện lý luận kéo dài. Hơn nữa, nó lấy bất đồng bao nhiêu cấu hình trung, xứng thể đối bất đồng không gian lấy hướngdQuỹ đạo tác dụng làm thiết nhập điểm, đến ra bất đồng lấy hướngdQuỹ đạo sẽ phát sinh mức năng lượng phân liệt, cũng thành lập khởi phân liệt có thể cập tinh thể tràng ổn định hóa có thể khái niệm, lấy phỏng đoán phối hợp vật điện tử hình thể cập ổn định tính. Tinh thể tràng lý luận có thể tốt lắm giải thích phối hợp vật nhan sắc,Nhiệt lực họcTính chất cùng phối hợp vật cơ biến chờ hiện tượng, nhưng không thể hợp lý giải thích xứng thểQuang phổ hóa học danh sách,Cũng không thể tốt lắm ứng dụng với đặc thù cao / giá thấp phối hợp vật,Có nhân phối hợp vật,Cacbonyl phối hợp vậtCùngAnken phối hợp vật.
Ligand field theory lý luậnKết hợpPhần tử quỹ đạo lý luậnCùngTinh thể tràng lý luận.Nó tại lý luận thượng càng thêm nghiêm cẩn, nhưng mà định lượng tính toán tắc thực khó khăn, tính toán trong quá trình không thể không tiến cử xấp xỉ xử lý, cho nên cũng chỉ có thể được đến xấp xỉ kết quả.
Phản ứng[Biên tập]
Xứng thể trao đổi phản ứng[Biên tập]
Xứng vị hoá chất trung xứng thể nhưng bị cái khác xứng thể sởThay thế được,Xưng làXứng thể trao đổi phản ứng,Giống nhau phản ứng cơ chế vìThân hạch thay thế được phản ứng.Lấy khối bát diện phối hợp vật vì lệ, này loại phản ứng công thức chung vì:
Thức trung X vì bị thay thế được xứng thể, thông thường gọi là rời đi gốc; Y vì thay thế được tập đoàn, thông thường xưng là tiến vào gốc. Loại này xứng thể trao đổi phản ứng tốc độ kém rất lớn, có chút phản ứng ở 10−10Giây nội liền nhưng hoàn thành, mà có phản ứng tắc yêu cầu mấy tháng. Đối với hoạt tính sai biệt có một người vì quy định, cho rằng ở độ dày ước vì 0.1M,Độ ấm 25 °C khi,Thời kỳ bán phân rãLớn hơn một phút phối hợp vật thuộc về cái gọi là “Tính trơ” phối hợp vật, phản chi tắc xưng là hoạt tính phối hợp vật.
Giới kiện lý luận cùngLigand field theory lý luậnĐều đối loại này phản ứng tốc độ sai biệt làm giải thích, giống nhau tồn tại dưới quy luật:[7]
- Trung tâm kim loại ly tử điện tích gia tăng, sẽ sử phản ứng tốc độ hạ thấp;
- Trung tâm ly tử vì,,,,Cấu hình,Cao sự quay tròn,,Cấu hình cùng cao sự quay trònCấu hình phối hợp vật, đối với xứng thể trao đổi phản ứng đều là hoạt tính;
- Trung tâm ly tử vì,Cấu hình, hoặc thấp sự quay tròn,,Cấu hình khi, đối với xứng thể trao đổi phản ứng là tính trơ.
Ngoài ra, phản ứng tốc độ còn cùngDung môi,Xứng thể chủng loại cùng sắp hàng có rất lớn quan hệ.
Xứng vị phản ứng nhưng coi cùngLouis toan kiềm lý luậnTrungToan kiềm phản ứng:Kim loại ly tử vìToanCung cấp không quỹ đạo, xứng thể cung cấp điện tử đối vìKiềm,Quá độ kim loạiCùng xứng thể phản ứng thường cùng vớiNhan sắcBiến hóa. Tỷ như, đem HCl gia nhập [Cu(NH3)4]2+Y tự sinh ra [Cu(H2O)4]2+( màu lam nhạt ), [CuCl(H2O)3]+,[CuCl2(H2O)2], [CuCl3(H2O)]−,[CuCl4]2−,[Cu(NH3)4]2+( màu xanh biển ); lại như, đem quá liềuDung dịch amoniacGia nhập [Cu(H2O)4]2+Nhan sắc lập tức từ màu lam nhạt chuyển biến thành màu xanh biển:
- ( lam nhạt )( thâm lam )
Oxy hoá hoàn nguyên phản ứng[Biên tập]
Xứng vị hoá chấtOxy hoá hoàn nguyên phản ứngBao hàm hai loại loại hình, một loại là trung tâm nguyên tử cùng xứng thể chi gian oxy hoá hoàn nguyên phản ứng, một loại khác còn lại là hai cái phối hợp vật chi gian oxy hoá hoàn nguyên phản ứng. Người sau lại có thể chia làm hai loại:
- Điện tử dời đi cơ chế, ngoại tầng phản ứng cơ chế: Hai cái phản ứng vật đệ nhất xứng vị tầng đều bảo trì bất biến. Phản ứng tốc độ chủ yếu cùng phản ứng vật kết cấu cùngĐiện tử sự quay trònThái có quan hệ, đựngπCộng ách hệ thống (conjugated system) xứng thể, nhưLiên Pyridin,CN−Phối hợp vật phản ứng tốc độ thường thường khá nhanh. Ngoài ra, kiều liên xứng thể cũng có thể truyền lại điện tử, nhưng giống nhau không bằng trực tiếpĐiện tử dời điPhản ứng hữu hiệu.
- Kiều thức cơ chế, nội tầng phản ứng cơ chế: Hai cái kim loại nguyên tử đồng thời liên tiếp ở một cái kiều liên xứng thể thượng, tạo thànhQuá độ thái.
Phản ứng này đây ngoại tầng cơ chế tiến hành, vẫn là trong vòng tầng cơ chế tiến hành, cùng phối hợp vật kết cấu có quan hệ. Đối xứng thể trao đổi phản ứng trình tính trơ, không có kiều liên xứng thể hoặc điện tử dời điHoạt hoá có thểRất thấp phối hợp vật, chúng nó cơ chế bên ngoài tầng cơ chế là chủ. Đối xứng thể trao đổi phản ứng hoạt tính phối hợp vật chủ muốn phát sinh kiều thức cơ chế, kiều thức cơ chế sở cần khắc phục có thể lũy so ngoại tầng phản ứng cơ chế thấp rất nhiều, bởi vì kiều liên xứng thể truyền lại điện tử hạ thấp điện tử xuyên thấu xứng bên ngoài cơ thể tầng cùng thủy hóa tầng năng lượng.
Oxy hoá hoàn nguyên phản ứng trung còn có hai loại phản ứng so đặc thù:
- Song điện tử dời đi phản ứng: Phản ứng trungOxy hoá tháiThay đổi vì ±2, cơ chế vì kiều thức cơ chế khả năng tính trọng đại.
- Phi bổ sung cho nhau phản ứng:Oxy hoá tềCùngHoàn nguyên tềGiới thái thay đổi không bằng nhau, giống nhau phản ứng cơ chế phân vài bước tiến hành.
Henry · đào bốVì phối hợp vật oxy hoá hoàn nguyên phản ứng nghiên cứu làm rất nhiều cống hiến, cũng bởi vậy đạt được 1983 nămNobel hóa học thưởng.
Ứng dụng[Biên tập]
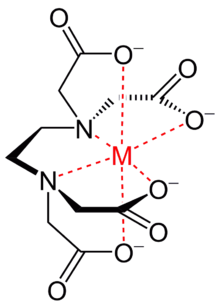
Xứng vị hoá chất ứng dụng bao gồm:
Phân tích hóa học trung, phối hợp vật nhưng dùng cho:
- Ly tử chia lìa: Thông qua sinh thành phối hợp vật tới thay đổi vật chấtĐộ hoà tan,Do đó cùng với nó ly tử chia lìa. Tỷ như lấy dung dịch amoniac cùngAgCl,Hg2Cl2CùngPbCl2Phản ứng tới chia lìa đệ nhất tộc dương ly tử:
- Cùng với lợi dụngAmonia phối hợp vậtSinh thành sửZn2+Tiến vào dung dịch[9]:
- Kim loại ly tửChuẩn độ:Tỷ như, định lượng trắc định dung dịch trung Fe3+Hàm lượng khi,Chỉ thị tềVì màu đỏ thẫm [Fe(phen)3]2+.
- Che đậy quấy nhiễu ví dụ: Dùng sinh thành phối hợp vật tới tiêu trừ phân tích thực nghiệm trung sẽ đối kết quả tạo thành quấy nhiễu nhân tố.So sắc phápTrắc định Co2+Lúc ấy đã chịu Fe3+Quấy nhiễu, nhưng gia nhậpF−Cùng Fe3+Sinh thành vô sắc ổn định xứng ly tử [FeF6]3−,Lấy che đậy Fe3+:
Công nghiệp sinh sản trung:
- Xứng vị thôi hóa:Thôi hóaPhản ứng cơ chế hội nghị thường kỳ đề cập đến xứng vị hoá chất trung gian thể, tỷ như hợp thànhAmoniaCông nghiệp có íchDấm chua nhị Amonia hợp đồngTrừ bỏCarbon monoxit,Hữu cơ kim loại chất xúc tác thôi hóaAnkenTụ hợp phản ứng hoặc khó hoà hợp thôi hóa phản ứng, cùng với không đối xứng thôi hóa vớiDược vậtChế bị.
- ChếKính:Lấy bạc Amonia dung dịch vì nguyên liệu, lợi dụngPhản ứng tráng gương,Ở pha lê mặt sau mạ lên một tầng ánh sáng bạc đồ tầng[10].
- Lấy ra kim loại: Tỷ nhưXyanogen hóa phápĐềKimBước đi trung, bởi vì sinh thành ổn định xứng ly tử [Au(CN)2]−,Khiến cho không hoạt bát kim tiến vào dung dịch trung:
- Cũng có thể lợi dụng rất nhiều cacbonyl phối hợp vật nhiệt phân giải nhắc tới thuần kim loại, tỷ như mông đức pháp trung, Nickel thuần hóa lợi dụngBốn cacbonyl NickelSinh thành cùng phân giảiPhản ứng thuận nghịch:[11]
- Tài liệu tiên phong vật: Oxy hoá nhôm lốm đốm cậpThân hóa gia(GaAs) lá mỏng chờ hợp thành.
- Nước cứng mềm hoá
Sinh vật họcTrung, rất nhiều sinh vật phần tử đều là phối hợp vật, hơn nữa hàmThiếtHuyết sắc tốCùngDưỡng khíCùngCarbon monoxitKết hợp, rất nhiềuMôiCập hàmMagieDiệp lục tốBình thường vận tác cũng đều không rời đi phối hợp vật cơ chế. Thường dùngUng thưTrị liệu dược vậtThuận bạc,Tứccis-[PtCl2(NH3)2], có thể ức chế ung thư tế bào DNA phục chế quá trình, đựng mặt bằng hình vuông phối hợp vật cấu hình.Ất nhị án bốn Ất toan,Chanh chua Natri,2,3- nhị khưu cơ đinh nhị toanChờThuốc giải độcNhưng dùng cho kim loại nặng giải độc cơ chế, thường thường là chúng nó nhưng cùng kim loại nặng ly tử phối hợp, làm này chuyển hóa vì độc tính rất nhỏ xứng vị hoá chất, do đó đạt tới giải độc mục đích.
Mệnh danh pháp[Biên tập]
| Xứng thể | Làm xứng thể khi tên |
|---|---|
| CO | Cacbonyl |
| OH− | Thưởng ( cơ ) |
| F− | Flo |
| PH3 | 膦 |
| NO2− | Tiêu cơ (-N-) Á axit nitric căn (-O-) |
| N2 | Song nitro |
| H2 | Song hydro |
| H− | Hydro |
Ở mệnh danh xứng vị hoá chất khi, giống nhau tuần hoànTiếng Trung IUPAC mệnh danh pháp,Mệnh danh quy luật có:[12][13][14]
- Ly tử phối hợp vật lấy muối hình thức xử lý. Mệnh danh xứng vị đơn nguyên khi, xứng thể ở phía trước, bất đồng xứng thể chi gian lấy viên điểm phân cách, thả cuối cùng một cái xứng thể cùng trung tâm nguyên tử tên gian muốn thêm “Hợp” tự. Xứng thể tên liệt bên phải biểu, này trình tự chủ yếu tuần hoàn “Trước vô cơ sau hữu cơ” cùng “Trước i-on âm sau trung tính phần tử” hai điều. Xứng thể trước muốn hơn nữa xứng thể cái số, lúc cần thiết thêm viên dấu móc đem xứng thể tên quát lên, để tránh miễn nghĩa khác. Trung tâm nguyên tử cần ở sau đó đánh dấuOxy hoá số,Lấy mang viên dấu móc chữ số La Mã tỏ vẻ. Chính ly tử phối hợp vật xưngClo hóa vật,Axit nitric muối,Axít muốiChờ, i-on âm phối hợp vật tắc xưng mỗ toan Kali / Natri hoặc mỗ toan.
- Kiều liên xứng thểTrước muốn thêm chúμ;ηnTắc tỏ vẻ xứng thể có n cái nguyên tử cùng trung tâm nguyên tử kiện kết ( n tức vì xứng thểHa phổ thác số). Đối với khả năng sinh raKiện hợp dị cấuPhối hợp vật, cần ở xứng thể sau ghi chú rõ xứng vị nguyên tử.
Kể trên chỉ là một ít đơn giản quy tắc, càng nhiều quy tắc thỉnh tham khảo:
- Trung Quốc hóa học sẽ: 《 hoá học vô cơ mệnh danh nguyên tắc 》(1980), khoa học nhà xuất bản, Bắc Kinh, 1982.
- 《 anh hán hóa học hóa chất từ ngữ 》, khoa học nhà xuất bản (1980).
- IUPAC, "Nomenclature of Inorganic Chemistry", 2nd Ed., Butterworth, "Coordination Compounds", 39-85 (1970).
Dưới là một ít ví dụ:
| Phối hợp vật | Mệnh danh |
|---|---|
| [NiCl4]2− | Bốn Clo hợp Nickel toan (II) căn ly tử |
| [Cu(NH3)Cl5]3− | Năm Clo · một Amonia hợp đồng toan (II) căn ly tử |
| [Cd(en)2(CN)2] | Nhị xyanogen · nhị ( Ất nhị án ) hợp cách (II) |
| [Co(NH3)5Cl]SO4 | Axít một Clo · năm Amonia hợp coban (III) |
| Fe2Cl6(Clo hóa thiếtNhị tụ thể ) | Bốn Clo nhị -μ- Clo hợp nhị thiết (III) |
| (NH4)3[Cr(NCS)6] | Sáu ( lưu xyanogen gốc a-xít )-N- hợp các toan (III) Amoni |
Tham kiến[Biên tập]
- Bao hợp vật
- Hữu cơ kim loại hóa học,Hoá học vô cơ
- Hoá học vô cơ mệnh danh pháp
- Đều xứng vật
- Tự xứng vị phản ứng
Trích dẫn[Biên tập]
- ^Lawrance, Geoffrey A. Introduction to Coordination Chemistry. Wiley. 2010.ISBN9780470687123.doi:10.1002/9780470687123.
- ^Quốc tế thuần hóa học cùng ứng dụng hóa học liên hợp sẽ,Hóa học thuật ngữ tóm tắt,Đệ nhị bản. ( kim da thư ) (1997). Tại tuyến chỉnh lý bản: (2006–) "complex".doi:10.1351/goldbook.C01203
- ^Quốc tế thuần hóa học cùng ứng dụng hóa học liên hợp sẽ,Hóa học thuật ngữ tóm tắt,Đệ nhị bản. ( kim da thư ) (1997). Tại tuyến chỉnh lý bản: (2006–) "coordination entity".doi:10.1351/goldbook.C01330
- ^Lưu trữ phó bản.[2023-06-20].( nguyên thủy nội dungLưu trữVới 2023-06-20 ).
- ^Greenwood, Norman N.; Earnshaw, Alan (1997). Chemistry of the Elements (2nd ed.). Butterworth-Heinemann.ISBN 978-0-08-037941-8.
- ^Trích dẫn sai lầm: Không có vì danh vì
#1Tham khảo văn hiến cung cấp nội dung - ^7.07.17.2Mang an bang chờ. 《 xứng vị hóa học 》, 《 hoá học vô cơ bộ sách 》 thứ mười hai cuốn. Bắc Kinh: Khoa học nhà xuất bản, 1987 năm 10 nguyệt.
- ^The Search for the Species with the Highest Coordination NumberAndreas Hermann, Matthias Lein, and Peter SchwerdtfegerAngew. Chem. Int. Ed.2007,46, 2444 –2447doi:10.1002/anie.200604148
- ^Essmann, R. Influence of coordination on N-H...X- hydrogen bonds. Part 1. [Zn(NH3)4]Br2and [Zn(NH3)4]I2.Journal of Molecular Structure. 1995,356:201–6.Bibcode:1995JMoSt.356..201E.doi:10.1016/0022-2860(95)08957-W.
- ^Hart, M. Manual of scientific glassblowing. St. Helens, Merseyside [England]: British Society of Scientific Glassblowers. 1992.ISBN0-9518216-0-1.
- ^Mond L, Langer K, Quincke F (1890). "Action of carbon monoxide on nickel".Journal of the Chemical Society:749-753. doi:10.1039/CT8905700749(Giao diện lưu trữ sao lưu,Tồn vớiInternet hồ sơ quán).
- ^Trung Quốc hóa học sẽ: 《 hoá học vô cơ mệnh danh nguyên tắc 》(1980), khoa học nhà xuất bản, Bắc Kinh, 1982.
- ^《 anh hán hóa học hóa chất từ ngữ 》, khoa học nhà xuất bản (1980).
- ^IUPAC, "Nomenclature of Inorganic Chemistry", 2nd Ed., Butterworth, "Coordination Compounds", 39-85 (1970).”.
Tham khảo văn hiến[Biên tập]
- De Vito, D.; Weber, J.; Merbach, A. E.Calculated Volume and Energy Profiles for Water Exchange on t2g6Rhodium(III) and Iridium(III) Hexaaquaions: Conclusive Evidence for an IaMechanismInorganic Chemistry, 2005, Volume 43, pages 858-863.
- Zumdahl, Steven S.Chemical Principles,Fifth Edition. New York: Houghton Mifflin, 2005. 943-946, 957.
- Naming Coordination Compounds(Giao diện lưu trữ sao lưu,Tồn vớiInternet hồ sơ quán)
- Harris, D., Bertolucci, M.,Symmetry and Spectroscopy.1989 New York, Dover Publications
- F. Basolo and R. G. Pearson,Mechanisms of Inorganic Reactions (A Study of Metal Complexes in Solution).John Wiley and Sons, Inc. (1967).
- H. J. Emeleus Editor, "Inorganic Chemistry; Series One, vol. 9, Reaction Mechanisms in Inorganic Chemistry", Butterworth, (1972).
Phần ngoài liên tiếp[Biên tập]
- IUPAC xứng vị hoá chất mệnh danh pháp(Giao diện lưu trữ sao lưu,Tồn vớiInternet hồ sơ quán)( tiếng Anh )
- Xứng vị hoá chất nhan sắc(Giao diện lưu trữ sao lưu,Tồn vớiInternet hồ sơ quán)( tiếng Anh )
| ||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||
|






![cis-[CoCl2(NH3)4]+](https://upload.wikimedia.org/wikipedia/commons/thumb/b/be/Cis-dichlorotetraamminecobalt%28III%29.png/120px-Cis-dichlorotetraamminecobalt%28III%29.png)
![trans-[CoCl2(NH3)4]+](https://upload.wikimedia.org/wikipedia/commons/thumb/5/56/Trans-dichlorotetraamminecobalt%28III%29.png/120px-Trans-dichlorotetraamminecobalt%28III%29.png)
![fac-[CoCl3(NH3)3]](https://upload.wikimedia.org/wikipedia/commons/thumb/6/69/Fac-trichlorotriamminecobalt%28III%29.png/109px-Fac-trichlorotriamminecobalt%28III%29.png)
![mer-[CoCl3(NH3)3]](https://upload.wikimedia.org/wikipedia/commons/thumb/5/54/Mer-trichlorotriamminecobalt%28III%29.png/120px-Mer-trichlorotriamminecobalt%28III%29.png)
![Λ-[Fe(ox)3]3−](https://upload.wikimedia.org/wikipedia/commons/thumb/d/df/Delta-tris%28oxalato%29ferrate%28III%29-3D-balls.png/110px-Delta-tris%28oxalato%29ferrate%28III%29-3D-balls.png)
![Δ-[Fe(ox)3]3−](https://upload.wikimedia.org/wikipedia/commons/thumb/6/6e/Lambda-tris%28oxalato%29ferrate%28III%29-3D-balls.png/111px-Lambda-tris%28oxalato%29ferrate%28III%29-3D-balls.png)
![Λ-cis-[CoCl2(en)2]+](https://upload.wikimedia.org/wikipedia/commons/thumb/1/12/Delta-cis-dichlorobis%28ethylenediamine%29cobalt%28III%29.png/78px-Delta-cis-dichlorobis%28ethylenediamine%29cobalt%28III%29.png)
![Δ-cis-[CoCl2(en)2]+](https://upload.wikimedia.org/wikipedia/commons/thumb/8/81/Lambda-cis-dichlorobis%28ethylenediamine%29cobalt%28III%29.png/78px-Lambda-cis-dichlorobis%28ethylenediamine%29cobalt%28III%29.png)













![{\displaystyle {\rm {[Cu(H_{2}O)_{4}]^{2+}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/42ba21537a7f36e76fa8de49e5b060c6e52962fe)
![{\displaystyle {\rm {+4NH_{3}\rightarrow [Cu(NH_{3})_{4}]^{2+}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/a09bab7f1d58e5fe5c46a8b91b2d45d268538641)


![{\displaystyle {\rm {Zn^{2+}+4NH_{3}\rightarrow [Zn(NH_{3})_{4}]^{2+}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9affafa84853f18177cb4a58b1a67eff70909e5d)
![{\displaystyle {\rm {Fe^{3+}+6F^{-}\rightarrow [FeF_{6}]^{3-}\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/9dcfbff12bedecfa784bb7a79aeaf7d95e625606)
![{\displaystyle {\rm {4Au+8NaCN+2H_{2}O+O_{2}\rightarrow 4Na[Au(CN)_{2}]+4NaOH\,}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/afe799cc709a02beb06c571b62be2241e4de0851)
