Germanium
Cho dù địa cầu mặt ngoài 鍺Phong độVỏ quả đất ẩn chứa lượng tương đối so cao,Nhưng bởi vì khoáng thạch trung rất ít đựng cao độ dày 鍺, cho nên nó ở hóa học sử thượng phát hiện đến tương đối trễ.Dmitri · Ivanovich · MendeleevỞ 1869 cuối năm theoNguyên tố bảng chu kỳVị trí, đoán trước đến 鍺 tồn tại cùng với các hạng thuộc tính, cũng đem nó gọieka-Tịch.Clemens · ôn khắc lặcVới 1886 năm ở một loại kêuLưu bạc 鍺 quặngHi hữu khoáng vật trung, trừ bỏ tìm được lưu cùng bạc ở ngoài, còn phát hiện một loại tân nguyên tố. Cứ việc loại này tân nguyên tố vẻ ngoài cùngThânCùngĐễCó điểm giống, nhưng là tân nguyên tố ở hoá chất trung hoá hợp so phù hợp khuê hạ nguyên tố đoán trước. Ôn khắc lặc lấy hắn quốc gia ——Nước ĐứcTiếng Latinh danh tới vì loại này nguyên tố mệnh danh.
鍺 là một loại quan trọngChất bán dẫnTài liệu, dùng với chế tạoBóng bán dẫnCập các loại điện tử trang bị. Chủ yếu đầu cuối ứng dụng vìSợi quang họcHệ thống cùng tia hồng ngoại quang học, cũng dùng vớiTụ hợp phản ứngChất xúc tác,Chế tạo điện tử linh kiện chủ chốt cùng năng lượng mặt trời điện lực chờ. Hiện tại, khai thác 鍺 dùng chủ yếu khoáng thạch làLóe kẽm quặng(KẽmChủ yếu khoáng thạch ), cũng có thể ởBạc,ChìCùngĐồngTrung, dùng thương nghiệp phương thức lấy ra 鍺. Một ít 鍺 hoá chất, nhưBốn Clo hóa 鍺( GeCl4) cùngGiáp Germanium hoàn( GeH4), sẽKích thíchĐôi mắt,Làn da,Phổi bộCùngYết hầu.
Phát hiện sử[Biên tập]
MendeleevVới 1869 năm phát biểu một phần tên là 《 nguyên tố hoá học chu kỳ luật 》 nghiên cứu báo cáo, giữa đoán trước nhiều loại không biết nguyên tố tồn tại, trong đó một loại bổ khuyết than trong tộcKhuêCậpTíchChi gian chỗ trống[5].Bởi vì nó ở bảng chu kỳ vị trí, Mendeleev đem nó mệnh danh làNghĩ khuê( Ekasilicon, Es ), cũng đem nàyNguyên tử lượngĐịnh vì 72.

1885 năm mùa hạ, ởSax sâm vương quốcFreiburgPhụ cận một cái quặng mỏ, phát hiện một loại tân khoáng vật. Bởi vì loại này khoáng vật hàm bạc lượng cao, cho nên bị mệnh danh làLưu bạc 鍺 quặng[b].Clemens · ôn khắc lặcKiểm nghiệm loại này khoáng vật, cũng với 1886 mùa màng công từ giữa tách ra một loại cùngĐễTương tự nguyên tố[6].Ở hắn phát biểu thành quả phía trước, hắn nguyên bản tính toán dùng hải vương tinh tới vì tân nguyên tố mệnh danh, bởi vì ở 1846 năm bị phát hiện hải vương tinh, toán học lý luận cũng đoán trước nó tồn tại[c].Nhưng mà, nã ( Neptunium ) tên này lúc ấy đã bị một khác nguyên tố chiếm dụng ( bất quá không phải hôm nay kêuNãCái loại này nguyên tố, nó đến 1940 năm mới bị phát hiện )[d],Bởi vậy ôn khắc lặc sửa dùng hắn tổ quốc —— nước ĐứcTiếng Latinh( germanium ) tới vì nguyên tố mệnh danh[6].Bởi vì 鍺 cùngThânCùngĐễGần, cho nên nó lúc ấy hay không nên xuất hiện ở bảng chu kỳ thượng vẫn bị chịu tranh luận, bất quá nó tính chất cùng Mendeleev nghĩ khuê rất giống, bởi vậy mới xác lập nó ở bảng chu kỳ đích xác thật vị trí[6][7]Ở phát hiện sau, Sax sâm quặng mỏ lại cho ôn khắc lặc 500 kg khoáng thạch, bởi vậy hắn có thể tiến hành kế tiếp nghiên cứu, cũng ở 1887 năm xác lập loại này tân nguyên tố tính chất hoá học[8][9][10].Hắn thông qua phân tích thuần bốn Clo hóa 鍺, đến ra 鍺 nguyên tử lượng vì 72.32, màĐức bố ngói bác đức lanTắc thông qua tương đối nên nguyên tố hỏa hoaQuang phổTuyến, đến ra 72.3[11].
Ôn khắc lặc lúc ấy thành công chế bị vài loại tân 鍺 hoá chất, bao gồm Flo hóa vật, Clo hóa vật, sunfua,Nhị oxy hoá 鍺CậpBốn Ất cơ 鍺,Mà bốn Ất cơ 鍺 còn lại là đệ nhất loại hữu cơ 鍺 hoàn[9].Có từ này đó hoá chất mà đến vật lý số liệu —— chúng nó phù hợp Mendeleev đoán trước ——鍺 phát hiện trở thành xác nhận MendeleevNguyên tố chu kỳQuan trọng chứng cứ. Hạ biểu tương đối đoán trước cùng ôn khắc lặc số liệu[9]:
| Đặc tính | Nghĩ khuê ( đoán trước ) | 鍺 |
|---|---|---|
| Nguyên tử chất lượng | 72 | 72.59 |
| Mật độ ( g/cm3) | 5.5 | 5.35 |
| Điểm nóng chảy ( ℃ ) | Cao | 947 |
| Nhan sắc | Màu xám | Màu xám |
| Oxy hoá giống loài loại | Nại hỏa( refractory ) nhị oxy hoá vật | Nại hỏa nhị oxy hoá vật |
| Oxy hoá vật mật độ ( g/cm3) | 4.7 | 4.7 |
| Oxy hoá vật tính chất | Nhược kiềm | Nhược kiềm |
| Clo hóa vật điểm nóng chảy | 100℃ dưới | 86℃ ( GeCl4) |
| Clo hóa vật mật độ ( g/cm3) | 1.9 | 1.9 |

Cho đến 1930 niên đại thời kì cuối, các nhà khoa học vẫn luôn cho rằng 鍺 chỉ là một loại dẫn điện tính kém kim loại[12].Bởi vì nó chất bán dẫn đặc tính đối điện tử thiết bị tới nói là phi thường có giá trị, cho nên đến 1945 năm 鍺 thành một loại có thể có lợi tài liệu. ỞThế chiến thứ haiTrong lúc 1941 năm, 鍺Nhị cực thểLiền bắt đầu thay thế được điện tử trang bị trungChân không quản[13][14].Nó đệ nhất hạng chủ yếu sử dụng vì chế tạoTiêu đặc cơ nhị cực thểTiếp điểm, nên nhị cực thể ở Thế chiến 2 trong lúc dùng vớiRadarTiếp thu[12].Đệ nhất loạiTịch 鍺Hợp kim ra đời với 1955 năm[15].Ở 1945 năm trước kia, 鍺 năm sản lượng chỉ có mấy trăm kg, nhưng tới rồi 1950 niên đại mạt, thế giới năm sản lượng cũng đã đạt tới 40 công tấn[16].
鍺Bóng bán dẫnỞ 1948 năm xuất hiện[17],Mở raTrạng thái cố định điện tửVô số ứng dụng chi môn[18].Từ 1950 năm đến 1970 niên đại sơ, cái này lĩnh vực vì 鍺 cung cấp tăng trưởng trung thị trường, nhưng lúc sau bóng bán dẫn,Nhị cực thểCùngMáy chỉnh lưuĐều bắt đầu chuyển dùng cao độ tinh khiếtKhuê[19].Khuê điện tử đặc tính so 鍺 ưu việt, nhưng là sở cần độ tinh khiết liền cao đến nhiều —— như vậy độ tinh khiết dùng thời trẻ thương nghiệp phương pháp thật sự không đạt được[20].
Cùng lúc đó,Sợi quang họcMạng lưới thông tin lạc, tia hồng ngoạiĐêm coiHệ thống cậpTụ hợp phản ứngChất xúc tácĐối 鍺 nhu cầu lượng đang ở cấp tốc tăng trưởng[16].Này đó đầu cuối ứng dụng đại biểu 2000 năm 鍺 dùng lượng 80%[19].Nước Mỹ chính phủ thậm chí đem 鍺 định vì chiến lược cập mấu chốt tài liệu, cũng bởi vậy với 1987 niên hạ lệnh quốc gia phòng ngự dự trữ trung tâm tồn nhập 132Công tấn鍺[16].Sinh sản 鍺 cùng khuê bất đồng chính là, khuê sản lượng chỉ chịu sức sản xuất hạn chế, mà 鍺 sản lượng tắc chịu khai thác nơi phát ra thiếu có hạn chế. Nguyên nhân chính là như thế, khuê ở 1998 năm giá cả vì mỗi kg 10 đôla dưới[16],Mà lúc ấy 鍺 giá cả đạt mỗi kg 1800 đôla[16].
Đặc tính[Biên tập]
ỞTiêu chuẩn trạng huốngHạ, 鍺 là một loại màu ngân bạchNửa kim loạiNguyên tố, ngạnh nhưng dễ toái[21].Loại này hình thức cấu thành một loạiCùng tố dị hình thể,Kỹ thuật thượng kêu α鍺, nó mang kim loại ánh sáng, kết cấu cùngKim cươngGiống nhau, vìKim cương lập phương tinh thể kết cấu[19].ĐươngÁp lựcCao với 120kPaKhi, sẽ hình thành một loại khác cùng tố dị hình thể, kêu β鍺, nó kết cấu cùng βTíchGiống nhau[22].CùngKhuê,Gia,鉍,ĐễCùngThủyGiống nhau, 鍺 ở nóng chảy thái thể rắn hóa khi ( tứcĐọng lại) sẽ bành trướng[22],Mà có loại này đặc tính vật chất cũng không nhiều.
鍺 là một loạiChất bán dẫn.DùngKhu nóng chảyKỹ thuật sinh sản ra chất bán dẫn dùng 鍺 tinh thể, này tạp chất hàm lượng chỉ có 10 tỷ phần có một[23],Bởi vậy loại này tinh thể là sử thượng nhất thuần tài liệu chi nhất[24].Đệ nhất loại ở cực cườngĐiện từ trườngHạ trở thànhChất siêu dẫnKim loại tài liệu, là một loại hàm 鍺,銠CùngUraniHợp kim, với 2005 năm bị phát hiện[25].
Đã biết thuần 鍺 có thể tự phát mà bài trừ phi thường trườngXoắn ốc vị sai,Kêu “鍺 cần”. Này đó tinh cần tăng trưởng, là so cũ 鍺 chế nhị cực thể cùng bóng bán dẫn hư rớt nguyên nhân chủ yếu, bởi vì tinh cần rất có thể sẽ cấu thànhĐường ngắn,Nhưng đường ngắn cùng không coi cuối cùng tiếp xúc đến vật chất mà định[25].
Tính chất hoá học[Biên tập]
Ở 250℃ khi, 鍺 sẽ thong thả mà oxy hoá thànhGeO2[26].鍺 không dung với hi toan cập kiềm, nhưng dung với nùngAxít,Cũng cùng nóng chảy kiềm phản ứng, sinh thành鍺 toan muối( GeO32-). 鍺 nhất thường xuất hiệnOxy hoá tháiLà +4, nhưng là đã biết nó ở không ít hoá chất trung oxy hoá thái vì +2[27].Mặt khác oxy hoá thái tắc thực hiếm thấy, tỷ như hoá chất Ge2Cl6Trung vì +3, cùng với ở oxy hoá vật mặt ngoài trắc đến +3 cùng +1 oxy hoá thái[28],Hoặc là鍺 hóa vậtTrung phụ oxy hoá thái, như làMg
2GeTrung -4. Nhiều loại hàm 鍺 âm tính thốc ly tử (Tân đặc nhĩLy tử ) đã bị chế bị ra tới, giữa bao gồm Ge42-,Ge94-,Ge92-Cập [(Ge9)2]6-,Trong đó một loại phương pháp là ởẤt nhị ánHoặcHuyệt mêThôi hóa hạ, từ trí với trạng thái dịchAmonia鍺 cùngKiềm kim loạiHợp kim trung tiến hành lấy ra[27][29].Này đó ly tử trung 鍺 oxy hoá thái đều không phải là số nguyên —— điểm này cùngOzone căn ly tửTrung oxy giống nhau.
Đã biết 鍺 cùng sở hữu hai loại oxy hoá vật:Nhị oxy hoá 鍺CùngMột oxy hoá 鍺[22].NungNhị lưu hoá 鍺( GeS2) sau nhưng đến nhị oxy hoá 鍺, nhị oxy hoá 鍺 là một loại màu trắng bột phấn, hơi dung với thủy, nhưng cùng kiềm phản ứng cũng sinh thành 鍺 toan muối[22].Đương nhị oxy hoá 鍺 cùng 鍺 kim loại ở cực nóng hạ phản ứng khi, sẽ sinh thành một oxy hoá 鍺[22].Nhị oxy hoá 鍺 ( và tương quan oxy hoá vật cập 鍺 toan muối ) có một loại thực không tầm thường đặc tính, chính là đối ánh sáng mắt thường nhìn thấy được có caoChiết xạ suất,Nhưng đồng thời đốiTia hồng ngoạiẨn hình[30][31].Mà鍺 toan 鉍Tắc bị dùng làmLóe thước khí( scintillator )[32].
鍺 còn có thể cùng với nóOxy tộc nguyên tốSinh thànhHai nguyên tố hoá chất,Tỷ như nhịSunfua( GeS2), nhịSelen hóa vật( GeSe2), một sunfua ( GeS ), một selen hóa vật ( GeSe ) cậpĐế hóa vật( GeTe )[27].ĐemHydro SulfuaKhí thể thông qua hàm Ge(IV) cường toan dung dịch khi, sẽ sinh thành màu trắng lắng đọng lại vật, tức nhị lưu hoá 鍺[27].Nhị lưu hoá 鍺 có thể tốt lắm dung với thủy,Hà tính NatriDung dịch cậpKiềm kim loạiSunfua dung dịch trung. Nhưng là, nó không dung với toan tính dung dịch, ôn khắc lặc chính là bằng vào cái này tính chất mới phát hiện 鍺[33].Đem nhị lưu hoá 鍺 trí vớiHydroLưu trung đun nóng, sẽ sinh thành một lưu hoá 鍺 ( GeS ), nóThăng hoaSau sẽ hình thành một vòng sắc ám nhưng cụ kim loại ánh sáng lá, nó hòa tan được với hà tính Natri dung dịch trung. Đem một lưu hoá 鍺, kiềm kim loại than toan muối cùng lưu cùng nhau đun nóng sau, sẽ sinh thành một loại 鍺 muối hoá chất, kêu lưu đại 鍺 toan muối[34].
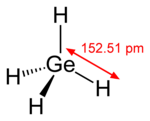
鍺 cùng sở hữu bốn loại đã biết bốnKho hóa vật.Ở bình thường trạng huống hạ bốn iốt hóa 鍺 ( GeI4) vì thể rắn, bốn Flo hóa 鍺 ( GeF4) vì khí thể, còn lại hai loại vìTính bốc hơiChất lỏng. Đem 鍺 cùng Clo một khối đun nóng, sẽ được đến một loại điểm sôi vì 83.1℃ vô sắc phát yên chất lỏng, tứcBốn Clo hóa 鍺[22].鍺 sở hữu bốn kho hóa vật đều dễ dàngThuỷ phân,Sinh thành mangTinh thể ngậm nướcNhị oxy hoá 鍺[22].Bốn Clo hóa 鍺 dùng với chế bị hữu cơ 鍺 hoá chất[27].Cùng bốn kho hóa vật tương phản chính là, toàn bộ bốn loại đã biết nhị kho hóa vật, toàn vì tụ hợp thể rắn[27].Mặt khác đã biết kho hóa vật còn bao gồm Ge2Cl6Cập GenCl2n+2[22].Còn có một loại kỳ lạ hoá chất Ge6Cl16,Trong đó đựng cùng loạiTân mậu hoànKết cấu Ge5Cl12[35].
Giáp 鍺 hoàn( GeH4) là một loại kết cấu cùngMetanGần hoá chất. Nhiều 鍺 hoàn ( tức cùngHoàn hydrocarbonTương tự 鍺 hoá chất ) công thức hoá học vì GenH2n+2,Hiện thời vẫn không có phát hiện n lớn hơn năm nhiều 鍺 hoàn[27].Tương đối vớiKhuê hoàn,鍺 hoàn tính bốc hơi cùngHoạt tínhĐều so thấp[27].GeH4Ở trạng thái dịchAmoniaTrung cùng kiềm kim loại phản ứng sau, sẽ sinh ra màu trắng MGeH3Tinh thể, giữa đựng GeH3−I-on âm[27].Hàm một, hai, ba cáiHalogenNguyên tử hydro kho hóa 鍺, toàn vì vô sắc hoạt tính chất lỏng[27].

Ôn khắc lặc với 1887 năm hợp thành ra đệ nhất loạiHữu cơ 鍺 hoá chất( organogermanium compound ); bốn Clo hóa 鍺 cùngNhị Ất cơ kẽmPhản ứng sinh thànhBốn Ất cơ 鍺( Ge(C2H5)4)[9].R4Ge hình ( trong đó R vì烴 cơ) hữu cơ 鍺 hoàn, nhưBốn nhóm methyl 鍺( Ge(CH3)4) cậpBốn Ất cơ 鍺,Là từ nhất tiện nghi 鍺 đi đầu vậtBốn Clo hóa 鍺Cập nhóm methylThân hạch tềPhản ứng mà thành. Hữu cơ 鍺 hydro hóa vật, nhưDị đinh cơ 鍺 hoàn( (CH3)2CHCH2GeH3) tính nguy hiểm tương đối thấp, bởi vậyChất bán dẫnCông nghiệp sẽ dùng chất lỏng hydro hóa vật tới thay thế được khí thểGiáp 鍺 hoàn.Đã biết 鍺 có không ít hoạt tínhTrung gian vật:鍺 đạiTự do cơ,鍺 hi ( cùngCarbeneGần ) cùng 鍺 khuyết ( cùngTạp tânGần )[36][37].Hữu cơ 鍺 hoá chất2- thoa Ất cơ 鍺 lần nửa oxy hoàn( 2-carboxyethylgermasesquioxane ), với 1970 năm bị phát hiện, đã từng có một đoạn thời gian bị dùng làmĐồ ăn bổ sung tề,Lúc ấy cho rằng nó khả năng đối u có hiệu quả trị liệu[38].
Chất đồng vị[Biên tập]
鍺 cùng sở hữu năm loại thiên nhiên tồn tạiChất đồng vị:70Ge,72Ge,73Ge,74Ge cùng76Ge. Giữa,76Ge mang mỏng manhTính phóng xạ,NàySuy biến hình thứcVìSong β suy biến,Thời kỳ bán phân rãVì 1.58 × 1021Năm.74Ge là nhất thường thấy chất đồng vị,Phong độƯớc vì 36%.76Ge tự nhiên phong độ là thấp nhất, ước vì 7%[39].Đương72Ge bị α hạt oanh kích khi, sẽ sinh ra ổn định77Se,Cũng ở trong quá trình phóng xuất ra cao năng lượngĐiện tử[40].Bởi vậy, nó cùngĐôngTổ hợp sau nhưng dùng làmHạch pin[40].
鍺 ít nhất có 27 loại hợp thànhTính phóng xạ chất đồng vị,Các nguyên tử chất lượng giới chăng 58 đến 89 chi gian. Giữa nhất ổn định chính là68Ge, này suy biến hình thức vìĐiện tử bắt được,Thời kỳ bán phân rãTắc vì 270.95d.Mà giữa nhất không ổn định còn lại là60Ge, này thời kỳ bán phân rã vì 30ms.Cứ việc đại bộ phận 鍺 chất đồng vị suy biến hình thức toàn vìβ suy biến,Nhưng là cũng có ngoại lệ.61Ge cập64Ge suy biến hình thức vìβ+Trì hoãnHạt nhân phóng ra( proton emission )[39],Mà84Ge đến87Ge tắc có khả năng tiến hànhβ-Trì hoãnNơ-tron phóng ra[39].
Tự nhiên phong độ[Biên tập]
鍺 là từHằng tinh hạch hợp thànhSở sáng tạo, chủ yếu là xuyên thấu quaTiệm gần siêu sao chi nhánhThượng hằng tinh nộiS- quá trình.S- quá trình là một loại chậmNơ-tronBắt được quá trình, phát sinh với mạch xungHồng siêu saoTrung nguyên tố nhẹ[41].Ở sao Mộc tầng khí quyển trung có thể phát hiện 鍺[42],Ở một ít xa xôi hằng tinh trung cũng có thể phát hiện 鍺[43].鍺Ở địa cầu vỏ quả đất phong độƯớc vì 1.6ppm[44].Hàm 鍺 lượng khả quan khoáng thạch chỉ có vài loại, nhưLưu bạc 鍺 quặng,Hôi 鍺 quặng( briartitie ),Lưu 鍺 mỏ đồng( germanite ) cậpLưu 鍺 thiết mỏ đồng( renierite ), mà chúng nó đều không có nhưng cung khai thác hầm mỏ. Cứ việc như thế, khai thác này đó khoáng thạch đều không phải vì chúng nó sở hàm 鍺[19][45].Một ít kẽm đồng chì quặng thể hàm 鍺 lượng đủ cao, bởi vậy có thể từ chúng nó cuối cùng áp súc khoáng vật trung lấy ra 鍺[44].
Nước ĐứcKhoáng vật học giảUy đặc · qua tư mật( Victor Goldschmidt ) ở đo lường 鍺 hầm mỏ khi, phát hiện một loại kỳ lạ áp súc quá trình, nó khiến cho một ítThan đáLớp quặng có thể có được cao hàm 鍺 lượng[46][47].Tối cao hàm 鍺 lượng xuất hiện ởAnh quốcNorthumberland quậnHeart lai thôn ( Hartley ) than đá hôi trung, đạt 1.6%[46][47].Nội Mông CổTích lâm làng thịPhụ cận mỏ than tầng hàm 鍺 lượng phỏng chừng đạt 1600Công tấn[44].
Chế bị[Biên tập]

2007 năm 鍺 năm sinh sản lượng ước vì 100Công tấn[19].Hiện tại, chủ yếu phương pháp là từ 鍺 độ dày đạt 0.3%Lóe kẽm quặngTrung lấy ra 鍺[48],Nó là giữa sản phẩm phụ, loại này khoáng thạch nhất thường xuất hiện với lấy trầm tích vật vi chủ thể đại hìnhZn-Pb-Cu(-Ba) hầm mỏ, cập lấyThan toan muốiVi chủ thể Zn-Pb hầm mỏ[44].Cứ việc không có toàn cầu 鍺 dự trữ lượng đích xác số thực tự, nhưng là phỏng chừng nước Mỹ dự trữ lượng ước ở 500 công tấn tả hữu[44].Ở 2007 năm, 鍺 nhu cầu lượng có 35% là từTuần hoàn tái tạoSở thỏa mãn[44].
鍺 chủ yếu là từLóe kẽm quặngTrung chế lấy, mà lóe kẽm quặng là một loạiKẽmKhoáng thạch, nhưng là cũng có thể ởBạc,ChìCậpĐồngQuặng trung tìm được 鍺. Nếu than đá nhà máy điện dùng than đá là từ cao 鍺 độ dày hầm mỏ tới nói, như vậy nhà máy điệnTro bụi( fly ash ) cũng là 鍺 một cái nơi phát ra.NgaCùngTrung QuốcĐều có ở dùng loại này 鍺 nguyên[49].Nga 鍺 hầm mỏ nằm ở này Viễn ĐôngKho trang đảo,MàVladivostokĐông Bắc mỏ than cũng bị dùng làm 鍺 nguyên[44].Trung Quốc 鍺 hầm mỏ chủ yếu nằm ởVân Nam tỉnhLâm thương thịThan nâuQuặng mỏ, cậpNội Mông Cổ khu tự trịTích lâm làng thịPhụ cận mỏ than, mà chúng nó đều là khai thác trung 鍺 nguyên[44].
| Niên đại | Giá cả ($/kg)[50] |
|---|---|
| 1999 | 1,400 |
| 2000 | 1,250 |
| 2001 | 890 |
| 2002 | 620 |
| 2003 | 380 |
| 2004 | 600 |
| 2005 | 660 |
| 2006 | 880 |
| 2007 | 1,240 |
| 2008 | 1,490 |
| 2009 | 950 |
鍺 đại bộ phận áp súc khoáng vật vìSunfua;Chúng nó ở trong không khí đun nóng sau sẽ biến thànhOxy hoá vật,Cái này quá trình kêuNung( roasting ):
- GeS2+ 3O2→ GeO2+ 2SO2
Ở cái này trong quá trình, bộ phận 鍺 sẽ đi vào sở sinh ra tro bụi trung, mà dư lại 鍺 tắc bị chuyển hóa thành 鍺 toan muối, sau đó bịAxítXối dung, lúc này ở xỉ than trung kẽm cũng bị xối dung. ỞTrung hoà phản ứngSau, chỉ có kẽm lưu tại dung dịch trung, lắng đọng lại vật trung đựng 鍺 cùng mặt khác kim loại. Ở dùngWill tư dã kẽm pháp( Waelz process ) đem lắng đọng lại vật trung hàm kẽm lượng giảm bớt sau, mà còn sót lại Will tư oxy hoá vật tắc tiếp thu lần thứ hai xối dung. Lúc này từ lắng đọng lại vật trung nhưng đếnNhị oxy hoá 鍺,CùngKhí CloHoặcHClPhản ứng sau bị chuyển hóa thànhBốn Clo hóa 鍺,Bởi vì nó điểm sôi thấp, bởi vậy nhưng dùngChưng cất phápTiến hành chia lìa[49]:
- GeO2+ 4HCl → GeCl4+ 2H2O
- GeO2+ 2Cl2→ GeCl4+ O2
Bốn Clo hóa 鍺 sẽ bị thuỷ phân thành nhị oxy hoá 鍺, hoặc dùngLọc phápTinh lọc sau lại bị thuỷ phân[49].Cực thuần GeO2Áp dụng với chế tạo 鍺 pha lê. Thuần nhị oxy hoá 鍺 cùng hydro phản ứng sau bị hoàn nguyên thành 鍺, dùng loại này hoàn nguyên phương thức đoạt được 鍺, áp dụng với tia hồng ngoại quang học hoặc chất bán dẫn công nghiệp:
- GeO2+ 4H2→ Ge + 2H2O
Dùng với sắt thép sinh sản cùng mặt khác công nghiệp quá trình 鍺, giống nhau sẽ dùng than tới hoàn nguyên[51]:
- GeO2+ C → Ge + CO2
Ứng dụng[Biên tập]
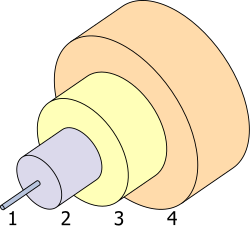
1. Trung tâm 8 µm
2. Bao tầng 125 µm
3. Giảm xóc tầng 250 µm
4. Hộ bộ 400 µm
鍺 ở 2007 năm phỏng chừng toàn cầu đầu cuối ứng dụng vì:Sợi quang họcHệ thống chiếm 35%,Tia hồng ngoại quang học( infrared optics ) chiếm 30%,Tụ hợpChất xúc tác chiếm 15%, cậpĐiện tửCùngNăng lượng mặt trờiPhát điện cũng chiếm 15%[19].Còn lại 5% vì mặt khác ứng dụng, nhưLân quang thể( phosphor ),Luyện kimCậpHóa học trị liệu[19].
Quang học[Biên tập]
Nhị oxy hoá 鍺Nhất đáng giá chú ý vật lý đặc tính, chính là nó caoChiết xạ suất,Cùng thấpSự tán sắc.Bởi vậy đặc biệt áp dụng vớiThấu kính wide,Kính hiển viCùngSợi quang họcTrung tâm[52][53].Nó càng thay thế đượcNhị oxy hoá thái,Trở thành silic oxit sợi quang học trung tâm trộn lẫn vật, như vậy liền không cần lại làm kế tiếpXử lý nhiệt,Mà loại này xử lý sẽ sử sợi quang học trở nên dễ toái[54].Ở 2002 năm mạt, sợi quang học công nghiệp chiếm nước Mỹ 鍺 dùng lượng 60%, nhưng chỉ chiếm toàn cầu dùng lượng không đến 10%[53].鍺 đễ đế ( GeSbTe ) là một loạiTương biếnHợp kim, lấy này quang học đặc tính xưng, ứng dụng ví dụ bao gồmNhưng trọng viết quang đĩa[55].
Bởi vìTia hồng ngoạiCó thể không tổn hao gì thất xuyên thấu 鍺, bởi vậy nó thành một loại quan trọng tia hồng ngoại quang học tài liệu, có thể thực dễ dàng bị cắt hoặc mài giũa thành thấu kính cập cửa sổ. Nó ở tia hồng ngoại quang học trung hạng nhất quan trọng ứng dụng, chính là chế tácNhiệt hình ảnh cameras( thermal imaging camera ) màn ảnh đồ tầng. Hàm 鍺 này một loại màn ảnh dùng vớiBước sóngVì 8 đến 14MicrometTia hồng ngoại, như vậy tia hồng ngoại nhưng dùng với bị động nhiệt thành tượng cập nhiệt điểm dò xét, bởi vậy có thể bị ứng dụng với quân sự, ô tôĐêm coiHệ thống cập phòng cháy[51].Như vậy màn ảnh còn có thể dùng với kính hiển viMáy đo quang phổ,Cùng mặt khác yêu cầu cực mẫn cảmTia hồng ngoại dò xétQuang học dụng cụ[53].鍺 loại này tài liệu có phi thường caoChiết xạ suất( 4.0 ), bởi vậy yêu cầu kháng phản xạ đồ tầng. Đặc biệt làLoại đá kim cương thanKháng phản xạ đồ tầng, đây là một loại đặc biệt cứng rắn đặc thù đồ tầng, này chiết xạ suất vì 2.0, cùng 鍺 tương nhược, hơn nữa sẽ sinh ra một tầng như kim cương cứng rắn mặt ngoài, đủ để đối mặt bên ngoài các loại khắc nghiệt hoàn cảnh[56][57].
Điện tử công nghiệp[Biên tập]
Bóng bán dẫn chủ yếu từ Germanium cùng khuê hai loại cao độ tinh khiết chất bán dẫn chế tác, mà Germanium bóng bán dẫn ( tên gọi tắt Germanium quản ) từng là bóng bán dẫn thời đại lúc đầu ( với 40 niên đại mạt bắt đầu ) quan trọng nhất chất bán dẫn sản phẩm, bởi vì lúc ấy chế tác cao thuần khuê cùng chế tạo khuê quản công nghệ đều không đủ thành thục. Germanium bóng bán dẫn so sánh với khuê quản, có B-E kết áp hạ thấp ( Germanium quản ước 0.2V, mà khuê quản vì 0.6V tả hữu ) ưu thế, nhưng là nhiệt ổn định tính tương đối kém, thả hưởng ứng tốc độ cực hạn rõ ràng không bằng khuê quản. Germanium quản đại quy mô ứng dụng đại khái liên tục đến 1970 năm tả hữu, từ nay về sau từ phát đạt quốc gia bắt đầu dần dần đào thải, đến 1980 năm, cơ hồ ở toàn thế giới phạm vi hoàn toàn bị khuê quản thay thế được mà rời khỏi điện tử công nghiệp[58].Nhưng mà, một ít âm hưởng người đam mê cho rằng Germanium quản có độc đáo âm sắc, tương đối với khuê quản “Lãnh ngạnh”, Germanium quản ấm áp thuần hậu thanh âm đặc tính bị một ít người chơi xưng là ‘ áp lực thấp bóng điện tử ’[59]Bởi vậy một ít sinh sản với 60 niên đại điện thanh thiết bị cùng linh kiện đến nay đã chịu bộ phận người chơi truy phủng, một ít âm nhạc dùng bàn đạpHiệu quả khíCòn ở dùng 鍺 bóng bán dẫn, bởi vì loại này hiệu quả khí có thể sinh ra lúc đầuRock and rollĐặc có “Mơ hồ” âm sắc, giữa nổi tiếng nhất chính là Dallas Arbiter công ty sở sinh sản Fuzz Face hiệu quả khí[60].
Sau lại điện tử tài liệu giới lại bốc cháy lên đối Germanium tài liệu hứng thú, bất quá đã không cực hạn với thuần Germanium tinh thể. 鍺 hóa khuê hợp kim ( giống nhau xưng là “Khuê 鍺”) chính cấp tốc mà trở thành một loại quan trọngChất bán dẫnTài liệu, dùng với cao tốcMạch điện hợp thành.Sử dụng Si-SiGe tiếp mặt mạch điện, bởi vì loại này tiếp mặt đặc tính, mà so chỉ dùng Si muốn mau đến nhiều[61].ỞVô tuyến thông tin( wireless communication ) trang bị trung, 鍺 hóa khuê chính bắt đầu thay thế đượcThân hóa gia[19].Có cao tốc đặc tính SiGe tinh phiến, có thể dùngKhuê tinh phiếnCông nghiệp truyền thống sinh sản kỹ xảo, cũng lấy chi phí rẻ sinh sản[19].
Theo nguồn năng lượng phí tổn dâng lên, khiến choNăng lượng mặt trời bảnKinh tế giá trị có điều đề cao, mà đây cũng là 鍺 một đại tiềm tàng ứng dụng[19].鍺 là vũ trụ dùng hiệu suất caoNhiều kết quang phục pinTinh viênCơ bản. Bởi vì 鍺Tinh cách hằng số( lattice constant ) cùngThân hóa giaGần, cho nên có thể dùng 鍺 cơ bản tới chế tạo thân hóa giaNăng lượng mặt trời pin[62].Hoả tinh dò xét dạo chơi giảCập mấy cáiVệ tinh nhân tạo,Đều có sử dụng 鍺 thượng tam liên điểm thân hóa giaPin[63].
Thượng 鍺 hạ vật cách điện cơ bản, có hi vọng có thể thay thế được mini tinh phiến trung khuê[19].Mặt khác điện tử ứng dụng còn bao gồmHuỳnh quang đènLân quang thể( phosphor )[23],Cập 鍺 cơ trạng thái cố địnhSáng lên nhị cực thể[19].
Mặt khác ứng dụng[Biên tập]
Ở sinh sảnTụ đối benzen nhị axit formic Ất nhị chỉTrong quá trình, nhị oxy hoá 鍺 còn có thể dùng vớiThôi hóaTụ hợpTác dụng[64].Như vậy sinh sản ra tới thành phẩm diệu độ rất cao, cho nên ởNhật BảnTiêu thụ PET cái chai đều chuyên môn tuyển dụng này một loạiTụ chỉ[64].Nhưng mà, nước Mỹ không đem 鍺 dùng làm tụ hợp chất xúc tác[19].Bởi vìSilic oxitCùng nhị oxy hoá 鍺 gần, cho nênKhí tương sắc phổTrụ trung cố địnhTươngSilic oxit, nhưng dùng nhị oxy hoá 鍺 tới thay thế được[65].
Năm gần đây, ởKim loại quýHợp kim trung gia nhập 鍺 là càng ngày càng nhiều. Tỷ như, ởAnh tệ tiêu chuẩn bạc( sterling silver ) ( hàm bạc lượng đạt 95% trở lên hợp kim ) trung gia nhập 鍺, là có thể giảm bớtHỏa văn( firescale ), gia tăng khángRỉ sắt sắcTính ( tarnish ) cập gia tăng đốiPhân ra cứng đờ( precipitation hardening ) phản ứng. Có một loại kháng rỉ sắt sắc bạc hợp kim, nhãn hiệu tên là Argentium, này hàm 鍺 lượng cần đạt 1.2%[19].
Cao độ tinh khiết 鍺 đơn tinh dò xét khí, có thể chuẩn xác mà dò xét ra phóng xạ nơi phát ra, bởi vậy nhưng dùng với sân bay bảo an hệ thống[66].鍺 cũng bị dùng vớiTinh thể đơn quang nghi( crystal monochromator ), này đài dụng cụ có thể sinh thànhĐơn tinhNơ-tron tản ra( neutron scattering ) cậpĐồng bộ X xạ tuyếnNhiễu xạ sở cần tuyến tính thúc. Ở nơ-tron cập năng lượng caoX xạ tuyếnỨng dụng, 鍺 phản xạ tính so khuê xuất sắc[67].Cao độ tinh khiết 鍺 tinh thể còn bị dùng vớiGià Mã quang phổ học( gamma spectroscopy ) cùng tìm kiếmÁm vật chấtDò xét khíTrung[68].
鍺 một ít hoá chất đốiBú sữa loạiĐộng vật không gì sao độc tính, chính là đối nào đóVi khuẩnTắc có tương đương độc tính[21].Liền bởi vì cái này đặc tính, cho nên này đó 鍺 hoá chất nhưng dùng làmHóa học trị liệuTề[69].
Đối sinh vật ảnh hưởng[Biên tập]
Giống nhau cho rằng 鍺 đối động thực vật khỏe mạnh cũng không quan trọng.[70]Bởi vì 鍺 ở khoáng thạch cùngThanChất tài liệu trung là một loại nguyên tố hiếm, hơn nữa ở thương nghiệp ứng dụng trung sử dụng lượng cũng không tính nhiều, cho nên nó đối tự nhiên cũng không có cái gì ảnh hưởng[19].
Germanium hoá chất bị dùng choBệnh bạch cầuCùngUng thư phổiThay thế liệu pháp[16],Nhưng không cóY học chứng minh thực tếChứng thực 鍺 chỗ tốt, thậm chí có chứng cứ cho thấy chúng nó có hại[70].Nước Mỹ thực phẩm dược phẩm giám sát quản lý cụcNghiên cứu kết luận cho rằng, đương 鍺 bị dùng làmĐồ ăn bổ sung tềKhi “Có khả năng nguy hại nhân thểKhỏe mạnh”[38].
Germanium bản thân không nguy hiểm, nhưng nào đó hoạt bát Germanium hoá chất có độc.[71]Tỷ nhưBốn Clo hóa 鍺CậpGiáp 鍺 hoàn,Phân biệt vì chất lỏng cập khí thể, có thể đôi mắt, làn da, phổi bộ cập yết hầu tạo thành rất lớn kích thích[72].Có chút Germanium hoá chất đốiĐộng vật có vúĐộc tính thấp, nhưng đốiVi khuẩnTới nói có độc.[21]
Tham kiến[Biên tập]
- Nguyên tố
- Bóng bán dẫn
- Than tộc nguyên tố
- Đệ 4 chu kỳ nguyên tố
- Nguyên tố bảng chu kỳ
- Chất đồng vị danh sách
Chú thích[Biên tập]
- ^“Nhật” cũng vì nguyên tố hoá họcLôiCũ dịch, nhân tạo thành lẫn lộn mà chọn dùng tân dịch.[73]
- ^Ở Hy Lạp ngữ trung, Argyrodite một từ có “Hàm bạc” ý tứ[74].
- ^Cùng đoán trước đến tân nguyên tố tồn tại giống nhau, toán học giaAdamsCùngLặc uy gia,Lợi dụngSao Thiên vươngQuỹ đạo bị kéo ra ngoài lệch lạc, ở 1843 năm trước sau liền đoán trước đến hành tinhHải vương tinhTồn tại[75].Charlie sĩ( James Challis ) với 1846 năm 8 nguyệt bắt đầu sưu tầm thứ tám viên hành tinh[76],MàThêm lặcTắc với 1846 năm 9 nguyệt 23 ngày chính thức quan trắc đến nó[77].
- ^Hermann ( R. Hermann ) ở 1877 năm công bố phát hiện chu kỳ tố trung vị với鉭Hạ nguyên tố, cũng lấy La Mã thần thoại hải vươngNeptuneMệnh danh là nã ( Naptunium )[78][79].Nhưng sau lại phát hiện loại nàyKim loạiChỉ là nguyên tốNiCùng 鉭Hợp kim[80].Thật lâu về sau,NãTên này cho ở bảng chu kỳ nằm ởUraniHạ hợp thành nguyên tố, nó là từHạch vật lýHọc giả ở 1940 năm sở phát hiện[81].
Tham khảo tư liệu[Biên tập]
- ^Prohaska, Thomas; Irrgeher, Johanna; Benefield, Jacqueline; Böhlke, John K.; Chesson, Lesley A.; Coplen, Tyler B.; Ding, Tiping; Dunn, Philip J. H.; Gröning, Manfred; Holden, Norman E.; Meijer, Harro A. J.Standard atomic weights of the elements 2021 (IUPAC Technical Report).Pure and Applied Chemistry. 2022-05-04.ISSN 1365-3075.doi:10.1515/pac-2019-0603( tiếng Anh ).
- ^Magnetic susceptibility of the elements and inorganic compoundsInternet hồ sơ quánLưu trữ,Lưu trữ ngày 2012-01-12., in Handbook of Chemistry and Physics 81st edition, CRC press.
- ^3.03.13.23.3Properties of Germanium.Ioffe Institute. ( nguyên thủy nội dungLưu trữVới 2012-01-25 ).
- ^M. Agostini; et al. Final Results of GERDA on the Two-Neutrino Double-β Decay Half-Life of76Ge. Physical Review Letters (American Physical Society (APS)). 2023-10-03,131(14).ISSN 0031-9007.doi:10.1103/physrevlett.131.142501.
- ^ Kaji, Masanori.D. I. Mendeleev's concept of chemical elements andThe Principles of Chemistry(PDF).Bulletin for the History of Chemistry. 2002,27(1): 4–16[2008-08-20].(Nguyên thủy nội dung(pdf)Lưu trữ với 2008-12-17 ).
- ^6.06.16.2Winkler, Clemens.Germanium, Ge, a New Nonmetal Element(English translation[Mất đi hiệu lực liên kết]).Berichte der deutschen chemischen Gesellschaft. 1887,19(1): 210–211.doi:10.1002/cber.18860190156.( nguyên thủy nội dungLưu trữVới 2012-10-13 )( tiếng Đức ).
- ^Germanium, a New Non-Metallic Element.The Manufacturer and Builder. 1887: 181[2008-08-20].( nguyên thủy nội dungLưu trữVới 2008-12-19 ).
- ^Winkler, Clemens.Mittheilungen über das Germanium.J. Prak. Chemie. 1886,34:177–229.doi:10.1002/prac.18860340122.( nguyên thủy nội dungLưu trữVới 2012-11-03 )( tiếng Đức ).
- ^9.09.19.29.3Winkler, Clemens.Mittheilungen über des Germanium. Zweite Abhandlung.J. Prak. Chemie. 1887,36:177–209[2008-08-20].doi:10.1002/prac.18870360119.( nguyên thủy nội dungLưu trữVới 2012-11-03 )( tiếng Đức ).
- ^Brunck, O. Obituary: Clemens Winkler. Berichte der deutschen chemischen Gesellschaft. 1886,39(4): 4491–4548.doi:10.1002/cber.190603904164( tiếng Đức ).
- ^de Boisbaudran, M. Lecoq.Sur le poids atomique du germanium.Comptes rendus. 1886,103:452[2008-08-20].( nguyên thủy nội dungLưu trữVới 2013-06-20 )( tiếng Pháp ).
- ^12.012.1Haller, E. E.Germanium: From Its Discovery to SiGe Devices(pdf).Department of Materials Science and Engineering, University of California, Berkeley, and Materials Sciences Division, Lawrence Berkeley National Laboratory, Berkeley,.[2008-08-22].( nguyên thủy nội dungLưu trữ(PDF)Với 2019-07-10 ).
- ^W. K.Germanium for Electronic Devices.NY Times. 1953[2008-08-22].( nguyên thủy nội dungLưu trữVới 2013-06-13 ).
- ^1941 - Semiconductor diode rectifiers serve in WW II.Computer History Museum.[2008-08-22].(Nguyên thủy nội dungLưu trữ với 2008-09-24 ).
- ^SiGe History.University of Cambridge.[2008-08-22].(Nguyên thủy nội dungLưu trữ với 2008-08-05 ).
- ^16.016.116.216.316.416.5Halford, Bethany.Germanium.Chemical & Engineering News (American Chemical Society). 2003[2008-08-22].( nguyên thủy nội dungLưu trữVới 2008-05-13 ).
- ^Bardeen, J.; Brattain, W. H. The Transistor, A Semi-Conductor Triode. Physical Reviews. 1948,74:230–231.doi:10.1103/PhysRev.74.230.
- ^Electronics History 4 - Transistors.National Academy of Engineering.[2008-08-22].(Nguyên thủy nội dungLưu trữ với 2007-10-20 ).
- ^19.0019.0119.0219.0319.0419.0519.0619.0719.0819.0919.1019.1119.1219.1319.14U.S. Geological Survey.Germanium—Statistics and Information.U.S. Geological Survey, Mineral Commodity Summaries. 2008[2008-08-28].( nguyên thủy nội dungLưu trữVới 2008-09-16 ).
Select 2008
- ^Teal, Gordon K.Single Crystals of Germanium and Silicon-Basic to the Transistor and Integrated Circuit(PDF).IEEE Transactions on Electron Devices. July 1976,ED–23(7): 621–639.doi:10.1109/T-ED.1976.18464.[Mất đi hiệu lực liên kết]
- ^21.021.121.2Emsley, John. Nature's Building Blocks. Oxford: Oxford University Press. 2001: 506–510.ISBN0-19-850341-5.Trích dẫn sai lầm: Có chứa name thuộc tính “nbb”
<ref>Nhãn dùng bất đồng nội dung định nghĩa nhiều lần - ^22.022.122.222.322.422.522.622.7Holleman, A. F.; Wiberg, E.; Wiberg, N. Lehrbuch der Anorganischen Chemie 102. de Gruyter. 2007.ISBN978-3-11-017770-1.OCLC 145623740.
- ^23.023.1Germanium.Los Alamos National Laboratory.[2008-08-28].(Nguyên thủy nội dungLưu trữ với 2008-06-10 ).
- ^Chardin, B. Dark Matter: Direct Detection. Binetruy, B. ( biên ). The Primordial Universe: 28 June - 23 July 1999. Springer. 2001: 308.ISBN3540410465.
- ^25.025.1Lévy, F.; Sheikin, I.; Grenier, B.; Huxley, Ad. Magnetic field-induced superconductivity in the ferromagnet URhGe. Science. 2005-08,309(5739): 1343–1346.PMID 16123293.doi:10.1126/science.1115498.
- ^Tabet, N. KRXPS study of the oxidation of Ge(001) surface. Applied Surface Science. 1998,134:275.doi:10.1016/S0169-4332(98)00251-7.
- ^27.0027.0127.0227.0327.0427.0527.0627.0727.0827.09Greenwood, N. N.; Earnshaw, A.Chemistry of the Elements2nd. Oxford:Butterworth-Heinemann. 1997.ISBN0-7506-3365-4.
- ^Tabet, N. XPS study of the growth kinetics of thin films obtained by thermal oxidation of germanium substrates. Journal of Electron Spectroscopy and Related Phenomena. 1999,. 101-103: 233.doi:10.1016/S0368-2048(98)00451-4.
- ^Xu, Li; Sevov, Slavi C. Oxidative Coupling of Deltahedral [Ge9]4−Zintl Ions. J. Am. Chem. Soc. 1999,121(39): 9245–9246.doi:10.1021/ja992269s.
- ^Bayya, Shyam S.; Sanghera, Jasbinder S.; Aggarwal, Ishwar D.; Wojcik, Joshua A. Infrared Transparent Germanate Glass-Ceramics. Journal of the American Ceramic Society. 2002,85(12): 3114–3116.
- ^Drugoveiko, O. P.Infrared reflectance and transmission spectra of germanium dioxide and its hydrolysis products.Journal of Applied Spectroscopy. 1975,22:191.doi:10.1007/BF00614256.
- ^Lightstone, A. W.; McIntyre, R. J.; Lecomte, R.; Schmitt, D. A Bismuth Germanate-Avalanche Photodiode Module Designed for Use in High Resolution Positron Emission Tomography. IEEE Transactions on Nuclear Science. 1986,33(1): 456–459.doi:10.1109/TNS.1986.4337142.
- ^Johnson, Otto H. Germanium and its Inorganic Compounds. Chem. Rev. 1952,3:431 – 431.doi:10.1021/cr60160a002.
- ^Fröba, Michael. First synthesis of mesostructured thiogermanates. Chemical Communications. 1997: 1729.doi:10.1039/a703634e.
- ^Beattie, I.R.; Jones, P.J.; Reid, G.; Webster, M. The Crystal Structure and Raman Spectrum of Ge5Cl12·GeCl4and the Vibrational Spectrum of Ge2Cl6.Inorg. Chem. 1998,37(23): 6032–6034.doi:10.1021/ic9807341.
- ^Satge, Jacques. Reactive intermediates in organogermanium chemistry. Pure & Appl. Chem. 1984,56(1): 137–150.doi:10.1351/pac198456010137.
- ^Quane, Denis; Bottei, Rudolph S. Organogermanium Chemistry. Chemical Reviews. 1963,63(4): 403–442.doi:10.1021/cr60224a004.
- ^38.038.1Tao, S. H.; Bolger, P. M. Hazard Assessment of Germanium Supplements. Regulatory Toxicology and Pharmacology. June 1997,25(3): 211–219.doi:10.1006/rtph.1997.1098.
- ^39.039.139.2Audi, G. Nubase2003 Evaluation of Nuclear and Decay Properties. Nuclear Physics A (Atomic Mass Data Center). 2003,729:3–128.doi:10.1016/j.nuclphysa.2003.11.001.
- ^40.040.1Alpha Fusion Electrical Energy Valve(PDF).Nu Energy Research Institute.[2008-09-10].(Nguyên thủy nội dung(pdf)Lưu trữ với 2008-10-01 ).
- ^Sterling, N. C.; Dinerstein, Harriet L.; Bowers, Charles W. Discovery of Enhanced Germanium Abundances in Planetary Nebulae with the Far Ultraviolet Spectroscopic Explorer. The Astrophysical Journal Letters. 2002,578:L55–L58.doi:10.1086/344473.
- ^Kunde, V.; Hanel, R.; Maguire, W.; Gautier, D.; Baluteau, J. P.; Marten, A.; Chedin, A.; Husson, N.; Scott, N. The tropospheric gas composition of Jupiter's north equatorial belt /NH3,PH3,CH3D, GeH4,H2O/ and the Jovian D/H isotopic ratio. Astrophysical J. 1982,263:443–467.doi:10.1086/160516.
- ^Cowan, John. Astronomy: Elements of surprise. Nature. 2003-05-01,423(29): 29.doi:10.1038/423029a.
- ^44.044.144.244.344.444.544.644.7Höll, R.; Kling, M.; Schroll, E. Metallogenesis of germanium—A review. Ore Geology Reviews. 2007,30(3–4): 145–180.doi:10.1016/j.oregeorev.2005.07.034.
- ^Lifton, Jack.Byproducts II: Another Germanium Rush?.Resource Investor. 2007-04-26[2008-09-09].(Nguyên thủy nội dungLưu trữ với 2007-06-12 ).
- ^46.046.1Goldschmidt, V. M.Ueber das Vorkommen des Germaniums in Steinkohlen und Steinkohlenprodukten.Nachrichten von der Gesellschaft der Wissenschaften zu Göttingen, Mathematisch-Physikalische Klasse. 1930: 141–167[2012-10-16].(Nguyên thủy nội dungLưu trữ với 2008-12-01 ).
- ^47.047.1Goldschmidt, V. M.; Peters, Cl.Zur Geochemie des Germaniums.Nachrichten von der Gesellschaft der Wissenschaften zu Göttingen, Mathematisch-Physikalische Klasse. 1933: 141–167[2012-10-16].(Nguyên thủy nội dungLưu trữ với 2008-12-01 ).
- ^Bernstein, L.Germanium geochemistry and mineralogy.Geochimica et Cosmochimica Acta. 1985,49:2409.doi:10.1016/0016-7037(85)90241-8.
- ^49.049.149.2Naumov, A. V. World market of germanium and its prospects. Russian Journal of Non-Ferrous Metals. 2007,48(4): 265–272.doi:10.3103/S1067821207040049.
- ^R.N. Soar.USGS Minerals Information.U.S. Geological Survey Mineral Commodity Summaries. 1977.2003-01,2004-01,2005-01,2006-01,2007-01,January 2010[2013-04-22].ISBN978-0-85934-039-7.OCLC 16437701.( nguyên thủy nội dungLưu trữVới 2013-05-07 ).
- ^51.051.1Moskalyk, R. R. Review of germanium processing worldwide. Minerals Engineering. 2004,17:393–402.doi:10.1016/j.mineng.2003.11.014.
- ^Rieke, G.H. Infrared Detector Arrays for Astronomy. Annu. Rev. Astro. Astrophys. 2007,45:77.doi:10.1146/annurev.astro.44.051905.092436.
- ^53.053.153.2Brown, Jr., Robert D.Germanium(pdf).U.S. Geological Survey. 2000[2008-09-22].( nguyên thủy nội dungLưu trữ(PDF)Với 2011-08-22 ).
- ^Chapter III: Optical Fiber For Communications.Stanford Research Institute.[2008-08-22].(Nguyên thủy nội dungLưu trữ với 2006-06-15 ).
- ^Understanding Recordable & Rewritable DVD First Edition(PDF).Optical Storage Technology Association (OSTA).[2008-09-22].(Nguyên thủy nội dung(pdf)Lưu trữ với 2009-04-19 ).
- ^Lettington, Alan H. Applications of diamond-like carbon thin films. Carbon. 1998,36(5–6): 555–560.doi:10.1016/S0008-6223(98)00062-1.
- ^Gardos, Michael N.; Soriano, Bonnie L.; Propst, Steven H. Study on correlating rain erosion resistance with sliding abrasion resistance of DLC on germanium. Proc. SPIE,. 1990,1325(Mechanical Properties): 99.doi:10.1117/12.22449.
- ^Lưu trữ phó bản(PDF).[2016-06-02].(Nguyên thủy nội dung(PDF)Lưu trữ với 2016-08-07 ).
- ^Lưu trữ phó bản.[2016-06-02].(Nguyên thủy nội dungLưu trữ với 2017-03-05 ).
- ^Szweda, Roy. Germanium phoenix. III-Vs Review. 2005,18(7): 55.doi:10.1016/S0961-1290(05)71310-7.
- ^Washio, K. SiGe HBT and BiCMOS technologies for optical transmission and wireless communication systems. IEEE Transactions on Electron Devices. 2003,50:656.doi:10.1109/TED.2003.810484.
- ^Bailey, Sheila G. Space and terrestrial photovoltaics: synergy and diversity. Progress in Photovoltaics Research and Applications. 2002,10:399.doi:10.1002/pip.446.
- ^Crisp, D.; Pathare, A.; Ewell, R. C. The performance of gallium arsenide/germanium solar cells at the Martian surface. Progress in Photovoltaics Research and Applications. 2004,54(2): 83–101.doi:10.1016/S0094-5765(02)00287-4.
- ^64.064.1Thiele, Ulrich K. The Current Status of Catalysis and Catalyst Development for the Industrial Process of Poly(ethylene terephthalate) Polycondensation. International Journal of Polymeric Materials. 2001,50(3): 387 – 394.doi:10.1080/00914030108035115.
- ^Fang, Li; Kulkarni, Sameer; Alhooshani, Khalid; Malik, Abdul. Germania-Based, Sol-Gel Hybrid Organic-Inorganic Coatings for Capillary Microextraction and Gas Chromatography. Anal. Chem. 2007,79(24): 9441–9451.doi:10.1021/ac071056f.
- ^Keyser, Ronald; Twomey, Timothy; Upp, Daniel.Performance of Light-Weight, Battery-Operated, High Purity Germanium Detectors for Field Use(PDF).Oak Ridge Technical Enterprise Corporation (ORTEC).[2008-09-06].(Nguyên thủy nội dung(pdf)Lưu trữ với 2007-10-26 ).
- ^Ahmed, F. U. Optimization of Germanium for Neutron Diffractometers. International Journal of Modern Physics E. 1996,5:131.doi:10.1142/S0218301396000062.
- ^Diehl, R. Astrophysical constraints from gamma-ray spectroscopy. Nuclear Physics A. 2006,777:70.doi:10.1016/j.nuclphysa.2005.02.155.
- ^Slavik, Milan; Blanc, Oscar; Davis, Joan. Spirogermanium: A new investigational drug of novel structure and lack of bone marrow toxicity. Investigational New Drugs. 1983,1(3): 225–234.doi:10.1007/BF00208894.
- ^70.070.1Germanium.American Cancer Society.[2008-08-31].(Nguyên thủy nội dungLưu trữ với 2008-06-10 ).
- ^Brown, Robert D. Jr.Commodity Survey:Germanium(PDF)( báo cáo ). US Geological Surveys.[2008-09-09].( nguyên thủy nội dungLưu trữ(PDF)Với 2018-03-04 ).
- ^Gerber, G.B.; Léonard, A. Mutagenicity, carcinogenicity and teratogenicity of germanium compounds. Regulatory Toxicology and Pharmacology. 1997,387:141–146.doi:10.1016/S1383-5742(97)00034-3.
- ^Nhật.Giáo dục bộ 《 chữ dị thể từ điển 》. ( nguyên thủy nội dungLưu trữVới 2015-06-20 ).
- ^Argyrodite—Ag
8GeS
6(pdf)( báo cáo ).Mineral Data Publishing.[2008-09-01].( nguyên thủy nội dungLưu trữ(PDF)Với 2008-12-19 ). - ^Adams, J. C.Explanation of the observed irregularities in the motion of Uranus, on the hypothesis of disturbance by a more distant planet.Monthly Notices of the Royal Astronomical Society (Blackwell Publishing). November 13, 1846,7:149[2008-02-18].( nguyên thủy nội dungLưu trữVới 2016-01-10 ).
- ^Challis, Rev. J.Account of observations at the Cambridge observatory for detecting the planet exterior to Uranus.Monthly Notices of the Royal Astronomical Society (Blackwell Publishing). November 13, 1846,7:145–149[2008-02-18].( nguyên thủy nội dungLưu trữVới 2016-01-10 ).
- ^ Galle, J. G. Account of the discovery of the planet of Le Verrier at Berlin. Monthly Notices of the Royal Astronomical Society. 13 November 1846,7:153.Bibcode:1846MNRAS...7..153G.
- ^Sears, Robert.Scientific Miscellany.The Galaxy (Columbus, O[hio]: Siebert & Lilley). 1877-07,24(1): 131.ISBN0665501668.OCLC 16890343.
- ^Editor's Scientific Record.Harper's new monthly magazine. 1877-06,55(325): 152–153[2012-10-09].( nguyên thủy nội dungLưu trữVới 2012-05-26 ).
- ^van der Krogt, Peter.Elementymology & Elements Multidict: Niobium.[2008-08-20].(Nguyên thủy nội dungLưu trữ với 2008-09-22 ).
- ^Westgren, A. The Nobel Prize in Chemistry 1951: presentation speech.Nobel Lectures, Chemistry 1942-1962.Elsevier. 1964. ( nguyên thủy nội dungLưu trữVới 2008-12-10 ).
Phần ngoài liên tiếp[Biên tập]
- Nguyên tố Germanium ởLạc tư a kéo mạc tư quốc gia phòng thí nghiệmGiới thiệu( tiếng Anh )
- EnvironmentalChemistry—— Germanium( tiếng Anh )
- Nguyên tốGermaniumỞThe Periodic Table of Videos( Nottingham đại học ) giới thiệu( tiếng Anh )
- Nguyên tố Germanium ởPeter van der Krogt elements siteGiới thiệu( tiếng Anh )
- WebElements – Germanium( tiếng Anh )
| Nguyên tố bảng chu kỳ(Loại kim loại) | |||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| IA 1 |
IIA 2 |
IIIB 3 |
IVB 4 |
VB 5 |
VIB 6 |
VIIB 7 |
VIIIB 8 |
VIIIB 9 |
VIIIB 10 |
IB 11 |
IIB 12 |
IIIA 13 |
IVA 14 |
VA 15 |
VIA 16 |
VIIA 17 |
VIIIA 18 | ||||||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |||||
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |||||
| |||||||||||||||||||||||||||||||||||||
| ||||||||||||