A-xít ribonucleic
Bổn điều mục tồn tại dưới vấn đề,Thỉnh hiệp trợCải thiện bổn điều mụcHoặc ởThảo luận trangNhằm vào đề tài thảo luận phát biểu cái nhìn.
|


A-xít ribonucleic( tiếng Anh:ribonucleicacid,Viết tắt:RNA) là một loại từHạch đường NucleotitThông qua3',5'- axit phosphoric nhị chỉ kiệnTụ hợp mà thành tuyến tính đại phần tử[1].Trong giới tự nhiên RNA thông thường là đơn liên, thả RNA trung cơ bản nhất bốn loạiKiềm cơViTuyến piu-rin( A ),Nước tiểu pirimidin( U ),Điểu piu-rin( G ),Bào pirimidin( C )[Chú 1],Tương đối, cùng RNA cùng vi acid nucleicDNAThông thường là song liên phần tử, thả này đựng hàm nitroKiềm cơ trung tướngRNANước tiểu pirimidinThay đổi vìNgực tuyến pirimidin( T ).
RNA có nhiều mặt công năng, nhưng ởDi truyền mã hóa,Chuyển dịch,Điều tiết khống chế,Gien biểu đạtChờ thêm trình trung phát huy tác dụng. Ấn RNA công năng, nhưng đem RNA phân vi nhiều loại loại hình. Tỷ như, ở tế bào sinh vật trung,mRNA( đưa tin RNA ) vi di truyền tin tức truyền lại giả, nó có thể chỉ đạoProteinHợp thành. Nhân vi mRNA có mã hóa protein năng lực, nó lại bị xưng vi mã hóa RNA. Mà mặt khác không có mã hóa protein năng lực RNA tắc bị xưng viPhi mã hóa RNA( ncRNA ). Chúng nó đi qua thôi hóa sinh hóa phản ứng, hoặc xuyên thấu qua điều tiết khống chế hoặc tham dựGien biểu đạtQuá trình phát huy tương ứng sinh lý công năng. Tỷ như,tRNA( đổi vận RNA ) ở chuyển dịch trong quá trình khởi đổi vận RNA tác dụng,rRNA( hạch đường thể RNA ) với chuyển dịch trong quá trình khởi thôi hóaChuỗi peptideHình thành tác dụng,sRNA( tiểu RNA ) khởi đến điều tiết khống chế gien biểu đạt tác dụng. Ngoài ra,RNA virusThậm chí lấy RNA làm vi chúng nó di truyền vật chất.
RNA thông thường từDNAĐi quaSang băngSinh thành. RNA ở tế bào trung rộng khắp phân bố, thật hạch sinh vậtNhân tế bào,Tế bào chất,Viên tuyến thểTrung đều có RNA[2]:36.
Cùng DNA tương đối
[Biên tập]
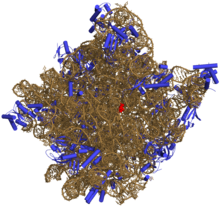
Cùng DNA tương tự, đại bộ phận có sinh vật hoạt tính RNA, bao gồm mRNA, tRNA, rRNA, snRNA, cùng với mặt khác một ít phi mã hóa RNA, tuy rằng là đơn liên, nhưng đựng tự mình bổ sung cho nhau danh sách, có thể khiến cho chúng nó có thể tiến hành gấp điệp[7],Hình thành bổ sung cho nhau song liên kết cấu ( hành ). Đối RNA phân tích cho thấy, chúng nó có tương đối càng phức tạp kết cấu. Cùng DNA bất đồng, RNA nhị cấp kết cấu cũng không phải đơn thuần song xoắn ốc, mà từ một loạt đoảnNhị cấp kết cấuCấu thành. Thông qua này đó đoản nhị cấp kết cấu tổ hợp, RNA thậm chí có thể có được cùng protein tương tự kết cấu, cũng giốngMôiNhư vậy thôi hóa phản ứng hoá học ( như vậy RNA bị xưng viHạch môi)[8].Tỷ như, đối hạch đường thể tiến hành phân tích cho thấy, này thôi hóa thành thái phản ứng hoạt tính vị điểm hoàn toàn từ RNA cấu thành[9].
| Hạng mục | DNA | RNA | Giải thích |
|---|---|---|---|
| Tạo thành thân cây chiĐường loạiPhần tử[10] | 2-Đi oxy hạch đườngCùngAxit phosphoric | Hạch đườngCùng axit phosphoric | |
| Khung xương kết cấu | Quy tắc[Yêu cầu so giai nơi phát ra][11]:50Song xoắn ốc kết cấu[12] | Đơn xoắn ốc kết cấu[Yêu cầu so giai nơi phát ra][12]HoặcHành hoàn kết cấu[13] | Tức khử ô-xy a-xít ribonucleic từ hai điều khử ô-xy Nucleotit liên cấu thành, mà a-xít ribonucleic từ một cái hạch đường Nucleotit liên cấu thành.[11]:49 |
| NucleotitSố | Thông thường thượng trăm vạn | Thông thường mấy trăm đến mấy ngàn cái | |
| Kiềm cơChủng loại[14][12] | Tuyến piu-rin( A )···Ngực tuyến pirimidin( T ) Bào pirimidin( C ) ···Điểu piu-rin( G ) |
Tuyến piu-rin( A ) ···Nước tiểu pirimidin( U ) Bào pirimidin( C ) ···Điểu piu-rin( G ) |
Trừ bộ phận ngoại lệ, DNA vì ngực tuyến pirimidin ( 5- nhóm methyl nước tiểu pirimidin ), RNA vì nước tiểu pirimidin, sử RNA càng dễ bị thuỷ phân. |
| Năm than đườngChủng loại[12] | Khử ô-xy hạch đường | Hạch đường | |
| Năm than đườngLiên tiếp tạo thành phân | Hydro nguyên tử | Gốc OH | ỞNăm than đườngCái thứ haiThanNguyên tử thượng liên tiếp tạo thành phân bất đồng. |
| Tồn tại với ( đối với thật hạch tế bào mà nói )[12] | Nhân tế bào( chút ít tồn tại vớiTuyến viên thể,Diệp lục thể) | Tế bào chất |
Kết cấu
[Biên tập]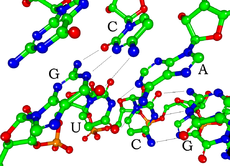
RNA đơn thể viHạch đường Nucleotit,Trong đó mậu đường viHạch đường,YHệ thống mệnh danh phápNhưng đem trong đó nguyên tử cacbon từ 1' đánh số đến 5'. Hàm nitro kiềm cơ cùng 1' nguyên tử cacbon tương liên. RNA trung cơ bản nhất bốn loại kiềm cơ phân biệt viA( tuyến piu-rin ),U( nước tiểu pirimidin ),G( điểu piu-rin ),C( bào pirimidin ). Trong đó, tuyến piu-rin cùng điểu piu-rin vi song hoànPiu-rin,Nước tiểu pirimidin cùng bào pirimidin vi đơn hoànPirimidin.Axit phosphoric gốc cùng một cái hạch đường tàn cơ 3' nguyên tử cacbon tương liên, cùng tiếp theo cái hạch đường Nucleotit 5' nguyên tử cacbon tương liên. Axit phosphoric gốc ở sinh lý pH hạ, cũng không đều có thể mang lên điện tích âm, cho nên RNA ở sinh lý điều kiện hạ là mang điện tích phần tử ( tụ i-on âm ). C cùng G, U cùng A, G cùng U chi gian có thể hình thành hydro kiện[15].Bất quá, kiềm cơ chi gian cũng có thể phát sinh mặt khác một ít hỗ trợ lẫn nhau. Tỷ như, ở một cái đột ra bộ phận trung, một đám tuyến piu-rin có thể cho nhau liên tiếp[16],GNRA bốn hoànTetraloopTrung có một cái G-A kiềm cơ đối[15].
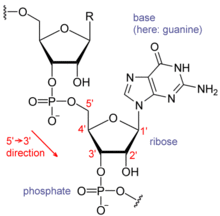
Hạch đường 2 vị than thượng liền có 羥 cơ vi RNA một cái quan trọng kết cấu đặc điểm. Loại này 羥 cơ khiến cho RNA song liên kết cấu ứng cùngA hình cấu tượngNhất tiếp cận[17],Bất quá, ở đơn liên nào đó nhị Nucleotit hoàn cảnh hạ, cũng có cực tiểu khả năng hình thành DNA nhất thường thấyB hình xoắn ốc cấu tượng[18].A hình cấu tượng khiến cho RNA song liên đại mương hẹp hòi mà thâm, tiểu mương thiển mà khoan[19].Ở RNA phần tử cấu tượng độ cao có thể biến đổi khu vực ( tức không sinh thành song liên kết cấu khu vực ), 2'-OH còn có thể công kích phụ cận axit phosphoric nhị chỉ kiện, khiến cho hạch đường - axit phosphoric liên đứt gãy[20].

Thông qua sang băng, gần có thể sử RNA liên thượng mang A, U, G, C bốn loại hàm nitro kiềm cơ[21]Bất quá, sang băng sau tân trang có thể thông qua nhiều loại con đường đối RNA tiến hành cải tạo. Tỷ như, sang băng sau tân trang có thể đem hi hữu kiềm cơGiả nước tiểu pirimidin( Ψ ) thêm đến RNA liên thượng. Giả nước tiểu pirimidin cùng hạch đường chi gian liên kết hoá học là C-C kiện mà không phải nước tiểu pirimidin ( U ) C-N kiện. Ngực tuyến pirimidin thêm đến RNA liên thượng tình hình cũng thực thường thấy ( nhất điển hình ví dụ là tRNA TΨC hoàn )[22].Mặt khác,Thứ hoàng piu-rinCũng là một loại thường thấy hi hữu kiềm cơ. Thứ hoàng piu-rin vi tuyến piu-rinThoát AmoniaSản vật, đựng thứ hoàng piu-rin hạch đại bị xưng vi cơ đại ( I ). ỞGien mã hóaĐong đưa giả thuyếtTrung, cơ đại có quan trọng tác dụng[23].
Trừ trở lên liệt ra ở ngoài, trải qua biên tập hạch đại còn có 100 nhiều loại[24].Từ tân trang dẫn phát kết cấu tính biến hóa ởtRNATrung nhất vi rõ ràng[25],Giả nước tiểu pirimidin cùng thường xuyên ở rRNA trung xuất hiện2'- giáp oxy cơ hạch đườngLà nhất thường thấy tân trang sản vật[26].Này đó tân trang cụ thể tác dụng còn không có hoàn toàn tỏ rõ. Bất quá, đáng chú ý chính là, ở rRNA trung, rất nhiều sang băng sau tân trang phát sinh ở độ cao công năng hóa khu vực, tỷ như thái cơ dời đi môi thôi hóa trung tâm cùng với á cơ kết hợp bộ vị, tựa hồ thuyết minh sang băng sau tân trang đối RNA phát huy bình thường công năng tới nói tương đương quan trọng[27].
Có thôi hóa công năng đơn liên RNA phần tử, cùng protein tương cùng loại, yêu cầu đặc thùRNA tam cấp kết cấu.Thông qua phần tử nội hydro kiện hình thànhNhị cấp kết cấuNguyên kiện cấu thành tam cấp kết cấu dàn giáo. Nhị cấp kết cấu hình thành rất nhiều nhưng phân biệt “Kết cấu vực” —— tỷ như hành hoàn kết cấu, to ra kết cấu ( bulges ),Nội hoàn kết cấu[28].Nhân vi RNA phần tử mang điện tích, không ít nhị cấp kết cấu cùng tam cấp kết cấu yêu cầuMg2+Chờ kim loại ly tử tới tiến hành ổn định[29].
Trong giới tự nhiên RNA đều là từ D- hạch đường Nucleotit tụ hợp mà thành D-RNA. Sử dụng L- hạch đường Nucleotit tắc nhưng hợp thành L-RNA. L-RNA đối RNA môi nại chịu lực muốn cường đến nhiều[30].
Hợp thành cùng tân trang
[Biên tập]RNA hợp thành giống nhau từ RNA tụ hợp môi thôi hóa.RNA tụ hợp môiLấy DNA vi khuôn mẫu, thông quaSang băngHợp thành RNA. Sang băng lúc đầu với RNA tụ hợp môi cùng khải động tử kết hợp ( khải động tử giống nhau nằm ở gien thượng du ). Nhân vi RNA tụ hợp môi tự mangGiải toàn môiHoạt tính, chỉ dựa vào RNA tụ hợp môi có thể thực hiện DNA song liên cởi bỏ. Sang băng trong quá trình, RNA tụ hợp môi lấy 3' đoan đến 5' quả nhiên phương hướng đọc lấy DNA khuôn mẫu liên, cũng lấy 5' đoan đến 3' quả nhiên phương hướng hợp thành cùng chi ngược hướng song song bổ sung cho nhau RNA liên. Sang băng ngưng hẳn từNgưng hẳn tửGiới đạo. Nguyên hạch sinh vật ngưng hẳn tử có hai loại: Đơn giản ngưng hẳn tử cùngρ ước sốỶ lại tính ngưng hẳn tử. Đơn giản ngưng hẳn tử chỉ dựa RNA hình thành nhị cấp kết cấu có thể ngưng hẳn sang băng, mà người sau ởρ ước sốDưới tác dụng mới có thể sử sang băng ngưng hẳn. Thật hạch sinh vật sang băng ngưng hẳn tắc cùngSang băng sau tân trangChặt chẽ tương quan[2]:323[31][32]:531-535.
Ở thật hạch sinh vật trung, RNAMới bắt đầu sang băng vậtThông thường sẽ trải quaSang băng sau tân trang.Tỷ như, thật hạch sinh vật mRNA phần lớn sẽ bị hơn nữaPoly(A) đuôi( nhiều tuyến piu-rin cái đuôi ) cùng với5' đoan mũ,mRNA trước thể trung đựng ở trong chứa tử danh sách cũng sẽ bịCắt nối thểCắt bỏ[32]:580-581.
Một ít RNA là từRNA phục chế môi( RNA ỷ lại tính RNA tụ hợp môi ) lấy RNA vi khuôn mẫu thôi hóa hợp thành. Nói ví dụ, RNA virus thông qua RNA phục chế môi phục chế này di truyền vật chất[33].Mặt khác, RNA phục chế môi cũng tham dự đông đảo sinh vật thểRNA can thiệpQuá trình[34].
Phân loại
[Biên tập]ỞTế bàoTrung, căn cứ kết cấu công năng bất đồng, RNA chủ yếu phân tam loại, tứctRNA,rRNA,Cùng vớimRNA.mRNA là căn cứ DNA danh sáchSang băngMà thànhProteinHợp thành khuôn mẫu; tRNA là mRNA thượngDi truyền mật mãPhân biệt giả cùngAxit aminĐổi vận giả; rRNA là tạo thànhHạch đường thểBộ phận, mà hạch đường thể là protein hợp thành máy móc.
Tế bào trung còn có rất nhiều chủng loại cùng công năng không đồng nhất loại nhỏ RNA, như là tạo thànhCắt nối thể( spliceosome )snRNA,Phụ tráchrRNAThành hìnhsnoRNA,Cùng với tham dựRNAiTác dụngmiRNACùngsiRNAChờ, nhưng điều tiết gien biểu hiện. Mà mặt khác như I, II hìnhỞ trong chứa tử,RNase P, HDV, hạch đường thể RNA từ từ đều có thôi hóa sinh hóa phản ứng quá trình hoạt tính, tức cóMôiHoạt tính, loại này RNA được xưng làHạch môi.
Điều tiết khống chế RNA
[Biên tập]Rất nhiều chủng loại RNA, có thể xuyên thấu qua cùng mRNA hoặc DNA thượng gien đoạn ngắn, bộ phận bổ sung cho nhau phương thức, tới điều hàng gien biểu hiện. Tỷ như ở thật hạch Heidi nt), có thể dẫn phát RNA quấy nhiễu. miRNA cùng enzim hợp lại thể, sẽ cắt nát mRNA, ngăn cản nên mRNA bị chuyển dịch, hoặc gia tốc này thoái biến.[35][36]
Tuy rằngTiểu quấy nhiễu RNA(siRNA; 20-25 nt) sinh ra, thông thường là từ phân giải virus RNA được đến, nhưng mà cũng tồn tại nội nguyên tính siRNA.[37][38]Mà siRNA dẫn phát RNA quấy nhiễu cơ chế cùng loại miRNA, có chút miRNA cùng siRNA, có thể tạo thành này mục tiêu gien bịNhóm methyl hóa,Do đóXúc tiếnHoặc ức chế nên gien sang băng..[39][40][41]Ngoài ra, ở động vật sinh sản tế bào nội, sở sinh độngPiwi-interacting RNA(piRNA; 29-30 nt), bị cho rằng có thể dự phòngChuyển đĩa,Cũng ở giao tử phát sinh thượng, sắm vai quan trọng nhân vật.[42][43]
Rất nhiều nguyên hạch sinh vật, cóCRISPR RNAs,Này tác dụng cơ chế cùng loại với thật hạch sinh vật RNA quấy nhiễu.[44]Trong đó phản nghĩa RNA(Antisense RNAs) là nhất thường thấy, đại đa số có thể điều hàng gien biểu hiện, nhưng cũng có thiếu bộ phận sẽ hoạt hoá sang băng tiến hành.[45]Phản nghĩa RNA tác dụng cơ chế chi nhất, là tạ từ cùng mRNA bổ sung cho nhau ghép đôi, tới hình thành hai đùi RNA, mà bị enzim thoái biến.[46]Ngoài ra, ở thật hạch tế bào nội, có lẽ nhiều có thể điều tiết khống chế gienPhi mã hóa RNA,[47]Một cái thường thấy ví dụ là Xist, nó sẽ bám vào giống cái động vật có vú trong đó một cái X nhiễm sắc thể thượng, tạo thành nàyĐi hoạt hoá.[48]
Một đoạn mRNA tự thân khả năng có chứa điều tiết khống chế thiết bị, tỷ như riboswitches, ở thứ năm đoan phi chuyển dịch khu (5' untranslated region) hoặc tam đoan phi chuyển dịch khu (3' untranslated region), bao hàm cóThuận thức tác dụng thiết bị(cis-regulatory elements) có thể điều tiết khống chế nên mRNA hoạt tính.[49]Ngoài ra, phi mã hóa khu thượng cũng có khả năng có chứa, có thể điều tiết khống chế cái khác gien điều tiết khống chế thiết bị.[50]
Tân trang cái khác RNA
[Biên tập]
Rất nhiều RNA sẽ trợ giúp tân trang cái khác RNA. NhưTrước người mang tin tức RNA(pre-mRNA) trungỞ trong chứa tử,Sẽ bị đựng rất nhiềuHạch tiểu RNA(snRNA)Cắt nối thểCắt nối.[6]Hoặc là RNA bản thân có thể làm hạch môi, cắt nối chính mình ở trong chứa tử.[51]
RNA thượng Nucleotit cũng có thể bị tân trang, biến thành phi A, U, G, C Nucleotit. Ở thật hạch tế bào trung, RNA thượng Nucleotit tân trang, thông thường là từ ởNhân tế bàoCùngTạp ha ngươi thểTrung phát hiện,Tiểu hạch nhân RNA(snoRNA; 60-300 nt) sở chủ đạo.[52]snoRNA sẽ liên kết enzim, cũng lấy kiềm cơ đối phương thức, dẫn đường chúng nó đi tiếp thượng RNA, lúc sau enzim liền bắt đầu RNA Nucleotit tân trang. Kiềm cơ tân trang rộng khắp phát sinh vớirRNACùngtRNATrung, nhưng màsnRNACùngmRNACũng có khả năng là kiềm cơ tân trang mục tiêu.[53][54]Ngoài ra, RNA cũng có thể bị nhóm methyl hóa.[55][56]
RNA gien tổ
[Biên tập]Giống như DNA, RNA cũng có thể mang theo di truyền tin tức.RNA virusGien tổTừ RNA tạo thành, có thể chuyển dịch ra nhiều loại protein, trong đó một ít phụ trách gien tổ phục chế, mà cái khác tắc làm bảo hộ cấu tạo, ở virus rời đi ký chủ tế bào sau, bảo hộ gien tổ.Loại virusLà một loại khác loại hình vi khuẩn gây bệnh, nhưng chúng nó chỉ từ RNA tạo thành, thả nên RNA cũng không sẽ chuyển dịch ra bất luận cái gì protein, cũng lợi dụng ký chủ tụ hợp môi tới phục chế.[57]
Nghịch chuyển lục
[Biên tập]Xoay ngược lại lục virusTạ từ đem RNAXoay ngược lại lụcTrở thành DNA, DNA phó bản lại sang băng vì RNA phương thức, tới phục chế bọn họ gien tổ.Xoay ngược lại lục chuyển đĩaCũng lợi dụng này phương pháp, tới phục chế DNA cùng RNA, lấy hoàn thành chuyển tòa.[58]Ngoài ra, thật hạch tế bào nộiĐoan viên môi,Cũng bao hàm một cái làm khuôn mẫu RNA, lợi dụng nó tới kéo dài nhiễm sắc thể đoan viên.[59]
Song liên RNA
[Biên tập]Song liên RNA(dsRNA) là chỉ có hai cái bổ sung cho nhau liên RNA, cùng tế bào trung DNA kết cấu tương tự, nó cũng là nào đóVirus( song liên RNA virus ) di truyền vật chất. Song liên RNA như virus RNA hoặcTiểu quấy nhiễu RNA(siRNA), có thể kích phátThật hạch sinh vậtRNA quấy nhiễu,Cùng vớiĐộng vật có xương sốngQuấy nhiễu tốPhản ứng.[60][61][62][63]
Giống nhau song liên RNA là một cái RNA gấp bổ sung cho nhau.
Phát hiện sử
[Biên tập]
Cùng RNA tương quan nghiên cứu, tạo thành rất nhiều sinh vật học phát hiện, cùng với giải Nobel. MàAcid nucleicVới 1868 năm từFred hi · MichellePhát hiện, lúc ấy hắn đem nên vật chất gọi “Hạch tố”, bởi vì nó là ở nhân tế bào trung bị tìm được.[64]Nhưng sau đó không lâu, nhà khoa học cũng ở không có nhân tế bào nguyên hạch sinh vật trung, cũng phát hiện acid nucleic. Ngoài ra, sớm tại 1939 năm liền có người hoài nghi, RNA ở protein hợp thành trung sở sắm vai nhân vật.[65]Tắc Vi la · áo kiều áCùngArthur · khoa ân Berg,Bởi vì ở phòng thí nghiệm nội phát hiện, có thể hợp thành RNA enzim, mà thu hoạch đến 1959 nămNobel sinh lý học hoặc y học thưởng[66]Nhưng mà, lúc sau nghiên cứu biểu hiện, từ bọn họ sở phát hiện enzimNhiều Nucleotit axit phosphoric hóa môi,Là phụ trách RNA thoái biến, mà phi RNA hợp thành.
Robert · William · hoắc lợiVới 1965 năm, phát hiện nấm men lớn nhỏ vì 77 cái Nucleotit tRNA danh sách,[67]Cũng với 1968 năm cùngHa ngươi · cát tân · khoa kéo nạpCùng vớiMarshall · ốc luân · ni luân BergCộng đồng đạt được Nobel sinh lý hoặc y học thưởng. Ở 1967 năm,Carl · ô tưPhỏng đoán RNA khả năng có thôi hóa năng lực, cũng đưa ra kiến nghị chỉ ra, sớm nhất sinh mệnh hình thức ( tự mình phục chế phần tử ) khả năng ỷ lại với RNA, tới mang theo di truyền tin tức cùng thôi hóa sinh hóa phản ứng, tứcRNA thế giới học thuyết.[68][69]
Xoay ngược lại lục virusCậpXoay ngược lại lục môi,Với 1970 niên đại lúc đầu bị phát hiện, làm mọi người hiểu biết đến RNA có thể bị xoay ngược lại lục vì DNA ( cùngTrung tâm pháp tắcTình hình chung, DNA sang băng vì RNA tương phản ). Cái này phát hiện, sửMang duy · Baltimore,La nạp thác · Duer bối khoaCùngHoward · Martin · đặc minh,Cộng đồng đạt được 1975 năm Nobel sinh lý học hoặc y học thưởng. Ngoài ra ở 1976 năm,Walter · PhilsCùng với hắn đoàn đội, đầu độ xác định RNA virus hoàn chỉnh gien tổ kiềm cơ danh sách ( phệ khuẩn thể MS2).[70]
Ở 1997 năm,Philip · hạ phổCùngLý sát · Roberts,Bởi vì phát hiện bú sữa loại động vật virus cập tế bào gien trung, cóỞ trong chứa tửThả sẽ phát sinhRNA cắt nối,Mà thu hoạch đến 1993 năm Nobel sinh lý học hoặc y học thưởng. Có thôi hóa công năng RNA (Hạch môi) ở 1980 niên đại lúc đầu bị phát hiện, mà khiến choThomas · thiết háchCùngSidney · Altman,Đạt được 1989 năm Nobel hóa học thưởng. Mà 1990 năm sở phát hiện ởBích đông gia thuộcThượng, dẫn vào gien sẽ lặng im thực vật thể tự thân tương tự gien hiện tượng, hiện nay bị cho rằng làRNA quấy nhiễuKết quả.[71][72]
Thả ước chừng ở đồng thời, lớn nhỏ ước 22 cái Nucleotit RNA( hiện tại được xưng làHơi RNA), bị phát hiện ởTuyến trùngPhát dụcThượng, sắm vai quan trọng nhân vật.[73]Mà với RNA quấy nhiễu nghiên cứu, làmAndrew · pháp áchCùngKhắc lôi cách · Merlot,Đạt được 2006 năm Nobel sinh lý học hoặc y học thưởng; mà cùng năm Nobel hóa học thưởng, từRoger · khoa ân BergĐạt được, đoạt giải nguyên nhân cũng cùng RNA tương quan ( ở RNA sang băng thượng nghiên cứu ). Ngoài ra điều tiết khống chế RNA phát hiện, thúc đẩy RNA dược vật khai phá, như lợi dụngTiểu quấy nhiễu RNATới lặng im mục tiêu gien.[74]
Tham kiến
[Biên tập]Chú thích
[Biên tập]- ^Thông qua sang băng sau tân trang, RNA khả năng sẽ mang lênGiả nước tiểu pirimidin( Ψ ) như vậy hi hữu kiềm cơ
Tham khảo văn hiến
[Biên tập]- ^David Hames & Nigel Hooper. Instant Notes in Biochemistry ( hướng dẫn đọc bổn ) 3rd. Khoa học nhà xuất bản. 2005: 193.ISBN978-7-03-025218-0.
- ^2.02.1Tra tích lương dược lập sóng.Sinh vật hóa học cùng phần tử sinh vật học thứ tám bản.Nhân dân vệ sinh nhà xuất bản. 2013.ISBN978-7-117-17214-1.
- ^RNA: The Versatile Molecule.University of Utah.2015[2016-08-17].( nguyên thủy nội dungLưu trữVới 2016-07-20 ).
- ^Nucleotides and Nucleic Acids(PDF).University of California, Los Angeles.[2016-08-17].(Nguyên thủy nội dung(PDF)Lưu trữ với 2015-09-23 ).
- ^R.N. Shukla.Analysis of Chromosomes.[2016-08-17].ISBN9789384568177.( nguyên thủy nội dungLưu trữVới 2020-03-24 ).
- ^6.06.1Berg JM, Tymoczko JL, Stryer L. Biochemistry 5th. WH Freeman and Company. 2002: 118–19, 781–808.ISBN0-7167-4684-0.OCLC179705944,48055706,59502128.
- ^I. Tinoco & C. Bustamante. How RNA folds. J. Mol. Biol. 1999,293(2): 271–281.PMID 10550208.doi:10.1006/jmbi.1999.3001.
- ^Higgs PG.RNA secondary structure: physical and computational aspects.Quarterly Reviews of Biophysics. 2000,33(3): 199–253.PMID 11191843.doi:10.1017/S0033583500003620.
- ^Nissen P; Hansen J; Ban N; Moore PB; Steitz TA. The structural basis of ribosome activity in peptide bond synthesis. Science. 2000,289(5481): 920–30.Bibcode:2000Sci...289..920N.PMID 10937990.doi:10.1126/science.289.5481.920.
- ^Berg J., Tymoczko J. and Stryer L. (2002)Biochemistry.W. H. Freeman and CompanyISBN 0-7167-4955-6
- ^11.011.1Tiết Kim Tinh. Trung học giáo tài toàn giải công cụ bản cao trung sinh vật bắt buộc 1 phần tử cùng tế bào. Thiểm Tây nhân dân giáo dục nhà xuất bản.ISBN9787545015751.
- ^12.012.112.212.312.4Nhân dân giáo dục nhà xuất bản.Sinh vật 1 bắt buộc phần tử cùng tế bào.ISBN9787107176708.
- ^Setubal, João Carlos. Meidanis, João. Introduction to computational molecular biology.Chủ biên Nhiếp lý.《 phần tử sinh vật học lời giới thiệu 》.World Pub. Corperation. 2003.ISBN7-5062-6574-5.OCLC 880306796.
- ^Sinh mệnh xoắn ốc -DNA cùng RNA.Quốc lập khoa học công nghệ viện bảo tàng.
- ^15.015.1Lee JC; Gutell RR. Diversity of base-pair conformations and their occurrence in rRNA structure and RNA structural motifs. J. Mol. Biol. 2004,344(5): 1225–49.PMID 15561141.doi:10.1016/j.jmb.2004.09.072.
- ^Barciszewski J; Frederic B; Clark C. RNA biochemistry and biotechnology. Springer. 1999: 73–87.ISBN0-7923-5862-7.OCLC 52403776.
- ^Salazar M; Fedoroff OY; Miller JM; Ribeiro NS; Reid BR. The DNA strand in DNAoRNA hybrid duplexes is neither B-form nor A-form in solution. Biochemistry. 1992,32(16): 4207–15.PMID 7682844.doi:10.1021/bi00067a007.
- ^Sedova A; Banavali NK. RNA approaches the B-form in stacked single strand dinucleotide contexts. Biopolymers. 2016,105(2): 65–82.PMID 26443416.doi:10.1002/bip.22750.
- ^Hermann T; Patel DJ. RNA bulges as architectural and recognition motifs. Structure. 2000,8(3): R47–R54.PMID 10745015.doi:10.1016/S0969-2126(00)00110-6.
- ^Mikkola S; Stenman E; Nurmi K; Yousefi-Salakdeh E; Strömberg R; Lönnberg H. The mechanism of the metal ion promoted cleavage of RNA phosphodiester bonds involves a general acid catalysis by the metal aquo ion on the departure of the leaving group. Perkin transactions 2. 1999, (8): 1619–26.doi:10.1039/a903691a.
- ^Jankowski JAZ; Polak JM. Clinical gene analysis and manipulation: Tools, techniques and troubleshooting. Cambridge University Press. 1996: 14.ISBN0-521-47896-0.OCLC 33838261.
- ^Yu Q; Morrow CD.Identification of critical elements in the tRNA acceptor stem and TΨC loop necessary for human immunodeficiency virus type 1 infectivity.J Virol. 2001,75(10): 4902–6.PMC 114245
 .PMID 11312362.doi:10.1128/JVI.75.10.4902-4906.2001.
.PMID 11312362.doi:10.1128/JVI.75.10.4902-4906.2001.
- ^Elliott MS; Trewyn RW. Inosine biosynthesis in transfer RNA by an enzymatic insertion of hypoxanthine. J. Biol. Chem. 1983,259(4): 2407–10.PMID 6365911.
- ^Cantara, WA; Crain, PF; Rozenski, J; McCloskey, JA; Harris, KA; Zhang, X; Vendeix, FA; Fabris, D; Agris, PF.The RNA Modification Database, RNAMDB: 2011 update.Nucleic Acids Research. January 2011,39(Database issue): D195–201.PMC 3013656
 .PMID 21071406.doi:10.1093/nar/gkq1028.
.PMID 21071406.doi:10.1093/nar/gkq1028.
- ^Söll D; RajBhandary U.TRNA: Structure, biosynthesis, and function.ASM Press. 1995:165.ISBN1-55581-073-X.OCLC 183036381.
- ^Kiss T.Small nucleolar RNA-guided post-transcriptional modification of cellular RNAs.The EMBO Journal. 2001,20(14): 3617–22.PMC 125535
 .PMID 11447102.doi:10.1093/emboj/20.14.3617.
.PMID 11447102.doi:10.1093/emboj/20.14.3617.
- ^King TH; Liu B; McCully RR; Fournier MJ. Ribosome structure and activity are altered in cells lacking snoRNPs that form pseudouridines in the peptidyl transferase center. Molecular Cell. 2002,11(2): 425–35.PMID 12620230.doi:10.1016/S1097-2765(03)00040-6.
- ^Mathews DH; Disney MD; Childs JL; Schroeder SJ; Zuker M; Turner DH.Incorporating chemical modification constraints into a dynamic programming algorithm for prediction of RNA secondary structure.Proc. Natl. Acad. Sci. USA. 2004,101(19): 7287–92.Bibcode:2004PNAS..101.7287M.PMC 409911
 .PMID 15123812.doi:10.1073/pnas.0401799101.
.PMID 15123812.doi:10.1073/pnas.0401799101.
- ^Tan ZJ; Chen SJ.Salt dependence of nucleic acid hairpin stability.Biophys. J. 2008,95(2): 738–52.Bibcode:2008BpJ....95..738T.PMC 2440479
 .PMID 18424500.doi:10.1529/biophysj.108.131524.
.PMID 18424500.doi:10.1529/biophysj.108.131524.
- ^Vater A; Klussmann S. Turning mirror-image oligonucleotides into drugs: the evolution of Spiegelmer therapeutics. Drug Discovery Today. January 2015,20(1): 147–155.PMID 25236655.doi:10.1016/j.drudis.2014.09.004.
- ^Nudler E; Gottesman ME. Transcription termination and anti-termination in E. coli. Genes to Cells. 2002,7(8): 755–68.PMID 12167155.doi:10.1046/j.1365-2443.2002.00563.x.
- ^32.032.1Jocelyn E.KREBS; et al. Gene XI. JONES&BARTLETT LEARNING( giáo dục cao đẳng nhà xuất bản xuất bản ). 2014.ISBN978-7-04-039649-2.
- ^Jeffrey L Hansen; Alexander M Long; Steve C Schultz. Structure of the RNA-dependent RNA polymerase of poliovirus. Structure. 1997,5(8): 1109–22.PMID 9309225.doi:10.1016/S0969-2126(97)00261-X.
- ^Ahlquist P. RNA-Dependent RNA Polymerases, Viruses, and RNA Silencing. Science. 2002,296(5571): 1270–73.Bibcode:2002Sci...296.1270A.PMID 12016304.doi:10.1126/science.1069132.
- ^Wu L, Belasco JG. Let me count the ways: mechanisms of gene regulation by miRNAs and siRNAs. Mol. Cell. January 2008,29(1): 1–7.PMID 18206964.doi:10.1016/j.molcel.2007.12.010.
- ^Matzke MA, Matzke AJM.Planting the seeds of a new paradigm.PLoS Biology. 2004,2(5): e133.PMC 406394
 .PMID 15138502.doi:10.1371/journal.pbio.0020133.
.PMID 15138502.doi:10.1371/journal.pbio.0020133.
- ^Vazquez F, Vaucheret H, Rajagopalan R, Lepers C, Gasciolli V, Mallory AC, Hilbert J, Bartel DP, Crété P. Endogenoustrans-acting siRNAs regulate the accumulation ofArabidopsismRNAs. Molecular Cell. 2004,16(1): 69–79.PMID 15469823.doi:10.1016/j.molcel.2004.09.028.
- ^Watanabe T, Totoki Y, Toyoda A,; et al. Endogenous siRNAs from naturally formed dsRNAs regulate transcripts in mouse oocytes. Nature. May 2008,453(7194): 539–43.Bibcode:2008Natur.453..539W.PMID 18404146.doi:10.1038/nature06908.
- ^Sontheimer EJ, Carthew RW. Silence from within: endogenous siRNAs and miRNAs. Cell. July 2005,122(1): 9–12.PMID 16009127.doi:10.1016/j.cell.2005.06.030.
- ^Doran G.RNAi – Is one suffix sufficient?.Journal of RNAi and Gene Silencing. 2007,3(1): 217–19. (Nguyên thủy nội dungLưu trữ với 2007-07-16 ).
- ^Pushparaj PN, Aarthi JJ, Kumar SD, Manikandan J.RNAi and RNAa — The Yin and Yang of RNAome.Bioinformation. 2008,2(6): 235–7.PMC 2258431
 .PMID 18317570.doi:10.6026/97320630002235.
.PMID 18317570.doi:10.6026/97320630002235.
- ^Horwich MD, Li C Matranga C, Vagin V, Farley G, Wang P, Zamore PD. TheDrosophilaRNA methyltransferase, DmHen1, modifies germline piRNAs and single-stranded siRNAs in RISC. Current Biology. 2007,17(14): 1265–72.PMID 17604629.doi:10.1016/j.cub.2007.06.030.
- ^Girard A, Sachidanandam R, Hannon GJ, Carmell MA. A germline-specific class of small RNAs binds mammalian Piwi proteins. Nature. 2006,442(7099): 199–202.Bibcode:2006Natur.442..199G.PMID 16751776.doi:10.1038/nature04917.
- ^Horvath P, Barrangou R.CRISPR/Cas, the Immune System of Bacteria and Archaea.Science. 2010,327(5962): 167–70[2013-04-14].Bibcode:2010Sci...327..167H.PMID 20056882.doi:10.1126/science.1179555.( nguyên thủy nội dungLưu trữVới 2010-07-23 ).
- ^Wagner EG, Altuvia S, Romby P. Antisense RNAs in bacteria and their genetic elements. Adv Genet. Advances in Genetics. 2002,46:361–98.ISBN9780120176465.PMID 11931231.doi:10.1016/S0065-2660(02)46013-0.
- ^Gilbert SF.Developmental Biology7th. Sinauer. 2003:101–3.ISBN0-87893-258-5.OCLC154656422,154663147,174530692,177000492,177316159,51544170,54743254,59197768,61404850.
- ^Amaral PP, Mattick JS. Noncoding RNA in development. Mammalian genome: official journal of the International Mammalian Genome Society. October 2008,19(7–8): 454–92.PMID 18839252.doi:10.1007/s00335-008-9136-7.
- ^Heard E, Mongelard F, Arnaud D, Chureau C, Vourc'h C, Avner P.HumanXISTyeast artificial chromosome transgenes show partial X inactivation center function in mouse embryonic stem cells.Proc. Natl. Acad. Sci. USA. 1999,96(12): 6841–46.Bibcode:1999PNAS...96.6841H.PMC 22003
 .PMID 10359800.doi:10.1073/pnas.96.12.6841.
.PMID 10359800.doi:10.1073/pnas.96.12.6841.
- ^Batey RT. Structures of regulatory elements in mRNAs. Curr. Opin. Struct. Biol. 2006,16(3): 299–306.PMID 16707260.doi:10.1016/j.sbi.2006.05.001.
- ^Scotto L, Assoian RK.A GC-rich domain with bifunctional effects on mRNA and protein levels: implications for control of transforming growth factor beta 1 expression.Mol. Cell. Biol. June 1993,13(6): 3588–97[2013-04-14].PMC 359828
 .PMID 8497272.( nguyên thủy nội dungLưu trữVới 2019-09-24 ).
.PMID 8497272.( nguyên thủy nội dungLưu trữVới 2019-09-24 ).
- ^Steitz TA, Steitz JA.A general two-metal-ion mechanism for catalytic RNA.Proc. Natl. Acad. Sci. U.S.A. 1993,90(14): 6498–502.Bibcode:1993PNAS...90.6498S.PMC 46959
 .PMID 8341661.doi:10.1073/pnas.90.14.6498.
.PMID 8341661.doi:10.1073/pnas.90.14.6498.
- ^Wirta W.Mining the transcriptome – methods and applications.Stockholm: School of Biotechnology, Royal Institute of Technology. 2006[2013-03-24].ISBN91-7178-436-5.OCLC 185406288.( nguyên thủy nội dungLưu trữVới 2016-03-04 ).
- ^Xie J, Zhang M, Zhou T, Hua X, Tang L, Wu W.Sno/scaRNAbase: a curated database for small nucleolar RNAs and cajal body-specific RNAs.Nucleic Acids Res. 2007,35(Database issue): D183–7.PMC 1669756
 .PMID 17099227.doi:10.1093/nar/gkl873.
.PMID 17099227.doi:10.1093/nar/gkl873.
- ^Omer AD, Ziesche S, Decatur WA, Fournier MJ, Dennis PP. RNA-modifying machines in archaea. Molecular Microbiology. 2003,48(3): 617–29.PMID 12694609.doi:10.1046/j.1365-2958.2003.03483.x.
- ^Cavaillé J, Nicoloso M, Bachellerie JP. Targeted ribose methylation of RNA in vivo directed by tailored antisense RNA guides. Nature. 1996,383(6602): 732–5.Bibcode:1996Natur.383..732C.PMID 8878486.doi:10.1038/383732a0.
- ^Kiss-László Z, Henry Y, Bachellerie JP, Caizergues-Ferrer M, Kiss T. Site-specific ribose methylation of preribosomal RNA: a novel function for small nucleolar RNAs. Cell. 1996,85(7): 1077–88.PMID 8674114.doi:10.1016/S0092-8674(00)81308-2.
- ^Daròs JA, Elena SF, Flores R.Viroids: an Ariadne's thread into the RNA labyrinth.EMBO Rep. 2006,7(6): 593–8.PMC 1479586
 .PMID 16741503.doi:10.1038/sj.embor.7400706.
.PMID 16741503.doi:10.1038/sj.embor.7400706.
- ^Kalendar R, Vicient CM, Peleg O, Anamthawat-Jonsson K, Bolshoy A, Schulman AH.Large retrotransposon derivatives: abundant, conserved but nonautonomous retroelements of barley and related genomes.Genetics. 2004,166(3): 1437–50.PMC 1470764
 .PMID 15082561.doi:10.1534/genetics.166.3.1437.
.PMID 15082561.doi:10.1534/genetics.166.3.1437.
- ^Podlevsky JD, Bley CJ, Omana RV, Qi X, Chen JJ.The telomerase database.Nucleic Acids Res. 2008,36(Database issue): D339–43.PMC 2238860
 .PMID 18073191.doi:10.1093/nar/gkm700.
.PMID 18073191.doi:10.1093/nar/gkm700.
- ^Blevins T; Rajeswaran, R.; Shivaprasad, P. V.; Beknazariants, D.; Si-Ammour, A.; Park, H.-S.; Vazquez, F.; Robertson, D.; Meins, F.; et al.Four plant Dicers mediate viral small RNA biogenesis and DNA virus induced silencing.Nucleic Acids Res. 2006,34(21): 6233–46.PMC 1669714
 .PMID 17090584.doi:10.1093/nar/gkl886.
.PMID 17090584.doi:10.1093/nar/gkl886.
- ^Jana S, Chakraborty C, Nandi S, Deb JK. RNA interference: potential therapeutic targets. Appl. Microbiol. Biotechnol. 2004,65(6): 649–57.PMID 15372214.doi:10.1007/s00253-004-1732-1.
- ^Schultz U, Kaspers B, Staeheli P. The interferon system of non-mammalian vertebrates. Dev. Comp. Immunol. 2004,28(5): 499–508.PMID 15062646.doi:10.1016/j.dci.2003.09.009.
- ^Kathryn A. Whitehead, James E. Dahlman, Robert S. Langer, Daniel G. Anderson.Silencing or stimulation? siRNA delivery and the immune system.Annual Review of Chemical and Biomolecular Engineering. 2011,2:77–96[2019-05-26].ISSN 1947-5438.PMID 22432611.doi:10.1146/annurev-chembioeng-061010-114133.( nguyên thủy nội dungLưu trữVới 2020-04-09 ).
- ^Dahm R. Friedrich Miescher and the discovery of DNA. Developmental Biology. 2005,278(2): 274–88.PMID 15680349.doi:10.1016/j.ydbio.2004.11.028.
- ^Caspersson T, Schultz J. Pentose nucleotides in the cytoplasm of growing tissues. Nature. 1939,143(3623): 602–3.Bibcode:1939Natur.143..602C.doi:10.1038/143602c0.
- ^Ochoa S.Enzymatic synthesis of ribonucleic acid(PDF).Nobel Lecture. 1959[2013-04-23].( nguyên thủy nội dungLưu trữ(PDF)Với 2011-08-23 ).
- ^Holley RW; Apgar, J.; Everett, G. A.; Madison, J. T.; Marquisee, M.; Merrill, S. H.; Penswick, J. R.; Zamir, A.; et al. Structure of a ribonucleic acid. Science. 1965,147(3664): 1462–65.Bibcode:1965Sci...147.1462H.PMID 14263761.doi:10.1126/science.147.3664.1462.
- ^Siebert S.Common sequence structure properties and stable regions in RNA secondary structures(PDF).Dissertation, Albert-Ludwigs-Universität, Freiburg im Breisgau: 1. 2006. (Nguyên thủy nội dung(PDF)Lưu trữ với 2012-03-09 ).
- ^Szathmáry E. The origin of the genetic code: amino acids as cofactors in an RNA world. Trends Genet. 1999,15(6): 223–9.PMID 10354582.doi:10.1016/S0168-9525(99)01730-8.
- ^Fiers W; Ysebaert, R.; Duerinck, F.; Haegeman, G.; Iserentant, D.; Merregaert, J.; Min Jou, W.; Molemans, F.; Raeymaekers, A.; et al. Complete nucleotide-sequence of bacteriophage MS2-RNA: primary and secondary structure of replicase gene. Nature. 1976,260(5551): 500–7.Bibcode:1976Natur.260..500F.PMID 1264203.doi:10.1038/260500a0.
- ^Napoli C, Lemieux C, Jorgensen R.Introduction of a chimeric chalcone synthase gene into petunia results in reversible co-suppression of homologous genes in trans.Plant Cell. 1990,2(4): 279–89.PMC 159885
 .PMID 12354959.doi:10.1105/tpc.2.4.279.
.PMID 12354959.doi:10.1105/tpc.2.4.279.
- ^Dafny-Yelin M, Chung SM, Frankman EL, Tzfira T.pSAT RNA interference vectors: a modular series for multiple gene down-regulation in plants.Plant Physiol. December 2007,145(4): 1272–81.PMC 2151715
 .PMID 17766396.doi:10.1104/pp.107.106062.
.PMID 17766396.doi:10.1104/pp.107.106062.
- ^Ruvkun G. Glimpses of a tiny RNA world. Science. 2001,294(5543): 797–99.PMID 11679654.doi:10.1126/science.1066315.
- ^Fichou Y, Férec C.The potential of oligonucleotides for therapeutic applications.Trends in Biotechnology. 2006,24(12): 563–70.PMID 17045686.doi:10.1016/j.tibtech.2006.10.003.
Phần ngoài liên tiếp
[Biên tập]- ( tiếng Anh )RNA World websiteLiên tiếp bách khoa toàn thư ( kết cấu, trắc tự, công cụ cùng tập san )
- ( tiếng Anh )Acid nucleic cơ sở dữ liệuNội có DNA, RNA cùng tương quan hoá chất hình ảnh.
| ||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||
